所有患儿均进行脉搏指数连续心输出量(PICCO)穿刺,常采用套管针辅助引导穿刺法或B超引导下钢针直接穿刺法。PICCO穿刺时应避免反复穿刺,及时换对侧穿刺或更换医生穿刺,必要时放弃穿刺;导管接头处注意旋紧,避免脱开。
麻醉管理
无肝前期麻醉管理 无肝前期属于病肝游离阶段,先天性胆道闭锁患儿前期已接受葛西手术,腹腔粘连严重、创面渗血多,肝移植术中患儿有意外大出血可能。针对患儿存在肝功能异常、低蛋白血症、凝血功能异常、代谢性酸中毒、电解质水平紊乱、贫血、循环容量不足的特点,麻醉管理重在积极扩容、改善贫血、纠正酸中毒和电解质水平紊乱。
无肝期麻醉管理 无肝期为供肝血管吻合阶段,活体肝移植主要吻合肝静脉和门静脉,DCD肝移植主要吻合肝上下腔静脉、肝下下腔静脉和门静脉。无肝期下腔静脉、门静脉阻断,造成心输出量降低和血压下降;肾脏低灌注少尿或无尿;下肢和内脏静脉回流受阻,无氧代谢增加,造成血乳酸水平升高;肝糖原分解代谢降低,糖异生降低,导致血糖降低。麻醉管理重在维持生命体征平稳,如无肝期循环容量相对不足,可应用血管活性药物;如无肝期循环容量绝对不足,用药同时可输注白蛋白扩容。同时维持体温正常,继续纠正酸中毒和电解质紊乱,平稳度过无肝期。
新肝开放期麻醉管理 活体肝移植开放下腔静脉、门静脉,DCD肝移植开放肝上下腔静脉、肝下下腔静脉、门静脉。患儿在新肝开放期经历如下病理生理变化:随着下腔静脉开放,回心血量增加,血压升高;门静脉开放,低温血液、酸性代谢产物回心,炎性细胞因子释放,进入心肺系统,抑制心肌收缩力,转而血压下降,心率减慢;电解质水平紊乱,易诱发心律失常。麻醉管理时应积极应用血管活性药物,维持患儿生命体征平稳,同时积极外科复温,对症处理高钾血症导致的心动过缓。
新肝期麻醉管理 新肝期手术特点为肝动脉吻合、胆肠吻合和外科止血,患儿新肝功能缓慢恢复。术前凝血功能差的患儿创面渗血严重,贫血、代谢性酸中毒和严重的电解质紊乱。麻醉管理要点为:每隔一小时复查一次血气分析,积极纠正酸中毒和电解质紊乱;改善贫血状态;动脉吻合结束后纠正凝血功能紊乱;维持循环稳定;保证肝脏、肾脏灌注,关注尿量。
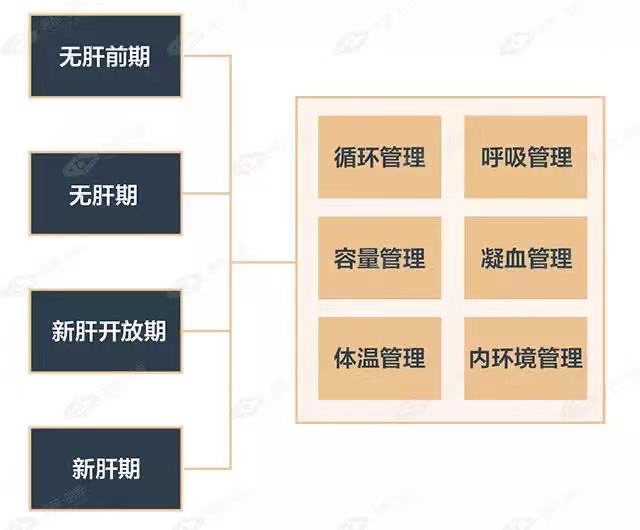
术中麻醉维持
术中维麻醉持采用静吸复合麻醉:舒芬太尼0.5~2μg/kg/h、罗库溴铵0.3mg/kg/h、右美托咪定0.2~1μg/kg/h、七氟醚1%~2%维持。
术中呼吸管理
气管插管后,通气是否恰当以听诊呼吸音、观察胸廓起伏度以及结合呼气末二氧化碳分压来确定;肝脏手术操作容易改变胸腔内压力,从而影响呼吸,需密切观察和及时调整;患儿体位变动后,需要再次确认气管导管和接口。呼吸首选压力控制通气(PCV)模式,潮气量设置为8~10ml/kg,分钟通气量(MV)为100~200ml/kg;吸气峰压一般维持在12~20cmH2O,最大不超过30cmH2O;呼吸频率为18~22次/分,吸呼比设置为1∶1.5;吸入氧浓度为60%~80%。
术中循环管理
术中常用监测项目为有创动脉压(ABP)、中心静脉压(CVP)、每博量变异度(SVV)、体循环阻力指数(SVRI)、全心舒张末期容积(GEDI)、血管外肺水指数(ELWI)和尿量。麻醉科医生应重视PICCO在肝移植术中的应用,因为肝移植手术不同阶段的容量管理需求并不同,麻醉科医生在关注外科手术操作和出血情况的同时,既要防止低血容量,又要防止容量过负荷,并合理应用血管活性药物。
术中液体管理
术中液体选择有晶体液、白蛋白、5%葡萄糖溶液、红细胞悬液、血浆。晶体液可选用乳酸林格氏液、醋酸林格氏液或生理盐水;白蛋白主要用于扩容,术前严重低蛋白血症、大量腹水的患者应适当增加白蛋白用量;5%葡萄糖溶液常规用量为100ml,后续依据血糖监测结果应用;血红蛋白(Hb)浓度<7g/dl时输注红细胞悬液,维持8g/dl<Hb<10g/dl;血浆输注用于严重凝血功能不全[凝血酶原时间(PT)>16秒]的患儿。一般情况较好的患儿,晶胶比为2∶1,低蛋白血症患儿,术中可适当增加白蛋白用量。
术中凝血功能监测
患儿术前凝血功能较差,长时间、大面积的创面渗血是肝移植手术出血多的主要原因,而且外科止血手段有限,因此,术中凝血功能监测非常重要。儿童肝移植术中强调“相对不凝”和“不能过凝”,这是因为肝动脉最细、极易栓塞,一旦肝动脉栓塞,手术也就失败了。术中强调血栓弹力图(TEG)全面监测凝血和纤溶全过程及血小板功能,应当加强TEG在肝移植术中的应用和指导作用。
▽ 儿童肝移植围术期处理
肝脏手术门静脉栓塞的预防
传统观点认为慢性肝病是一种获得性出血性疾病,但是于2011年发表在N Engl J Med的研究强调,不同慢性肝病患者的临床表现不同,抗凝与促凝血之间的失衡也会导致血栓形成,肝脏手术后部分患者可能发生门静脉栓塞。麻醉科医生应及时依据TEG监测结果,维持抗凝与促凝血之间的平衡。
肝硬化性心肌病
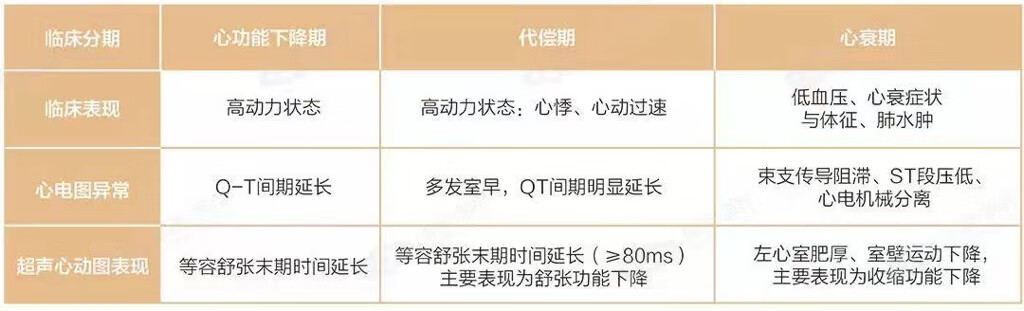
所有肝硬化患者都可能存在心肌病,且患者对于循环波动、内环境紊乱的代偿能力明显下降。肝硬化性心肌病分为三期(表):心功能下降期、代偿期和心衰期。针对大多数血管加压素水平较低的患者,单次静脉注射(3U)和持续输注(3U)血管加压素有效,SVR可增加33%;100mg亚甲蓝单次静脉注射可治疗肝移植术中对儿茶酚胺或血管加压素抵抗的低血压;部分学者尝试使用甘氨酸后叶加压素,处理肝硬化性心肌病。
表 肝硬化性心肌病临床分期
肝硬化患者的肺部疾患
肝肺综合征(HPS)和门脉高压相关肺动脉高压(PoPH)是肝硬化患者常见的肺部合并疾病,PoPH(阻力血管的收缩与重构)与HPS(微血管扩张与血管新生)有着不同的病理生理机制,但是两者一直被混用。PoPH有三个诊断标准:平均肺动脉压(MPAP)≥25mmHg、肺血管阻力(PVR)≥240dynes/s/cm5;肺动脉楔压(PAWP)<15mmHg,PoPH是进展性疾病,逐步发展成为右心衰,甚至导致死亡,围术期支持右心功能是供受体生存的关键。新肝再灌注后有一个不可预测的心输出量增加过程,可导致平均肺动脉压显著升高。PoPH具体处理流程见图。
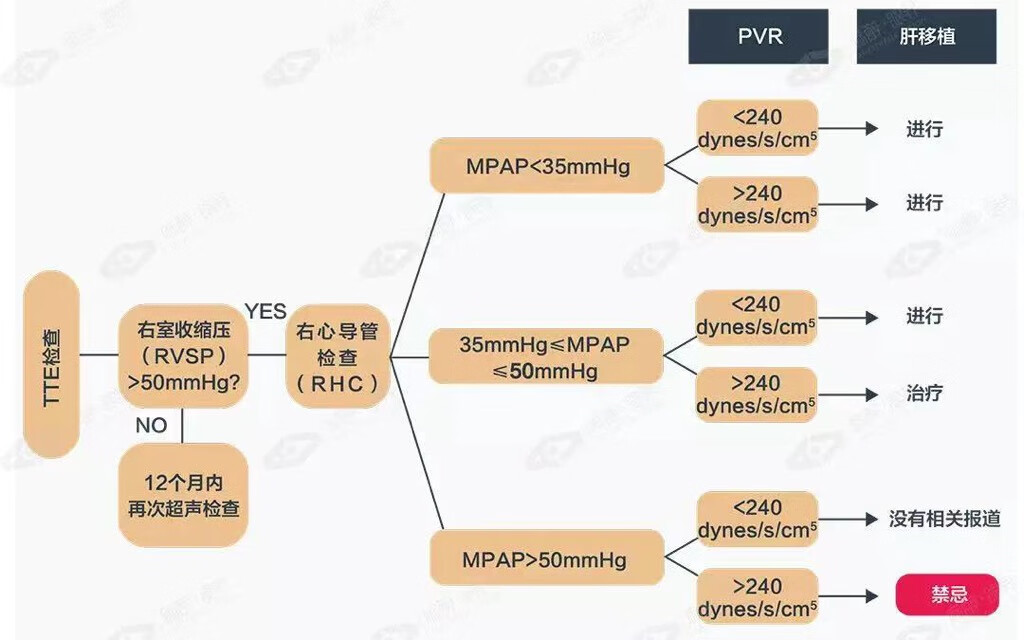
图 PoPH决策树
HPS临床表现为缺氧、紫绀、蜘蛛痣和直立性缺氧(Platypnea)-仰卧呼吸(Orthodeoxia)综合征。儿童肝硬化患者中HPS发病率为20%,HPS死亡率是同等严重肝硬化无HPS者的两倍。HPS无有效治疗药物,其处理原则为支持治疗维持动脉血氧分压(PaO2)在88%以上。
围术期急性肾功能不全
预先存在的肾功能损害、血流动力学不稳定、腔静脉受压和应用静脉-静脉转流、围术期出血和输血、炎症介质和再灌注期内皮功能障碍是肝移植围术期发生急性肾功能不全的危险因素。利尿剂、甘露醇治疗的肾保护作用尚无证据证实。大量随机对照研究和荟萃分析都不能证明传统肾保护剂多巴胺的益处,但是肾剂量多巴胺仍然在临床使用。
▽ 儿童肝移植临床研究
仁济医院麻醉科团队在儿童肝移植围术期管理领域开展了两项重要研究。第一项研究是于2020年发表在World J Gastronenterol、历时十年、纳入544例儿童肝移植病例的回顾性研究,研究者通过分析发现,2006年至2016年的十年间儿童肝移植总数逐年增加;术后患者死亡主要发生在术后3个月内;伴随着诊疗技术的发展,儿童肝移植术后总体生存率不断提高;通过多因素分析发现,重症监护病房(ICU)逗留时间、PELD评分、术前Hb水平是影响患儿术后一年生存率的独立危险因素,而ICU逗留时间、手术时长、PELD评分是影响术后三年生存率的独立危险因素。
第二项研究是研究团队借助430例儿童活体肝移植病例进行回顾性分析,探讨影响患儿预后的围术期危险因素、指标,并构建生存预测模型:患儿死亡主要发生在术后6个月内,死亡原因主要是移植物失功、脓血症、多器官功能障碍综合征(MODS)和严重肺炎等;通过多因素生存分析,研究者最终筛选出四个显著影响患儿预后和总体生存率的围术期危险因素,分别是移植物-受体体重比、PELD评分、中性粒细胞/淋巴细胞比值,以及术中是否使用去甲肾上腺素。
仁济医院麻醉科团队正在此领域进行其他多项临床研究,期待研究结果可以进一步指导儿童肝移植手术的围术期管理,改善患儿预后。

文章 围术期“理想”的循环管理 我们实现了吗?

俞卫锋
主任医师
上海交通大学医学院附属仁济医院
文章 麻醉学科:舒适化医疗实践之路

俞卫锋
主任医师
上海交通大学医学院附属仁济医院
文章 术前疼痛易化术后认知功能障碍

俞卫锋
主任医师
上海交通大学医学院附属仁济医院

