腹腔镜脾切除术简介
腹腔鏡脾切除术(Laparoscopic splenectomy,LS)是继腹腔镜胆囊切除术成熟起来的微创腔镜技术,虽然手术时间较开腹脾切除术(Open splenectomy OS)长,但具有创伤小、疼痛轻、恢复快、美观、住院时间短等微创手术的所有优点,已成为被外科医生和患者广泛接受的一种安全可行的脾切除新方法。由于脾脏血供丰富,位置深在,解剖关系复杂,腹腔镜脾切除术要求清晰解剖和彻底止血,技术难度远远大于腹腔镜胆囊切除术和开腹脾切除术,特别是对于脾脏巨大者。然而,自第一例腹腔镜脾切除开展以来,至今已有20余年的历史,腹腔镜手术先行者们积累了宝贵经验,为后来腹腔镜脾切除术的开展奠定了坚实基础。近年来,腹腔镜技术呈井喷式发展,腹腔镜脾切除技术已然成熟,并在各大医院逐渐得到广泛应用。本人结合目前国内外发表的文献、有关专著及个人体会概述如下。
一、LS的适应证
(1)血液病:主要是原发性血小板减少性性紫癜(ITP)和自身免疫性溶血性贫血,还有血栓性血小板减少性紫癜、毛细胞白血病、HIV相关性血小板减少性紫癜、镰状细胞贫血、β地中海贫血、遗传性球形红细胞增多症、Wiskoct-Aldrish 综合征等疾病。
(2)继发性脾功能亢进:如肝内型门静脉高压和肝外型门静脉高压合并脾功能亢进(脾动脉瘤、脾动静脉瘘、脾静脉血栓形成引起充血性脾肿大),系统性红斑狼疮并发脾亢等疾病的治疗;
(3)脾肿瘤:脾血管瘤、脾囊肿、脾恶性肿瘤;
(4)外伤性脾破裂;生命征平稳的外伤性脾破裂;
(5)脾感染性疾病:脾脓肿、脾结核。
二、LS的禁忌证
LS的绝对禁忌证为:
1、难以纠正的凝血机能障碍;
2、合并心、肺、肝、肾等重要脏器功能不全而不能耐受全麻的病人;
3、IV级外伤性脾破裂;
4、有上腹手术史导致腹腔严重粘连无法植入器械及显露脾脏。
相对禁忌证:
1、合并腹水;
2、合并妊娠;
3、巨脾(长径>20cm);
4、既往有上腹部手术史及高度肥胖。
随着腹腔镜手术技术的进步和设备的跟新,绝对禁忌证可转为相对禁忌证,相对禁忌证可转为适应证
三、LS的特殊术前准备
1、备好输血及中转开腹器械:脾脏血运丰富,血供复杂,拟行脾切除术的血液病病人又常合并血小板减少,因此脾切除过程中一旦发生大出血较难控制,LS时止血较OS更困难,因此LS术前除备足血液外,术中要保证术者随时可获得转开腹手术所需的器械。
2、术前应纠正凝血机制障碍和改善肝功能状态:如输注纤维蛋白原改善凝血技能,给予免疫球蛋白400mg/kg/d、血浆置换法可提高血小板数量;术前输注血小板可减少术中出血;尽可能在术前使肝功能达到Child-pugh A级。
3、有条件的病人可以主动免疫:术前2周给病人注射肺炎球菌、脑膜炎球菌疫苗,可减少术后感染发生率,这一术前准备尤其适用于婴儿、患地中海贫血的儿童和患肝病或淋巴瘤的成人;
4、对巨脾的病人手术当天术前应用脾动脉栓塞术:可使脾脏体积缩小、以减少术中出血。
四、LS的操作方法
1、术前置胃管胃肠减压,减小胃的体积,利于腹腔镜下观察。
2、麻醉与体位:全麻后病人取头高脚低、右侧卧位,使胃靠自身重力向右向下牵拉,利于显露脾胃韧带和脾门区。所谓“悬吊脾”技术的关键就是病人取右侧卧位同时左臂上抬,这样可较好地显露“悬吊”于膈上的脾。术者和第二助手站在病人右侧,第一助手站于病人左侧。也有主张病人取膀胱截石位,因为这种体位对右利手的术者来说手术操作更方便。
3、穿刺孔部位:多数作者采用四孔法或五孔法。即采用5mm、10mm、12mm的套管针在腹壁上打4~5个孔,打孔部位分别为:一个观察孔位于脐周,用来插入腹腔镜镜头;二个操作孔位于左中上腹(一般位于左锁骨中线平肚脐) 、左肋缘下(一般位于左腋前线,轴线经过脾门为佳),两者间距至少为12cm,用于分离、切断血管等主要操作,根据脾脏大小调整穿刺部位;另一个或二个位于剑突下及剑突与脐连线上(或稍偏左),主要用于牵拉胃和结肠,协助显露术野。对于脾脏巨大的病例,也可采取胰腺手术的五孔法。
4、建立人工气腹(气压2kPa)后插入腹腔镜探查:进入腹腔后先行探查,必要时可在超声引导下行细针活检;对淋巴瘤的病人行内窥镜超声检查有助于了解肝脏有无受累。然后开始在腹腔内寻找副脾,重点寻找部位是脾门、胰尾、网膜,仔细检查后再察看小肠、大肠的系膜、盆腔(包括Douglas窝,阔韧带、左腹股沟内环处),发现副脾时将其切除。
5、游离脾脏:自剑突下打孔处插入扇形牵开器向右侧牵拉胃或者由助手用无创钳将胃推向右侧,钝性分离加电凝、电切打开胃结肠韧带,先找到位于胰腺上缘的脾动脉主干。资料表明:脾动脉80%位于胰腺上缘偏后侧,8%位于胰腺后方,3%位于胰腺前方。脾动脉达到脾门时84%分为上下两支,16%分为上中下三支。在其发生分支之前用血管夹夹闭,或用体内(或体外)打结法将其缝扎,用牵开器将胃大弯向上方牵拉,显露出呈“窗帘”样或被上下牵直的胃短血管、脾上极和膈,靠近脾用血管夹夹闭、切断胃短血管,游离脾上极,用电切切断脾结肠韧带、脾肾韧带和脾膈韧带,随后分离、切断脾的韧带和血管,将脾脏游离。
6、处理脾蒂:如脾蒂血管为分散型则分别分离各脾段血管,用血管夹分别结扎、切断;如脾蒂血管为集中型则用Endo-GIA钉合器一并钉合后切断。无论用Endo-GIA钉合器还是用血管夹或体内(或体外)打结法,近侧的脾动脉断端均应双重结扎牢固、确切。脾脏切除后,彻底冲洗左上腹区,如发现有小的出血,用电凝止血。
7、取出脾脏:经腹壁打孔处送入非渗透性收集袋,打开后将脾脏移入袋中,将收集袋的开口经脐部打孔处提起,使其贴近腹壁,随后排出腹腔内二氧化碳,撤走脐部的套管,在脐部打孔处做一3~4cm的切口,通过这个切口用手指、剪刀或其他器械将脾脏搅碎后取出。如LS用于何杰金氏病的诊断分期,则需保证脾脏标本完整,以利做出病理诊断,此时需将腹壁切口延长至6~10cm,然后取出完整的脾脏。术毕置腹腔引流,便于观察术后腹腔内情况。术后可在腹壁打孔处用0.25%的盐酸利多卡因局部浸润注射可减轻术后疼痛。
五、术中应注意的问题
腹腔镜脾切除术的技术难点有三:控制出血、暴露脾上极、防止邻近的胃、结肠及胰腺副损伤。
1、根据脾脏大小和术者习惯,选择适当的操作孔位置,有利于手术操作。
2、探查需仔细,特别是仔细寻找副脾:ITP病人的副脾发生率约为20%,脾切除术后ITP复发的主要原因是术中遗留副脾,故LS术中应仔细探查腹腔,寻找副脾。副脾常见的部位依次为脾门,脾蒂血管区,腹膜后胰尾区,靠近胃大弯侧的大网膜,小肠、大肠的肠系膜,女性的左侧的阔韧带和Douglas窝以及男性的左侧睾丸附近。上述部位在LS术中能探查到的应尽力探查。取出脾脏后应对小网膜囊、胰尾、大网膜进行第二探查,严防遗留副脾。
3、术中有效控制出血是手术成败的关键所在。
术中出血的主要来源是脾动静脉、胃短血管、脾肾韧带后方异常曲张的血管及术中皮包膜破裂。大多数情况下,只要预先处理好脾动脉和胃短血管,一般都能保障手术顺利完成。一般来说,预先结扎脾动脉,然后根据具体情况结扎、切断胃短血管,即使术中脾脏包膜破裂有出血也只是切断脾脏血供的脾脏内残血流出而已,仍然可以保证手术安全进行。对于脾破裂者,应首先结扎脾动脉主干。对难以找到脾动脉主干者可采取脾下极入路脾蒂血流控制法控制脾脏血流,正如阻断肝蒂可以阻断入肝血流一样,阻断脾蒂可以阻断大部分入脾血流从而显著减少术中出血。
4、脾动脉的处理方法
73%的病人胰尾部距离脾门不到1cm,30%的病人胰尾紧贴脾门,因此分离脾门血管时注意勿伤及胰尾,尽量靠近脾被膜分离、切断脾动、静脉。脾血管可分为两型,①分散型(70%),特点是脾动脉主干短,其分出较长的4~6个分支进入脾门区;②主体型(30%),又称为集中型,特点是脾动脉主干长,其分出较短的2~4个分支进入脾门区。对主体型的脾血管适于用Endo-GIA钉合器,而对分散型的脾血管分支应逐一结扎或逐一用血管夹夹闭处理。
5.巨脾的处理
因LS取出脾脏的切口小,所以取脾的过程是手术的限速步骤。对巨大脾脏或脾上极粘连紧密,术中暴露上极困难,不要过于强调彻底有游离脾上极,可以先处理脾蒂,然后在处理脾上极的胃短血管及脾膈韧带。
6、术中脾脏显露的方法:前入路、前后入路、脾下极入路游离脾脏采用脾脏“抬起”法显露脾门,禁止牵拉和锐性器械钳夹,一避免脾脏破损。后外侧入路利用脾脏自身重力显露脾门。
7.脾切除后自腹腔内取出时应注意以下问题
①装脾的收集袋应结实,保证不会在搅碎的过程中破裂;
②收集袋应无渗透性,防止含脾组织的浆液外渗至腹腔内造成自体脾组织移植,而导致ITP复发;
③患ITP等血液病的病人术前多已经过激素治疗,40%以上的病人脾内含多种病原体,收集袋的破裂或渗透可能成为感染的重要原因。
8、手术操作应仔细、轻柔,避免锐性器械损伤脾脏,防止不必要的副损伤。
9、游离脾脏困难,出血多不易控制时应及时转开腹手术。
六、LS的并发症
1、出血:术中严重的并发症是因脾门血管损伤,脾撕裂等引起的大出血。术后出血分为早期出血和迟发性出血,早期出血因为血管结扎滑脱、止血不彻底、肝功能障碍致凝血机制不良等原因,迟发性出血常发生在肝功能障碍的病人。预防的措施是术前纠正凝血机制障碍,术中彻底止血,操作确实可靠。
2、膈下感染或脓肿:多继发于膈下积血,表现为术后3-4天体温突然增高,超声、CT等检查可放心膈下积液积脓。预防的措施在于术后充分的膈下引流。如已经形成脓肿,最佳措施是在超声引导下穿刺引流。
3、术后胰腺炎或胰瘘:少见,与术中损伤和刺激胰腺有关,临床上表现为左上腹剧痛,血淀粉酶增高、腹腔引流液淀粉酶高于血淀粉酶。预防的措施在于术中操作准确、轻柔,避免损伤胰腺。一旦发生胰腺炎或胰瘘,应充分引流,并用生长抑素治疗。
4、肺部并发症:肺不张和肺炎最常见,老年人更易发生,多为术中左膈肌受到刺激所致的反应性左侧胸腔积液。预防的措施在于术中尽可能减少对左侧膈肌的刺激。如胸腔积液影响到呼吸,则应行胸腔穿刺引流。
5、脾热:多为术后脾静脉残端血栓形成或并发感染发生脾静脉炎所致,脾切除术后病人免疫力低下也可引起感染。
5、术后肝功能不全甚至肝功能衰竭:术前病人合并肝硬化,肝代偿功能差,术后易于发生肝功能衰竭。一般术前肝功能Child-pugh A级发生肝衰竭的几率不大,Child-pugh C级则应视为手术禁忌症。一旦发生肝功不全,应积极保肝支持治疗,尽可能避免肝功能衰竭。
6、脾切除术后凶险感染(OPSI):全脾切除术后发生的特异性感染性并发症,终生均有发病的风险,但多发生于术后前2年,年龄越小发病越早,多为肺炎双球菌感染,也有其他病原菌的可能,开始可有轻度的流感样症状,短时间内发生高热、头痛、恶心、神志不清,甚至昏迷、休克,常在数小时内至十几小时内死亡。常并发DIC、菌血症。一旦发生,应积极采用大剂量抗生素控制感染、输血输液等抗休克治疗。该病发生率0.5%,死亡率50%。
7、ITP复发,须开腹切除副脾。因此,儿童全脾切除术应慎重考虑。
8、门静脉系统血栓形成:由于脾切除术后血小板迅速增高,超过500万/L时容易形成血栓,预防的措施是密切观察血小板变化,当血小板超过500万/L时应用抑制血小板聚集(祛聚)的药物进行预防,超过700万/L时,可以考虑低分子肝素预防血栓形成。一旦发现血栓形成,应立即进行溶栓、抗凝治疗。
9、切口感染、裂开。
10、胃、结肠、胰腺等邻近脏器损伤。
七、术后注意事项
针对上述并发症的防治,术后需注意如下方面:
1、观察生命体征,注意有无内出血发生;
2、术后胃肠减压2-3天,防止胃扩张;
3、对有肝硬化的病人,注意观察肝功能变化,加强支持、保肝治疗;
4、注意观察肾功能变化,防止肝肾综合征;
5、术后合理使用抗生素,防止膈下和腹腔感染。
6、检测血小板计数,防止门静脉系统血栓形成,血小板计数高于500万/L时要使用抑制血小板聚集的药物;有门静脉血栓形成史的病人必要时终身服用抗凝药。
八、LS的临床评价
LS优点:
1、创伤小、术后疼痛轻、术后麻醉药用量小、恢复快、住院时间短;
2、对有传染性疾病的病人,如HIV感染者,LS可减少手术人员被感染的机会;
3、手术后出现伤口并发症的机会相对较少。
LS也存在一些缺点:
1、手术时间长:LS最大的缺点是手术时间长,目前LS手术的最短时间为90min,平均为174和180min,而OS最短可以在30~40min完成。随着外科医生LS操作技术的熟练,LS手术时间可能会缩短;
2、脾脏取出费时:对巨脾、出血多或要求将脾标本较完整地自腹腔取出的病例,往往需要延长或另作切口,有时需中转开腹手术;
3、腹腔镜下手术缺乏接触内脏的手感,不利于寻找副脾,副脾残留可能导致术后血小板减少复发;
4、需使用穿刺器、切割闭合器、结扎夹等腔镜专用耗材,增加手术费用。
九、腹腔镜脾切除常见问题释疑
1、腹腔镜脾切除的技术关键是什么?
所有腹腔镜脾切除术的技术关键包括控制出血、游离脾脏、处理脾蒂,最为关键的技术是控制出血。腹腔镜脾切除控制出血的关键在于结扎脾动脉、妥善处理脾动静脉和胃短血管,首先应该控制脾动脉出血。
2、腹腔镜脾切除治疗ITP的机理是什么?如何判断其治疗效果?
目前LS最多用于ITP的病人,原因是①脾脏是血小板破坏的主要场所,也是ITP病人抗血小板抗体产生的重要脏器,ITP病人脾切除后至少有三分之二的人血小板可恢复并保持正常水平;②LS比较适合用于脾脏大小正常(长径<11cm)或轻、中度增大的病人,而ITP病人的脾脏多为大小正常或轻、中度增大,符合LS的条件。
对ITP的病人,脾切除治疗的有效标准为:①血小板绝对数大于100000/mm3;②术后、术前血小板计数比值大于、等于1.5;③术后毋须使用激素或γ球蛋白治疗。LS和OS治疗有效率接近。
3、腹腔镜脾切除术对于巨脾的治疗,术前、术中有何方法可以缩小脾脏?
(1)脾动脉栓塞:腹腔镜下游离巨脾比游离正常大小或轻、中度增大的脾脏更困难,故目前用LS方法切除巨脾的报道较少。Poulin报道了一LS切除长径为27cm、重量大于1000g巨脾的病例,方法是于手术当日晨行脾动脉栓塞术,使脾脏血供减少了95%,术中在耻骨上做一10cm长的腹部横切口,术者将前臂伸入腹腔,协助LS操作切下脾脏后,将其分解成几大块自下腹部的切口取出,彻底冲洗腹腔,避免发生脾组织移植,手术历时3小时,失血500ml,术后恢复良好。George主张脾动脉栓塞可于术中进行,这样可避免病人经历两次手术之苦。
(2)脾动脉主干结扎:术中最常规的方法是首先结扎脾动脉,阻断脾动脉血流,静脉血回流入肝,可有效地使脾脏缩小变软。
4、术中如何确定处理脾脏血管的顺序?
我们认为,首先应该在胰腺上缘分离结扎脾动脉以控制脾脏主要出血的来源,并使脾脏缩小变软,不易破裂。然后根据术中情况采取不同入路游离脾脏。前后入路可先断脾结肠韧带后将一个探条或肠钳置于脾门后,并将脾门抬起,这样有利于显露出脾门血管,由下至上分离脾的下极、上极和胃短血管,最后处理脾门血管;后外侧入路可依次游离切断脾结肠韧带游离脾下极,切断脾肾韧带游离脾门后方显露脾门血管,切断脾膈韧带和脾胃韧带游离脾上极并处理脾上极血管和胃短血管,在分离、切断胃短血管时如左肝外侧叶妨碍手术操作,可切开左肝三角韧带,将左肝外侧叶向右方牵开。如脾脏巨大,脾上、下极易于游离时可以采用脾下极入路脾蒂控制法预先控制脾蒂血流,在游离脾脏;如脾上下极均难于分离时,我们认为应采取前入路先处理脾门血管,然后根据具体情况处理从下而上或从上而下游离脾脏,不失为一种安全的脾切除方法。
5、腹腔镜脾切除各种手术入路的优势是什么?
(1)后外侧入路:采取后侧径路游离脾脏,主要依靠脾脏自身重力可达到清楚显露脾脏及脾门后方的目的,方便分离脾膈韧带,便于脾脏后方操作,从脾门背侧看到胰尾边缘,容易发现脾血管的走行和脾动脉分支类型,避免胰腺损伤,更有利于处理脾蒂,适用于脾上、下极易于分离的脾切除。缺点是探查腹腔或同时需行其他手术时需变换体位。
(2)脾下极入路:有作者称之为脾下极入路脾蒂控制法,方法是先游离脾下极,建立脾蒂下方隧道;再游离脾胃韧带,建立脾蒂上方隧道;然后将脾蒂上方隧道与下方隧道贯通建立脾蒂后方隧道,悬吊脾蒂,达到控制脾蒂,防止术中大出血。先处理脾动脉和脾蒂,然后自下而上、从前往后、由浅入深的原则,直视下安全可靠地结扎、切断脾周韧带,使脾脏得到充分游离。脾下极入路可以安全有效地建立脾脏后方隧道,控制脾蒂,适用于巨脾的切除。
(3)前入路:便于显露脾门和结扎脾动静脉。分层解剖脾蒂,可清楚显露脾门前方,无需过多搬动脾脏,减少术中意外损伤,缩短手术时间。特别适用于脾上下极严重粘连难于游离的脾切除,相当于原位脾切除。进行其他手术无需变换体位。缺点是处理脾脏膈面及显露脾蒂后方较困难,出血不易控制。
(4)前后入路:和开腹手术相同,结合前入路和后外侧入路的优点,可游离脾脏,清楚显露脾门,最后离断脾蒂。
6、腹腔镜脾切除中转开腹的原则是什么?中转开腹的主要原因有哪些?
腹腔镜脾切除中转开腹的原则是“生命安全第一,微创技术第二”,当微创手术危及病人生命安全或可能导致严重并发症时,必须当机立断中转开腹。中转开腹不是手术的失败,而是手术的延续,达到治疗目的才是手术成功的标志。中转开腹的常见原因有:
(1)脾蒂撕裂导致难以控制的大出血;
(2)胃短血管损伤导致难以控制的大出血;
(3)后腹膜异常扩张的静脉血管破裂出血难以控制;
(4)腹腔严重粘连无法显露脾脏与脾门;
(5)重要脏器损伤难以在腔镜下修复。
主要参考文献(略)
本文由作者上传,文章内容仅供参考。如有相关事宜可联系jdh-hezuo@jd.com
反馈

大家还在看
胃不舒服做胃镜,该做常规的还是无痛的?
#胃镜检查 #消化内科

赵彦鹏医生

腹部疾病术后护理要点
#康复训练 #患病护理

周宁医生
一文解惑腰椎穿刺术

京东健康
胃镜能发现哪些胃病,哪些人不适合无痛胃镜?
#检查 #消化内科

副主任医师丁彬彬
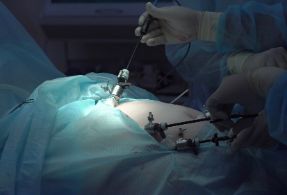
“外科的圣母峰”胰脏癌该怎么手术?我们首推腹腔镜
#疾病概述 #手术治疗

周宁医生
术前术后的多重讲究:关于扁桃体切除术你知道些什么?
#疾病概述 #疾病检查 #患病护理 #耳鼻喉头颈外科 #手术治疗

我是大医生

阴茎勃起困难吃药能好吗?
#男性健康 #概述 #男科

医联媒体

血脂高的人怎么吃?
#饮食营养 #疾病概述 #心血管内科 #营养治疗

美珍健康课堂

晨起恶心,是怎么回事?这个症状不能忽视
#疾病概述 #疾病预防 #耳鼻喉头颈外科

周宁医生
如果肾结石不疼,还需要摘除吗?
#疾病概述 #肾病内科 #手术治疗 #其他治疗

泌尿外科陆巍
医院推荐专家
地区推荐专家
患友问诊
*本站内容仅供医学知识科普使用,任何关于疾病、用药建议都不能替代执业医师当面诊断,请谨慎参阅


0
0
0