
皮肤的原发性损害主要有 8 点,对人体的上海相对比较大。
1)斑疹:
皮肤黏膜的局限性颜色改变,皮损与周围平齐,无隆起或凹陷。
- 直径一般小于 2cm,大于 2cm 时称斑片。
- 分为红斑、出血斑、色素沉着及色素减退斑等。
- 出血斑直径小于 2mm 时称瘀点,大于 2mm 时称瘀斑。
2)斑块:
为直径大于 1 cm 的隆起性、浅表性皮损,顶端较扁平,多为丘疹扩大或融合而成。
3)丘疹:
为限局性、充实性、浅表性皮损,隆起于皮面,直径小于 1 cm。
- 形态介于斑疹与丘疹之间的稍隆起皮损称斑丘
- 丘疹顶部有小水疱时称丘疱疹;
- 丘疹顶部有小脓疱时称丘脓疱疹。
4)风团:
为暂时性、隆起性皮损,由真皮乳头层血管扩张、血浆渗出所致。皮损发生快,消退快,消退后不留任何痕迹。
5)水疱和大疱:
水疱为高出皮面、内含液体的限局性、腔隙性皮损。
- 直径一般小于 1 cm,大于 1 cm 者称大疱。
- 内容物含血液者称血疱。
6)脓疱:
为高出皮面,内含脓液的局限性、腔隙性皮损。
7)结节:
为局限性、实质性、深在性皮损,位置可深达真皮或皮下,可由炎症浸润或代谢物沉积所致。
8)囊肿:
为含有液体、半固体粘稠物或细胞成分的囊性皮损,一般位于真皮或更深位置,可隆起于皮面或仅可触及。
梅毒是一种危害性极大的性传播疾病,是由梅毒螺旋体感染引起,主要通过性交、从母体通过胎盘传入,引起多器官的慢性传染性的疾病。
人是梅毒的唯一的传染源,通过性传播占 95%以上,未经治疗的患者一般在一到两年内具有强烈的传染性。随着时间延长,传染性会越来越小。感染两年以上传染性较小。
第二,通过胎盘传染。妊娠期内梅毒螺旋体通过胎盘以及脐静脉感染给胎儿。
第三,产道传染。梅毒孕妇在分娩时新生儿通过产道感染时发生感染。
还有非接触性传染,少数患者可以与梅毒患者皮肤黏膜发生非性接触的直接接触引起传染,如普通的接吻,握手,妇科检查,哺乳等。
输血也会引起梅毒的传染,个别患者因输入有传染性的梅毒患者的血液而被感染。
少数患者还可能因为接触带有梅毒螺旋体的内衣,被褥,毛巾,剃须刀以及医疗器戒间接感染,但这种现象病例极少。
通过切断传染源的途径,我们就可以起到预防梅毒的作用,保持身体的健康,注意个人卫生。

怎么样来判断有没有得梅毒,或者是得了梅毒以后病情的严重程度,那么通常我们用的方法是抽血来查梅毒的抗体。梅毒的抗体有两大类,一类是特异性抗体,通常是 TPPA 或者是 TPHA,还有是非特异性抗体,通常我们叫 RPR 或者是 TRUST。这些方法在不同的人身上和不同的时间,检测的具体的要求会有些不一样,这个需要有经验的医生来帮你安排。
大致说一下 TPPA、TPHA、RPR 和 TRUST,它们之间的关系,因为这几个指标是经常用到的,特异性抗体里边有个 TPPA 和 TPHA,这两个指标实际上是一样的意义,只是在用的试剂方面,略微有一点点差别,我们可以认为这两者是相等的。也就说 TPPA 等于 TPHA,这两个都指的是特性的抗体,它们的意义一旦你得过梅毒,只要是您得过,不管你好了还是没有好,TPPA 是持续阳性。
那 RPR 和 TRUST,它们俩其实也是相等的,也是有细微的差别,但是可以理解完全一样,它们的比值也是可以互换的,也就是说 RPR1: 4,和 TRUST 的 1: 4 是相等的。那么这种非特异性的抗体,主要用于判断,梅毒这个病得了以后,它的严重程度。它的指标一般是用,1: 1、1: 2、1: 4、1: 8 这种比值,并且翻倍增长的这种比值来表示,1: 8、1: 4 相比,1: 8 病情更严重一些,1: 4 更轻一些,最好的就是 1: 2、1: 1,最好降到阴性。
那么判断到底有没有治好,就是看最后非特异性抗体里边,RPR 指标能不能降到阴性,而特异性抗体,一旦感染了梅毒,它是终身阳性的,其实只需要测一次就可以。以后再测若干次,再测它滴度的高低,其实没有什么意义,只需要测一次,认为它有就可以了。
梅毒是由梅毒螺旋体感染所引起的一种常见性传播疾病,可以造成全身多组织器官的损伤,如果能早期发现,及时的治疗,预后还是比较好的,但是如果没有及时的治疗或者不正规的治疗,梅毒有可能会导致严重的后果,尤其是晚期梅毒会造成心血管、脑血管或者其他组织器官严重的损伤,治疗的难度非常的大,甚至部分病例会危及到患者的生命,对患者的身心产生严重的影响性,此时的梅毒是一种严重的临床疾病。
无论是梅毒还是淋病,都要给予足够的重视,正规的治疗,相对于梅毒来说,淋病的预后更好,疾病更为容易处理,导致严重后果的机会更少,但是不应该放松警惕,因为此类疾病容易造成传播,尤其是家庭内部的传播,有一定的危害性,都应该给予足够的重视,加强预防以及正规的治疗。
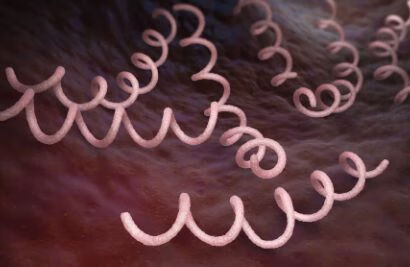
梅毒螺旋体
梅毒螺旋体感染是传统经典性病之一,也是一种全球性性传播疾病。近二、三十年,我国发病率有上升趋势。
梅毒螺旋体可使胎儿受到感染,致使新生儿发生脓毒血症而死亡,侥幸存活者也可能是先天性梅毒患者,即使儿童期无症状,到青春期可表现为梅毒三期。
孕前进行梅毒螺旋体抗体检测,阳性者需进一步确诊,及时治疗,治愈后再怀孕。如果孕早期感染,应在孕 16 周前接受正规治疗。
前几天,某大 V 和前妻因为离婚战在网上撕破脸皮,甚至前妻爆出该大 V 的私生活引起众多网友唏嘘不已。
而梅毒的这种疾病也引起了网友们的关注,同时也让不少人对这种传染病又有了新的认识。
大家对于“梅毒”并不陌生,它是性病的代表之一,主要通过梅毒螺旋体感染人体。
当被感染梅毒之后,这种病毒不仅会侵犯我们的生殖器官和皮肤,同时还会对全身各处器官造成伤害,从而出现多种症状和体征。
也即是说,人体一旦被感染梅毒,就意味着接下来的日子会不停的和梅毒做斗争。
梅毒有哪些传播途径?
梅毒既然是性病之一,所以当患上梅毒之后,大家首先就会想到不洁净的性生活。
其实不洁净的性生活只是梅毒传播的途径之一,除此之外,还有血液传播、母婴传播。
也就是说,即便你是乖乖女,没有不洁净性生活,依然有可能被感染梅毒。
这些方式也有可能让你感染梅毒
1.半永久美容
现在非常流行半永久的美容方式,比如纹眉、漂唇等。这不仅节省了自己的化妆时间,还提升了自身的整体颜值,所以一经推出就风靡了广大女性。
所谓的半永久是通过将染料注射与人体皮肤表皮层和真皮层之间,从而达到美容的效果。
如果在正规的美容机构做,起码可以保证安全,怕就怕在人们一方面贪图便宜,一方面不法商家浑水摸鱼,获取最大利益。
不正规的半永久美容店,甚至在没有合格证的情况下,就在顾客身上动手尝试。
这类半永久的美容店,不仅美容技术有待考证,如果器具消毒不到位的话,就容易通过血液传染各种疾病,比如梅毒就是其中的一种。
2.纹身
纹身和半永久的操作方式类似,都是通过针刺皮肤将金属氧化色素注入真皮层内,从而达到在皮肤留下图案的效果。在纹身操作的过程中,针尖会和纹身者的血液不断接触。
同时又在装有纹身药水的容器里反复蘸取,如果工具消毒不彻底、不更换,就可能会导致交叉感染,从而让病毒随着血液肆意传播,梅毒也会在这种可能下进入你的身体。
虽然纹身的人并非全部都会被感染,但也绝对不能存在侥幸心理。在我们下定决心做纹身时,一定要选择正规合格的机构,以免出现梅毒感染的问题。
3.美牙术
牙齿美容是现在很流行的一种方式,通过洗牙、贴片等一系列操作,让你的牙齿变得洁白有光泽。
但是有大约 80%-90%左右的人,在洗牙或补牙的过程中,都会有牙龈出血的情况,如果存在机头消毒不全面,就有可能通过残留血液传播疾病,导致自己感染梅毒。
“爱美之心,人皆有之”,女孩子对美的追求更现实,但是不能一味追求美而忽视安全问题。
所以预防传染病,除了要远离不洁净的性生活外,各位小仙女也要注意选择正规的美容场所,在美容之前一定要查看医生的资格证和医院合格证,以免出现意外。

情志内伤
情志内伤主要指七情过激。在一般情况下,喜、怒、忧、思、悲、恐、傢七种情志活动是人体对客观外界事物的不同反映,属生理现象,不足为病。但当突然、强烈或持久的情志刺激,超过了生理活动所能调节的范围,则可引起人体内阴阳、脏腑、气血、经络的功能失调而致病。正如《素问•阴阳应象大论》所说:“人有五脏化五气,以生喜怒悲忧恐。”可见情志活动必须以五脏精气作为物质基础,而外在的各种刺激只有作用于有关的内脏,才能表现出情志变化。对男科疾病而言,情志因素大都导致功能病变,少数可致器质性病变。
(一)突受惊恐
平时遭受惊恐,或性交时意外受吓,或初婚时性交痛而畏惧,久久不能自解,以致出现阳痿、遗精、射精不能等。如《灵枢•本神》说:“恐惧而不解则伤精,精伤则骨酸萎厥,精时自下。”《临证指南医案》谓:阳痿“亦有因恐惧而得者。盖恐则伤肾,恐则气下也。”
(二)所愿不遂
失恋失意,思虑过度;或情志抑郁或夫妻不睦,精神紧张;或性欲不一致,同房不协调,忍精不泄,可见性欲淡漠、阳痿、早泄、悬痈、疳疮等。如清•俞震说:“少年新婚,欲交媾,女子阻之,乃逆其意,遂阴痿不举。”(《古今医案按•卷八•阳痿》)吴谦说:“疳疮多由欲火未遂瘦淋难。”(《医宗金鉴外科•卷九•下部•疳疮》)清•许克昌说:“悬痈多有忍精提气而成。
所谓欲泄不泄,化为脓血是也。”(《外科证治全书 卷三•悬痈》)
(三)悲哀太甚
遇有严重痛心之事,悲哀欲绝,可出现性功能障碍和其他病变。如《素问•痉论》曰:
“悲哀太甚,则胞络绝,胞络绝则阳气内动,发则心下崩,数瘦血也。”
(四)恼怒太过
口角斗殴,怒发冲冠;或郁怒于中,未得发泄,以致阴纵、阴缩、淋证等。如《血证论》说:
“前阴属肝,肝火怒动,茎中不利,甚则劑痛,或兼血淋。”(卷大•淋浊)
情志之误有“因郁致病”和“因病致郁”两种情况。以不育症为例,可因各种情志因素导致不育(因郁致病);反之,长期不育,又可出现各种情志变化(因病致郁)。因此,正确认识和处理此类致病因素,尤宜引起医者和病者的重视。

性生活是人类正常生活的一部分,但若不加节制,则易引起房劳伤。房劳伤,又易导致其他一系列病变,其病根在于耗精伤气。因此,房劳过度,在中医男科的病因学中有着特殊的意义。
(一)房劳过度导致早衰、损寿
已婚者房事不节,纵欲无度,每夜必欲或一夜数欲;或年过四十,依然纵情恣欲,嗜而无厌,精耗气伤,而致早衰。《素问•上古天真论》说:“以酒为浆,以妄为常,醉以人房,以欲竭其精,以耗散其真,不知持满,不时御神,务快其心,逆于生乐,起居无节,故半百而衰也。”又青年人受黄色荒诞小说、书刊、电影、电视等精神污染,沉溺于色情之中,频频手淫和遗精,也可导致房劳伤。古云:”荒淫无伦,精神耗散,意淫于外,欲火内扇,虽不交合,但精已暗泄,自促其寿命。”上述“半百而哀”、“自促其寿命”,即指房劳伤的后果是早衰和损寿。
(二)房劳过度引起虚劳、消渴、痨瘵
虚劳原因甚多,房劳伤是其主要者。《金匮要略》虚劳门“五劳虚极”,房劳伤即是其中之一。葛可久《十药神书》云:“盖因人之壮年,气血充聚,精液完足之际,不能守养,唯务酒色,岂分饥饱,日夜耽嗜,无有休息,以致耗散精液,则呕血吐痰,骨蒸烦热,肾虚,精竭形羸,颊红面白,口干咽燥,小便白浊,遗精盗汗,饮食艰难,气力全无。”房劳又易伤肾之精,导致阴虚火旺,诱发消渴,故元•朱震享指出:“真水不竭,安有所谓渴哉?”(《丹溪心法•卷三•消渴四十六》)痨瘵每由纵欲而虚损,“瘵虫乘机袭人”之所致。故明•徐春甫有“凡人平素保养元气,爱惜精血,瘵不可得而传。唯夫纵欲多淫,若不自觉,精血内耗,邪气外乘。”(《古今医统大全•卷四十六•痨瘵》)即可患“痨瘵”之说。
(三)其他
此外,尚有大病后过早交合,招致旧病复发的“房劳复”如《金匮要略》所言之伤寒后房劳复,《血证论》所言的失血之人,不忌房劳,而致的血证后房劳复者即是。又产后房劳而致的产后房劳复者亦有之。

纵隔是位于双侧胸腔之间,胸骨之后,脊柱侧面,上为颈部入口,下达膈肌的一个区域。这个区域内包含了心脏、大血管、气管、食管、胸腺等重要结构。当这个区域出现肿物时,会让患者和家属面临一个关键问题:需要做手术吗?
一、纵隔肿物的类型
纵隔肿物种类繁多,可以简单分为良性肿物和恶性肿物。良性肿物常见的有胸腺瘤、神经源性肿瘤、支气管囊肿、食管囊肿等。胸腺瘤多位于前纵隔,部分患者可能没有任何症状,只是在体检时偶然发现。神经源性肿瘤常起源于后纵隔的神经组织,可压迫周围结构。囊肿类肿物则是由于先天发育异常形成,里面可能含有液体等成分。
恶性纵隔肿物包括恶性胸腺瘤、淋巴瘤、纵隔型肺癌等。淋巴瘤可以侵犯纵隔内的淋巴结,导致肿物形成,患者可能伴有发热、盗汗、体重减轻等全身症状。纵隔型肺癌则可能与原发肺部肿瘤侵犯纵隔有关,病情往往较为复杂。
二、是否手术的考虑因素
(一)肿物的性质
如果是良性肿物,且没有引起明显的症状,比如体积较小的囊肿,可能并不需要立即手术。医生通常会选择定期观察,通过影像学检查(如胸部 CT)来监测肿物的大小、形态变化。但如果良性肿物有增大趋势,压迫周围重要器官,如压迫气管导致呼吸困难、压迫食管影响吞咽,或者引起胸痛等不适,就需要考虑手术切除。
对于恶性肿物,手术往往是重要的治疗手段之一。不过,在手术前需要综合评估。如果是早期恶性纵隔肿瘤,没有远处转移,患者身体状况能够耐受手术,手术切除肿瘤可以提高患者的生存率和生活质量。但如果是晚期恶性肿瘤,已经广泛转移,手术可能无法完全切除肿瘤,此时可能需要先进行化疗、放疗等综合治疗,待肿瘤缩小、病情稳定后再评估手术的可能性。
(二)患者的身体状况
患者的年龄、心肺功能、是否有其他基础疾病等对是否手术有重要影响。老年患者或者心肺功能较差的患者,手术风险相对较高。比如,一位患有严重慢性阻塞性肺疾病的患者,如果要进行纵隔肿物切除手术,术后可能会出现呼吸衰竭等严重并发症。在这种情况下,医生需要谨慎权衡手术的利弊。如果患者有冠心病、心力衰竭等心脏疾病,手术中麻醉和操作对心脏的影响也需要充分考虑。
三、手术的风险与收益
(一)手术的风险
纵隔肿物手术是一种较为复杂的外科手术。手术过程中可能会损伤周围的血管、神经、气管、食管等重要结构。如果损伤大血管,可能会导致大量出血,甚至危及生命。损伤神经可能引起相应部位的感觉或运动功能障碍,比如损伤喉返神经可能导致声音嘶哑。另外,术后还可能出现感染、切口愈合不良等问题。对于一些切除范围较大的手术,患者术后呼吸功能和循环功能的恢复也需要密切关注。
(二)手术的收益
对于有手术指征的患者,成功的手术可以切除肿物,缓解肿物对周围组织器官的压迫。如果是恶性肿瘤,手术结合放化疗等综合治疗,可以提高治愈率和患者的生存时间。例如,早期胸腺瘤患者经过手术切除后,多数患者可以获得较好的预后,生活质量得到明显改善。即使是部分良性肿物,手术切除后也可以消除患者的心理负担,避免肿物恶变或进一步发展带来的潜在风险。
四、其他治疗选择
除了手术,对于纵隔肿物还有其他治疗方法。对于淋巴瘤等对放化疗敏感的恶性肿瘤,放化疗可以作为主要的治疗手段。在放化疗过程中,可以使肿瘤缩小、控制肿瘤的进展。对于一些无法耐受手术或者手术切除困难的患者,也可以采用介入治疗的方法,比如对于一些富血供的纵隔肿物,可以通过血管栓塞来减少肿物的血供,缓解症状。
总之,纵隔肿物是否需要做手术需要综合考虑肿物的性质、患者的身体状况等多方面因素。患者和家属应该与医生充分沟通,了解手术的风险和收益以及其他可能的治疗选择,从而做出最适合患者的决策。在面对纵隔肿物时,不要盲目地选择手术,也不要因害怕手术风险而拒绝必要的治疗,科学合理的治疗方案才是改善病情的关键。
在胸部影像学检查日益普及的今天,肺结节的检出率越来越高,这让许多患者陷入了恐慌。然而,并非所有的肺结节都需要手术,了解什么样的肺结节需要手术对于患者和家属来说至关重要。
肺结节的分类与特点
肺结节是指肺内直径小于或等于 3cm 的类圆形或不规则形病灶,影像学表现为密度增高的阴影,可单发或多发。根据密度不同,肺结节可分为实性结节、部分实性结节和磨玻璃结节。
实性结节是指结节内部全部是软组织密度的结节,其恶性概率相对较低,但一旦确诊为恶性,往往生长速度较快,侵袭性可能较强。磨玻璃结节就像在肺组织上蒙上了一层“磨砂玻璃”,密度较低,边界可能不太清晰。磨玻璃结节又分为纯磨玻璃结节和部分实性磨玻璃结节,纯磨玻璃结节有一部分是炎性或良性病变,但也有一定比例可能是恶性,特别是持续存在的纯磨玻璃结节。部分实性磨玻璃结节的恶性可能性相对更高,其中实性成分所占比例越大,恶性程度可能越高。
考虑手术的大小因素
一般来说,结节越大,恶性的可能性越大,需要手术干预的可能性也越高。对于直径大于 8mm 的肺结节,如果通过影像学判断有恶性的可能,往往需要更积极的处理。尤其是部分实性结节,即使直径在 6 - 8mm,若有明显的恶性影像学特征,也可能需要手术。而对于小于 5mm 的微小结节,多为良性,通常不需要立即手术,可以采取定期随访观察的策略。
影像学特征与手术决策
形态
如果肺结节的边缘不规则,有分叶、毛刺、胸膜牵拉征、血管集束征等,这些往往提示恶性的可能。例如,分叶征就像是结节表面有多个凸起,类似树叶的边缘,这是因为肿瘤各部分生长速度不均匀导致的。毛刺征表现为结节边缘有像刺一样的突起,是肿瘤细胞向周围组织浸润的一种表现。当出现这些特征时,需要高度警惕,进一步评估手术的必要性。
密度变化
磨玻璃结节中出现实性成分增加,或者原本的实性结节密度不均匀,出现坏死、空洞等情况,都可能提示结节的性质发生了变化,需要考虑手术切除并进行病理检查。
生长速度
如果在随访过程中,肺结节生长迅速,例如在短时间内(如 3 - 6 个月)体积增大一倍以上,或者原本稳定的结节出现新的实性成分等变化,这往往提示结节有较高的恶性倾向,需要手术治疗。但也有一些炎性结节在短期内也可能有体积变化,需要综合其他因素判断。
患者的相关危险因素
吸烟史
长期吸烟是肺癌的重要危险因素。有重度吸烟史(每天吸烟超过 20 支,吸烟年限超过 20 年)的患者,发现肺结节时,其结节为恶性的可能性相对较高。对于这类患者的肺结节,即使影像学特征不太典型,如果结节大小接近手术指征,也需要更密切的观察或更积极的手术决策。
家族史
有肺癌家族史的患者,其肺结节恶变的风险也会增加。如果家族中有直系亲属患有肺癌,尤其是多位亲属患病,发现肺结节时要更加谨慎。若结节存在可疑特征,即使较小,也可能需要考虑手术切除或更频繁的随访。
职业暴露史
长期接触石棉、氡、砷、铬、镍等致癌物质的人群,肺结节恶变的风险高于普通人群。对于这部分人群中的肺结节患者,手术决策也要适当放宽。
多学科综合评估的重要性
当发现肺结节后,不能仅凭单一因素就决定是否手术。需要呼吸内科、胸外科、放射科等多学科团队共同讨论。放射科医生通过对影像学资料的详细解读,提供结节的大小、形态、密度等信息。呼吸内科医生评估患者的基础肺功能和全身状况,判断患者是否能够耐受手术。胸外科医生则根据结节的特征和患者的整体情况,权衡手术的风险和收益。通过多学科会诊,可以为患者制定出最合理的治疗方案,避免不必要的手术或延误病情。
总之,肺结节是否需要手术需要综合考虑结节的大小、影像学特征、患者的危险因素以及多学科团队的评估结果。患者在得知自己有肺结节后,不要过度惊慌,应积极配合医生进行进一步的检查和诊断,以确定最佳的治疗策略。
展开更多















