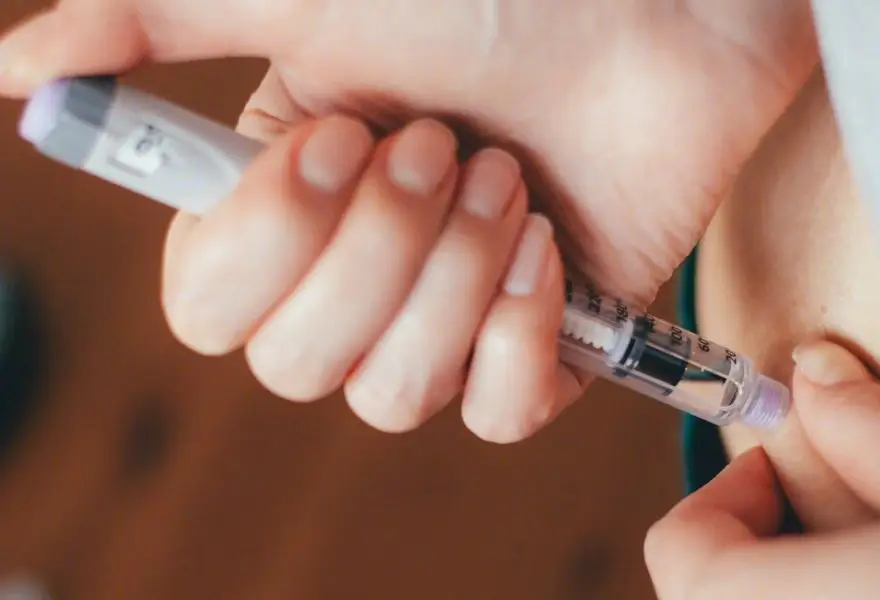
2024年9月5日,礼来公司官宣QWINT-1和QWINT-3两项关于糖尿病的Ⅲ期试验取得积极进展[1]。
这两项临床试验分别在两类患者中评估胰岛素周制剂efsitora的效果,这两类患者分别是首次使用基础胰岛素(未使用过胰岛素)的 2 型糖尿病患者、从每日注射基础胰岛素换成新药的患者。
从提高患者依从性而言,这项研究有重要意义,既往糖尿病患者每次用餐前都需要提取注射胰岛素,若出去吃饭可能会带来一些不便之处,如果能改为周注射还能控制好血糖,或许是糖尿病患者的福音。一起来看这两项研究积极的进展。
QWINT-1中52周糖化血红蛋白降低1.31%
QWINT-1研究是一项随机对照Ⅲ期试验,研究目的是评估与甘精胰岛素相比,每周使用固定剂量递增的胰岛素 efsitora (LY3209590)在首次使用基础胰岛素治疗的 2 型糖尿病(T2D)成人患者中的疗效和安全性[2]。
研究共纳入796名参与者,研究的主要评估结果是糖化血红蛋白(HbA1c)相对于基线的变化。根据礼来公布的结果,在第 52 周时,efsitora 组HbA1c 降低了 1.31%,HbA1c水平为6.92%;甘精胰岛素组降低了 1.27%,HbA1c水平为6.96%。这个试验主要对比efsitora和甘精胰岛素甘精的非劣效性,即控制血糖效果类似[1]。
QWINT-3中26周糖化血红蛋白降低0.86%
研究共纳入986名参与者,QWINT-3研究是一项多中心随机平行Ⅲ期临床试验,旨在评估 LY3209590 与德谷胰岛素在目前接受基础胰岛素治疗的 2 型糖尿病患者中的疗效和安全性,该研究最多持续86 周[3]。
主要研究结果QWINT-1一样,在第26周时,efsitora 组 HbA1c 降低了 0.86%,而德谷胰岛素组HbA1c 降低了 0.75%,26周时HbA1c水平分别为为 6.93% 和 7.03%。也验证了efsitora 与德谷胰岛素相比的非劣效性[1]。
就二个试验安全性而言,在QWINT - 1中,从试验开始到第52周,低血糖(血糖<54mg/dL)的综合发生率为:efsitora组为0.50,甘精胰岛素组为0.88,efsitora组比甘精胰岛素组低约40%。
在QWINT-3中,从试验开始到第78周,低血糖(血糖<54mg/dL)的综合发生率:efsitora组为0.84,胰岛素德谷组为0.74。
关于LY3209590
胰岛素 Efsitora Alfa(efsitora)基础胰岛素周制剂,是一种融合蛋白,将一种新型的单链胰岛素变体与人 IgG2 Fc 结构域结合在一起。其专门设计用于每周一次的皮下注射,,有可能在整个星期内提供更稳定的血糖水平(更少的血糖变异性)。目前该制剂正处于针对 1 型和 2 型糖尿病成人的 Ⅲ 期开发阶段[1]。
2型糖尿病
糖尿病是一组由多病因引起以高血糖为特征的代谢性疾病,是由于胰岛素分泌和/或利用缺陷引起。长期碳水化合物以及脂肪、蛋白质代谢紊乱可引起多系统损伤,导致眼、肾、神经、心脏、血管等组织器官发生进行性病变、功能减退及衰竭[4]。
我国≥65 岁的老年糖尿病患者数量约为3550万[5],居世界首位,且呈现上升趋势。老年糖尿病患者常伴有多种慢性疾病,多重用药较为普遍,可能影响降糖疗效及增加低血糖风险,患者依从性受多种因素影响。
关于礼来
礼来制药是一家致力于通过科学创新改善人类健康水平,惠及全球患者的医药公司。作为医疗健康行业的领军者,礼来制药拥有近150年的历史。今天,我们的药物已帮助全球超5100万人。
运用生物技术、化学和基因医学的力量,其科学家正在积极推动新的医学进展,以应对严峻的全球健康挑战。重新定义糖尿病与肥胖疗法,减少肥胖对人体的长期影响;助力阿尔茨海默病的防治行动;为一系列威胁人类健康的免疫性疾病提供解决方案;以及将难以治愈的癌症转变为可控的疾病。礼来制药迈向健康世界的每一步,都源自于其“致力于让数百万患者生活得更美好”的信念。这包括致力于解决全球多重挑战的创新临床试验,同时确保药物的可及性和可负担性。
参考文献
1.In a first-of-its-kind fixed dose study, once weekly insulin efsitora alfa leads to A1C reduction similar to daily insulin.
2.A Study of Insulin Efsitora Alfa (LY3209590) Compared to Glargine in Adult Participants With Type 2 Diabetes Who Are Starting Basal Insulin for the First Time (QWINT-1) (QWINT-1).
3.A Study of Insulin Efsitora Alfa (LY3209590) Compared With Insulin Degludec in Participants With Type 2 Diabetes Currently Treated With Basal Insulin.
4.中华医学会糖尿病学分会, 国家基层糖尿病防治管理办公室. 国家基层糖尿病防治管理手册(2022)[J]. 中华内科杂志, 2022, 61(7): 717-748.
5.国家老年医学中心, 中华医学会老年医学分会, 中国老年保健协会糖尿病专业委员会. 中国老年糖尿病诊疗指南(2024 版)[J]. 中华糖尿病杂志, 2024,16(2):147-189.
 京东健康互联网医院
京东健康互联网医院
 网站导航
网站导航
 4099
4099
 53
53

 141
141
 0
0
 0
0

 0
0
 0
0

 0
0

 0
0
 0
0