当地时间2024年10月10日,FDA批准组合疗法用于乳腺癌治疗[1]。组合疗法包括inavolisib、palbociclib和氟维司群,组合疗法所治疗的乳腺癌并不一般,是内分泌耐药、PIK3CA突变、激素受体(HR)阳性、人表皮生长因子受体2(HER2)阴性、局部晚期或转移性乳腺癌,且这类乳腺癌在辅助内分泌治疗期间或完成辅助内分泌治疗后复发。

最常见的乳腺癌与耐药
激素受体阳性、HER2-乳腺癌是最常见的乳腺癌亚型[2]。晚期或转移性疾病的初始治疗包括单独使用内分泌治疗 (ET) 或与靶向治疗联合治疗,此后,治疗选择包括单独使用ET或与PI3K/AKT/mTOR通路抑制剂联合使用。但约40%的激素受体(HR)阳性、HER2阴性晚期乳腺癌患者携带PIK3CA基因突变[3]。PIK3CA突变的存在导致磷酸肌醇 3-激酶 (PI3K) 信号通路过度激活、治疗耐药和更差的预后。适应性和获得性耐药的出现,可用疗法的临床获益仍然有限。
为了解决耐药问题,罗氏设计了一项随机双盲对照III期试验,以评估包括inavolisib在内的组合疗法在HR+/HER2-局部晚期或转移性乳腺癌中的疗效。患者按1:1的比例随机分配至inavolisib 9mg或安慰剂口服,每日一次;palbociclib 125mg口服,每日一次,连续21天,然后停药7天;氟维司群 500 mg 在第1周期的第1天和第15天肌肉注射,然后在每 28 天周期的第1天肌肉注射。
无进展生存期达15个月,缓解持续时间有18.4个月
疗效主要结局用无进展生存期 (PFS)评估,也包括括总生存期(OS) 、客观缓解率(ORR)和缓解持续时间(DOR)。
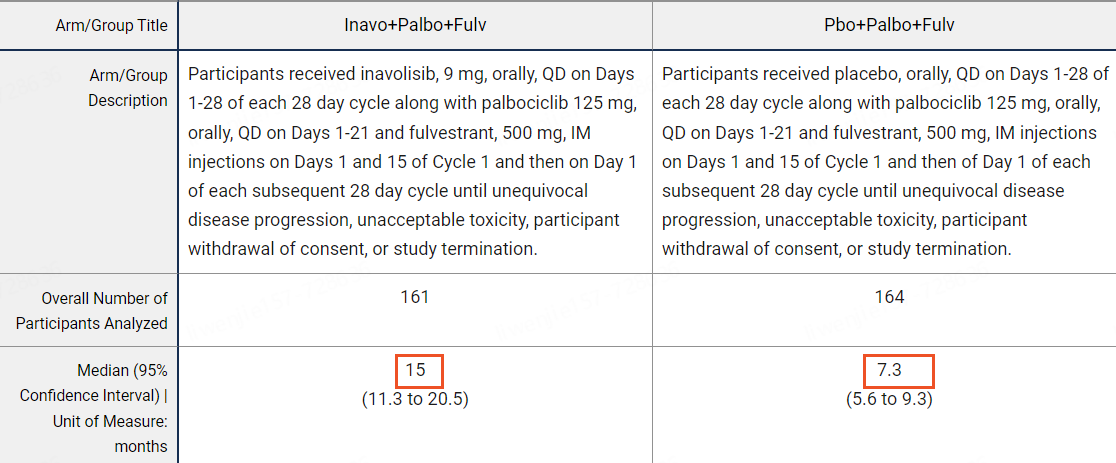
研究结果表明,inavolisib组的中位PFS为15.0个月 (95% CI: 11.3, 20.5),对照组为 7.3 个月 (95% CI: 5.6, 9.3) (风险比 0.43 [95% CI: 0.32, 0.59] p 值 <0.0001)。inavolisib组的 ORR为58% (95% CI: 50, 66),对照组的ORR为25% (95% CI: 19, 32)。中位 DOR 分别为 18.4 个月 (95% CI: 10.4, 22.2) 和 9.6 个月 (95% CI: 7.4, 16.6)[1,4]。
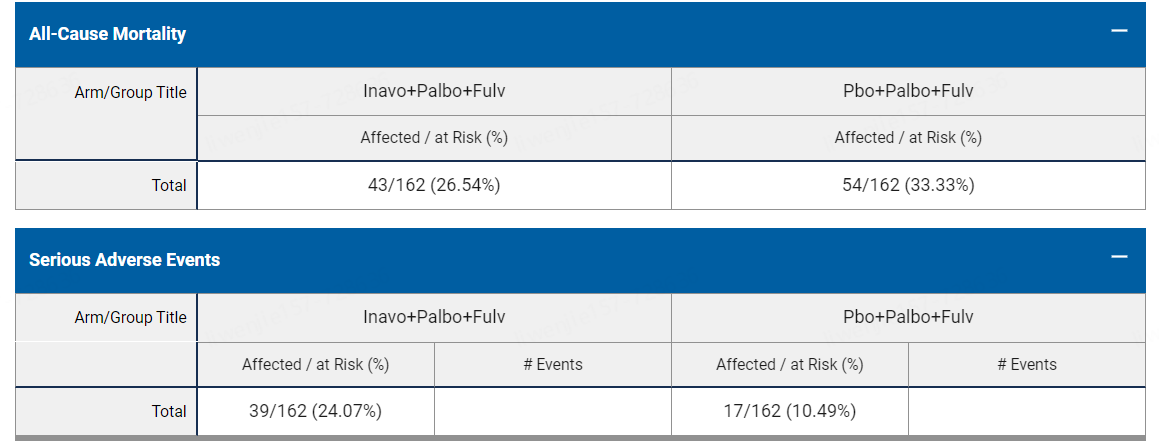
在安全性方面,最常见的不良反应 (≥20%),包括实验室异常,是中性粒细胞减少、血红蛋白降低、空腹血糖升高、血小板减少、淋巴细胞减少、口腔炎、腹泻、钙减少、疲劳、钾减少、肌酐增加、ALT增加、恶心、钠减少、镁减少、皮疹、食欲下降和头痛等。组合疗法组和对照的全因死亡率分别为26.54 vs 33.33%,而严重不良反应发生率分别为24.07% vs 10.49%[4]。
应用新药还需注意什么?
注意到这项试验中的一些不良反应,应用新药时还需注意高血糖、腹泻等风险。
1.高血糖风险
高血糖在inavolisib应用中较为常见,但也可能很严重。因此在用药前和治疗期间监测需要注意血糖水平。如果患者刚好还有糖尿病病史,则更需要注意监测血糖。另外在治疗期间,应保持充足的水分。如果出现下列症状,可能为高血糖,需及时就医。
症状包括呼吸困难、持续2h恶心和呕吐、食欲异常增加、胃痛、过度口渴、口干、脸红、困倦或疲倦、和皮肤干燥,以及排尿比平时更频繁或尿量比正常多[5]。
2.腹泻
用inavolisib期间可能出现腹泻,严重腹泻会导致体内水分流失过多(脱水)和肾损伤。如果您在治疗期间出现腹泻、胃部区域(腹痛)或看到粪便中有粘液或血液,需及时就医。此外用药期间注意多喝水。
3.联合用药
这次获批为组合疗法,最常见的不良反应和异常血液检查结果包括:白细胞计数、红细胞计数和血小板计数降低,血液中的钙、钾、钠和镁水平降低,血液中肌酐水平升高,血液中肝酶丙氨酸转氨酶 (ALT) 水平升高,恶心和食欲不振、头痛。
参考文献:
1.FDA approves inavolisib with palbociclib and fulvestrant for endocrine-resistant, PIK3CA-mutated, HR-positive, HER2-negative, advanced breast cancer.
2.Jhaveri KL, Accordino MK, Bedard PL, Cervantes A, Gambardella V, Hamilton E, Italiano A, Kalinsky K, Krop IE, Oliveira M, Schmid P, Saura C, Turner NC, Varga A, Cheeti S, Hilz S, Hutchinson KE, Jin Y, Royer-Joo S, Peters U, Shankar N, Schutzman JL, Juric D. Phase I/Ib Trial of Inavolisib Plus Palbociclib and Endocrine Therapy forPIK3CA-Mutated, Hormone Receptor-Positive, Human Epidermal Growth Factor Receptor 2-Negative Advanced or Metastatic Breast Cancer. J Clin Oncol. 2024 Sep 5:JCO2400110. doi: 10.1200/JCO.24.00110. Epub ahead of print. PMID: 39236276.
3.Potential for Long-Term Disease Control with Alpelisib Plus Fulvestrant Spans Patient Subgroups in HR+PIK3CA-Mutated Advanced Breast Cancer,The Oncologist, Volume 26, Issue S3, July 2021, Pages S11–S12,https://doi.org/10.1002/onco.13873
4.A Study Evaluating the Efficacy and Safety of Inavolisib + Palbociclib + Fulvestrant vs Placebo + Palbociclib + Fulvestrant in Patients With PIK3CA-Mutant, Hormone Receptor-Positive, Her2-Negative, Locally Advanced or Metastatic Breast Cancer (INAVO120)
5.FDA Approves Genentech’s Itovebi, a Targeted Treatment for Advanced Hormone Receptor-Positive, HER2-Negative Breast Cancer With aPIK3CAMutation
 京东健康互联网医院
京东健康互联网医院
 网站导航
网站导航
 8
8

 5
5

 5
5
 7
7

 6
6

 3
3

 6
6
 5
5

 0
0
 0
0