简称:
石家庄市裕华区银通北社区卫生服务站成立于2014年10月24日,注册地位于河北省石家庄市裕华区槐中路614号,法定代表人为刘君林。经营范围包括预防保健科、全科医疗科、内科、临床体液、血液专业、心电诊断专业、中医科
-
*元栋回复质量:暂无服务态度:暂无回复速度:暂无functions/format.html此用户未填写评价内容图文问诊
-
*佳莹回复质量:暂无服务态度:暂无回复速度:暂无functions/format.html此用户未填写评价内容图文问诊
-
*春艳回复质量:非常满意服务态度:非常满意回复速度:非常满意functions/format.html谈吐清晰,用药准确图文问诊
展开更多
-
总交流次数
68
总回复次数
40
患者:女 22岁 -
总交流次数
2
总回复次数
1
患者:男 22岁
展开更多
-



参考文献:
[1] 支气管扩张症专家共识撰写协作组, 中华医学会呼吸病学分会感染学组.中国成人支气管扩张症诊断与治疗专家共识 [J].中华结核和呼吸杂志 , 2021, 44(4): 311-321.
[2] 梁艳等. 支气管扩张症的治疗概述及进展[J]. 中西医结合心血管病杂志, 2018, 6(31):173-176
[3] 冯明发,张薇.支气管扩张症合并慢性阻塞性肺疾病的研究进展[J].临床与病理杂志,2021,41(10):2461-2467.
[4] 彭翠兰.成人支气管扩张症病原菌分布及咯血原因分析[J].中外女性健康研究,2019(03):119-120.
[5] 徐小勇,施毅.支气管扩张的诊断和治疗进展[J].中国呼吸与危重监护杂志,2017,16(02):186-190.
[6] 杨妹,霍建民.支气管扩张病因相关疾病的研究进展[J].临床肺科杂志,2022,27(04):607-611.
[7] 刘雪健,王佳贺.支气管扩张症微生物感染的研究进展[J].中国医科大学学报,2022,51(03):263-266.
-
免疫疗法,主要是靶向PD-1或PD-L1的免疫检查点抑制剂,已成为大多数晚期肺癌患者的标准治疗方法,与化疗相比具有生存优势,且副作用更低。在短短的时间内,PD-1和PD-L1抑制剂已经从一种有希望的挽救性疗法,变为晚期非小细胞肺癌(NSCLC)和小细胞肺癌(SCLC)的标准一线治疗策略,是局部晚期不可切除NSCLC的重要治疗手段,也是早期NSCLC的一种潜在治疗策略。下文总结了免疫疗法在转移性非小细胞肺癌一线治疗中的应用。
PD-1/PD-L1单药用于转移性NSCLC一线治疗
KEYNOTE-024试验是首个建立了免疫治疗可用于NSCLC一线治疗的研究。这项全球性III期试验纳入了305例PD-L1高表达的IV期NSCLC患者,患者被1:1随机分配至派姆单抗或铂类化疗。中位随访时间为11.2个月,派姆单抗组的中位无进展生存期(PFS)为10.3个月,明显高于化疗组的6.0个月。KEYNOTE-024证明了 在PD-L1高表达的转移性NSCLC患者中,一线治疗使用派姆单抗比化疗更有生存优势,FDA于2016年批准了该适应症。
IMpower 110试验探讨了阿特珠单抗在PD-L1阳性NSCLC患者一线治疗中的作用。这项III期试验纳入了572名患者,被1:1随机分配到阿特珠单抗组或化疗组。中位随访15.7个月,在PD-L1高表达人群中,阿特珠单抗组的表现优于化疗,阿特珠单抗组的中位总生存期(OS)为20.2个月,化疗组为13.1个月。 2020年5月,FDA批准阿特珠单抗用于PD-L1高表达晚期NSCLC患者的一线治疗。
双免疫检查点抑制剂用于转移性NSCLC的一线治疗
除了PD-1/PD-L1抑制剂外,另一种成功的免疫检查点抑制剂是CTLA-4抑制剂,如伊匹单抗是黑色素瘤和肾细胞癌的标准治疗组成。基于CheckMate 227试验显示出的疗效,也已成为NSCLC的标准一线治疗选择。
CheckMate 227试验纳入了既往未治疗过的NSCLC患者。1189名表达PD-L1的患者被随机分配至联合免疫治疗(纳武单抗 3mg/kg,伊匹单抗1mg/kg),纳武单抗单药治疗(240 mg),或铂类化疗。550名无PD-L1表达的患者,随机接受纳武单抗+伊匹单抗治疗,纳武单抗(360mg)联合化疗,或铂类化疗。
在PD-L1阳性组中,联合免疫治疗组优于化疗组,中位OS分别为17.1个月和14.9个月。 2020年5月15日,纳武单抗+伊匹单抗联合治疗被FDA批准用于PD-L1阳性晚期NSCLC的一线治疗。
化疗+免疫治疗用于晚期非鳞状NSCLC的一线治疗
另一种在肺癌治疗中获得成功的免疫治疗策略是将 PD(L)1抑制剂与化疗联合使用,这种策略对PD-L1阴性肿瘤也有效。目前已有许多组合被发现有效,化疗+免疫疗法策略已被证明有效且耐受性良好。
第一个被批准的肺癌化疗-免疫治疗方案是基于KEYNOTE-021G试验,该研究探讨了铂类化疗加上派姆单抗的疗效。在这项随机II期研究中,123例未经治疗的EGFR和ALK野生型、非鳞状NSCLC患者被随机分配到卡铂加培美曲塞组或化疗加派姆单抗组。结果显示,卡铂和培美曲塞的基础上加入派姆单抗可改善患者缓解率(58% vs. 33%)、PFS(24.5 vs. 9.9个月)和OS(34.5 vs. 21.1个月)。 派姆单抗+卡铂和培美曲塞方案于2017年5月10日获得FDA加速审批。
该方案的确证性III期试验为KEYNOTE-189,该研究以2:1的方式将616名既往未经治疗、EGFR和ALK野生型、非鳞状NSCLC患者随机分配至每3周一次的派姆单抗 200 mg组或安慰剂组,并加上4个周期的顺铂或卡铂加培美曲塞。中位随访23.1个月的结果显示,一线治疗中派姆单抗联合化疗改善了患者的生存率,卡铂+培美曲塞+派姆单抗的中位OS为22.0个月,化疗+安慰剂为10.7个月。基于该研究, FDA于2018年8月20日批准派姆单抗+铂类+培美曲塞用于非鳞状NSCLC的一线治疗。
一线化疗加上阿特珠单抗,也能改善患者结局。在IMpower 130试验中,724例既往未治疗的晚期非鳞状NSCLC患者以2:1的比例被随机分配至阿特珠单抗(1200mg)或安慰剂组,同时给予卡铂和白蛋白紫杉醇。中位随访18.5个月,阿特珠单抗组的生存期更好,中位OS为18.6个月,安慰剂组为13.9个月。 阿特珠单抗联合卡铂+白蛋白紫杉醇于2019年12月3日获得FDA批准。
另一个引人注目的免疫治疗策略是 化疗-免疫治疗再加上血管生成抑制剂。IMpower 150试验探讨了一线化疗中加入贝伐珠单抗和阿特珠单抗的疗效。既往未接受过治疗的非鳞状NSCLC患者接受四个周期的卡铂和紫杉醇治疗,并随机1:1:1接受贝伐珠单抗单药、阿特珠单抗单药或贝伐单抗联合阿特珠单抗。
结果显示,阿特珠单抗、贝伐珠单抗、卡铂和紫杉醇4药方案组的中位PFS为8.3个月,OS为19.2个月,优于贝伐珠单抗+卡铂+紫杉醇组(中位PFS为6.8个月,中位OS为14.7个月)。与其他研究类似,该方案在不同PD-L1表达水平的患者中均有获益。 阿特珠单抗+贝伐珠单抗+卡铂+紫杉醇的方案于2018年12月6日获得FDA批准,作为晚期非鳞状NSCLC的一线治疗策略。
化疗+免疫治疗用于晚期鳞状NSCLC的一线治疗
化疗+免疫治疗也能改善鳞状NSCLC患者的结局。KEYNOTE-407试验将559例未经治疗的鳞状NSCLC患者随机分配至派姆单抗或安慰剂组,并同时给予化疗(卡铂加紫杉醇或白蛋白紫杉醇)。结果显示,化疗基础上加入派姆单抗改善了患者生存期,中位OS为15.9个月,单纯化疗组为11.3个月,在不同PD-L1表达水平的患者中均有获益。 派姆单抗联合卡铂和紫杉醇或白蛋白紫杉醇于2018年10月30日被FDA批准为晚期鳞状NSCLC患者的一线治疗方案。
然而,研究显示, 卡铂和白蛋白紫杉醇基础上加用阿特珠单抗并不能改善鳞状NSCLC患者的总生存。在IMpower 131试验中,未经治疗的晚期鳞状NSCLC患者被1:1:1随机分配至卡铂和白蛋白紫杉醇加阿特珠单抗组,卡铂和紫杉醇加阿特珠单抗组,或卡铂和白蛋白紫杉醇组。结果显示,加上阿特珠单抗后PFS有所改善,但对总生存期没有改善,加用阿特珠单抗的中位OS为14.2个月,单纯化疗组为13.5个月。
参考文献:
J Surg Oncol. 2021 Mar;123(3):718-729.
京东健康互联网医院医学中心
作者:卢秀玲,毕业自北京大学公共卫生学院,曾在某知名医学网站担任医学总编辑,负责过肿瘤、心血管、内分泌等多个频道的内容产出。
-

子宫肌瘤是发生在子宫上的一种良性肿瘤,多发生于30~50岁女性,又被称为“子宫纤维瘤”、“子宫纤维肌瘤”、或“子宫平滑肌瘤”。
有资料显示,在35岁以上妇女中,每4~5人就有1人患有子宫肌瘤,只不过有些人症状不明显,没有被诊断出来而已。

子宫肌瘤的发生原因还不完全清楚,但一般认为与女性体内的雌激素水平升高或者紊乱有关。
另外,子宫肌瘤还有一定的遗传倾向,所以母亲有患子宫肌瘤,女儿患瘤几率也很大。
寻找子宫肌瘤的蛛丝马迹

俗话说:在其位而谋其政,位置很重要。不同位置上的子宫肌瘤,症状也不一样,甚至有的还可以无症状。一般而言,出现以下一种或数种症状的女性,要高度警惕。
阴道出血
是子宫肌瘤最常见的症状,需要提醒的是如果出现这一症状,不要自认为是由于劳累或是闹更年期而不重视。
盆腔包块
当肌瘤过大或体型偏瘦时,可在下腹部摸到较硬的实性包块,尤其是早晨排尿前更容易摸到。有些肥胖的人不一定能摸到瘤子,但会发现腰围增大,千万不要想当然的以为是发福。
压迫症状
肌瘤向前可压迫膀胱,可引起尿频、尿急,甚至排不出尿(称为尿潴留);向后可压迫直肠引起腹泻或便秘;发生在子宫两侧的阔韧带中的肌瘤可压迫输尿管、髂内外静脉和神经,从而发生输尿管梗阻、肾盂积水、下肢浮肿或疼痛。
不孕
有的肌瘤会改变子宫腔形态,或者阻碍受精卵的着床,或者长在子宫角处,压迫了输卵管进入子宫的开口而妨碍精子进入输卵管,都可造成不孕。
腹痛
子宫肌瘤一般很少引起腹痛。但如果肌瘤过大压迫盆腔的神经,或肌瘤因急性缺血而发生红色变性,或带蒂的浆膜下子宫肌瘤发生扭转时,可引起剧烈腹痛。
白带增多
当肌瘤脱出子宫颈口或阴道口时,其表面会溃疡坏死,出现白带增多,如果合并感染,可有脓性白带。肌壁间肌瘤如果体积较大,可使宫腔面积增大,子宫内膜分泌增加而且盆腔充血,也可引起白带增多。
贫血
长期月经过多,可造成继发性贫血,贫血严重者可有贫血性心脏病。
检查发现了子宫肌瘤,还能怀孕吗?

许多在孕前体检发现子宫肌瘤的女性,经常会担心还能不能怀孕,子宫肌瘤的检出可给了她们一个不小的打击。其实,子宫肌瘤与怀孕生子的关系还真是剪不断,理还乱。
如果不考虑怀孕生子的话,只有那些位置特殊、出现月经量多、月经淋漓不尽、贫血等症状,或者直径超过5厘米的肌瘤才需要手术。而对于准备怀孕的女性来说,治疗的指征可能更宽泛一些。
对于位于子宫腔内的粘膜下肌瘤,由于有可能妨碍未来的胚胎着床,从而导致流产。因此无论有无症状,都建议在怀孕前先进行处理。
那么,怀孕前到底多大的子宫肌瘤就必须手术呢?这个没有一个统一的标准,一般来说,如果子宫肌瘤直径不超过4厘米的肌壁间肌瘤或浆膜下肌瘤,可以考虑先怀孕。但是,怀孕期间肌瘤可能迅速长大,有引发流产或早产的风险。
如果肌瘤位于子宫的下端,即子宫颈、或者其他部位的子宫肌瘤直径小于4厘米,但患者有不孕历史或多次自然流产、又找不到其它明确原因时,可以先做子宫肌瘤剔除,然后再怀孕。
女性切除子宫后会变成男的吗?

子宫是女人不可或缺的一部分,但是子宫肌瘤让很多人无奈的选择在子宫上动刀,甚至是切除子宫。有的人会忧心忡忡地问,如果子宫被切除后,会变得声音低沉、长出胡须和喉结,甚至变成男的吗?回答当然是否定的!
男女之所以有差别,主要是因为性腺也就是女性卵巢与男性睾丸的不同作用,与子宫并没有直接的关系。
因子宫肌瘤需要切除子宫的妇女,在切除子宫时通常会保留一侧或双侧卵巢。只要卵巢保留下来,就仍然会分泌雌激素、孕激素和雄激素,所以人们不必过于担心。
子宫肌瘤会癌变吗?

子宫肌瘤会不会癌变?这是一个长期困扰着肌瘤患者的问题。一般来说,子宫肌瘤发生恶性变的几率不超过0.5%,也就是说每200例子宫肌瘤患者中,有一个可能发生恶性变。
0.5%的肌瘤恶变率,似乎看起来不是很高,但是谁又能保证不会发生在自己身上?特别是对于那些短期内突然长大,绝经后不缩小甚至长大的肌瘤,是最需要警惕的。
文章图片来源于网络,作品版权归原作者所有。
京东健康互联网医院医学中心
作者介绍:李颖,北京妇产医院,生殖医学中心,副主任医师,讲师 , 女性不孕症的诊断处理方案和辅助生殖技术的实施;生殖内分泌疾病的诊治;复发性流产的诊断和处理。擅长个体化超促排卵方案的制定;辅助生育技术治疗不孕不育症。
-
丙型肝炎持续是一个严重的公共卫生问题,2015年,全世界丙肝人数估计有7100万。丙肝直接抗病毒药物(DAA)的出现,使得丙型肝炎的治疗取得了显著进展。但需要关注的一个重要问题是,全球感染丙肝病毒的育龄女性和孕妇人数在增加,而妊娠期活动性丙肝与妊娠期胆汁淤积以及母婴传播的风险增加相关。有些指南和国家建议在怀孕期间进行更普遍的丙肝筛查,许多研究者也在对怀孕期间进行丙肝治疗的有效性和安全性开展了调查。
妊娠期丙肝的流行病学
对欧盟2005-2015年数据进行的系统评价估计,孕妇中丙肝的患病率为0.1%-0.9%。在非洲进行的一项荟萃分析估计,从2003-2015年,孕妇中丙肝的患病率为3.4%。最近对美国所有活产婴儿的评估显示,丙肝感染率从1.8/1000名活产儿增加到4.7/1000名活产儿。美国CDC对2000-2015年的数据进行分析发现,全国分娩女性中丙肝感染率增加了400%以上,从0.8/1000增至4.1/1000。在波兰等国家(从1998-2012年)进行的研究也显示,随着时间的推移,怀孕期间丙型肝炎的患病率有所上升。
既往推荐孕期的丙肝筛查是针对高风险人群进行,不过也有越来越多国家考虑孕期采取更普遍的丙肝筛查。更普遍的筛查需要考虑到成本效益,也要考虑到初始筛查后何时重新筛查的问题。目前欧洲肝病研究协会和亚太肝病研究协会都还是推荐对高风险人群的筛查,没有针对更普遍筛查更新推荐意见。
丙肝的母婴传播风险
妊娠期丙肝得到诊断的一个重要意义是了解母婴传播风险。2014年的一项荟萃分析对1997-2012年109项丙肝女性研究进行了分析,估计母婴传播率为5.8%,合并感染HIV女性的母婴传播率明显更高,达到10.8%。此外,在对接受HIV治疗的女性进行的观察研究中,发现母婴传播率降低了,表明抗HIV治疗可能是降低丙肝母婴传播风险的一种潜在有效的干预措施。
最近,一项来自美国的队列研究报告了丙肝母亲中的母婴传播率为3.6%。西班牙最近的一项研究估计,丙肝合并HIV感染母亲的母婴传播率为7%。然而,鉴于婴儿中的丙肝检测率较低,关于丙肝母亲所生婴儿中丙肝真实患病率的数据有限,因此准确估计母婴传播风险存在一定的挑战性。例如,在对8119名丙肝女性进行的一项研究中,只有84名(16%)婴儿接受过丙肝检测。同样,在另一项以人群为基础的回顾性队列研究中,只有30%的高危婴儿接受过丙肝检测。在一项对3000名孕妇的前瞻性研究中,母婴传播风险远远高于回顾性研究中的发现,3000名女性中,丙肝阳性女性有46例,其中8例新生儿出现了母婴传播(17.39%)。高母体病毒载量被确定为母婴传播的主要危险因素。
丙肝对妊娠结局的影响
妊娠期感染丙型病毒与不良的产科结局相关。在一项对超过400万名女性进行的大型荟萃分析中,有5000多人感染了丙肝病毒,结果发现早产和丙肝存在显著相关性。同样,瑞典一个纳入了2000多名丙肝新生儿的注册研究报告,在调整产妇年龄、吸烟、BMI、糖尿病和饮酒等因素后,丙肝与早产和新生儿死亡存在关联。妊娠期肝内胆汁淤积症(ICP)可能是最具确定性的丙肝相关的妇产科结局,妊娠前患有丙型肝炎的女性发生ICP的风险明显更高。考虑到这一风险的显著增加,以及ICP与不良胎儿结局的关联,患有丙型肝炎的女性应该在产前就这一潜在风险进行咨询。但目前尚不清楚妊娠期丙肝治疗或清除是否会降低ICP或其他不良妊娠结局的发生风险。
孕期直接抗病毒治疗(DAA)的注意事项
以前的AASLD/IDSA指南建议避免怀孕期间进行治疗,但目前的建议更新为:在患者和医生讨论潜在的风险和益处后,可以考虑在怀孕期间进行治疗。理想情况下,女性应该在怀孕前接受治疗,但如果在怀孕期间诊断出丙肝,就应讨论何时能够开始治疗丙肝。一项调查结果显示,超过一半的受访者表示会考虑在怀孕期间接受DAA治疗以预防母婴传播。
孕妇的安全是最重要的。真实世界的数据有限,许多动物生殖研究表明DAA在这种情况下的安全性,即没有发现索非布韦疗法或泛基因型丙肝鸡尾酒疗法(G/P)会导致新生儿不良发育结局。因为动物模型中显示DAA是安全的,目前众多研究在探讨怀孕期间或分娩后立即使用DAA的疗效和安全性。最近,匹兹堡开展了首个针对怀孕期间进行HCV治疗的试验。9名妊娠中期和晚期的患者入组,并接受12周疗程的索非布韦/雷迪帕韦治疗,结果显示治疗安全有效且耐受良好。但是,该研究的样本量还是太少了。其他研究还正在开展中。
因此,在还没有足够的安全性数据的情况下,许多医生在考虑孕期使用DAA治疗时犹豫不决,还需要更大规模的研究来确定DAA在怀孕期间的安全性和有效性。众所周知,药物暴露的最高潜在致畸风险发生在妊娠早期,因此非常有必要评估妊娠早期的治疗安全性(以及母乳喂养期间)。现在的指南建议,怀孕期间的治疗需要孕妇和医生基于获益/风险来共同决策。
总结
在过去十年中丙肝的流行病学发生了变化,需要加强对育龄期女性和怀孕期间丙肝感染的关注。尽管一些地区已经建议在怀孕期间普遍进行丙型肝炎的筛查,但尚不清楚这些建议是否会在国际层面上得到更广泛的推广,也不清楚在怀孕期间全面筛查是否会导致丙肝诊断显著增加。未来的研究方向应包括:评估妊娠期进行DAA治疗的成本效益、可行性和有效性,以及开发最佳的诊疗模式以降低母婴传播的风险。
参考文献:
J Hepatol. 2020; S0168-8278(20)33814-9.
京东健康互联网医院医学中心
作者:梁辰,约翰霍普金斯大学公共卫生学院流行病学硕士,主要研究方向为慢性病流行病学。
-




参考文献:
[1]丁盛玲.盆底重建术的术前与术后护理体会[J].中国临床保健杂志,2011,14(04):445.
[2]张志霞,顾雪敏,李怀芳.加速康复外科在盆底重建围手术期中的应用进展[J].同济大学学报(医学版),2021,42(06):846-852.
[3] 张园红.综合护理干预方案对盆底重建术后尿潴留的预防作用[J].河北北方学院学报(自然科学版),2021,37(08):25-26+29.
[4]石俊静,职梅,路萍.围术期护理对行盆底重建术治疗的盆底功能障碍性疾病女性患者的干预效果[J].慢性病学杂志,2021,22(06):877-879.DOI:10.16440/j.cnki.1674-8166.2021.06.016.
[5]张晓丽,陈海燕.中老年女性全盆底重建术围手术期护理体会[J].青海医药杂志,2013,43(12):41-42.
-

-

降血脂是降低心血管发病率和死亡率最有效的措施之一。通过他汀类药物、依折麦布或蛋白转化酶枯草杆菌蛋白酶/kexin9型抑制剂(PCSK9i)降低低密度脂蛋白(LDL-C)的临床获益已被充分证实。
胆固醇治疗研究者协作组(CTT)通过系统综述的方法评估了他汀类药物降低LDL-C的临床获益1。21篇研究的Meta分析表明:使用他汀类药物可以使LDL-C降低1.07mmol/L,每降低1.0mmol/L LDL-C 可使主要心血管事件降低21% (95% CI 19-23; p<0.0001)。CTT进一步评估了强化他汀治疗的临床效果,结果发现:强化他汀治疗可以在常规治疗的基础上降低LDL-C 0.51mmol/L,每降低1.0mmol/L LDL-C可进一步降低主要心血管事件28%(95% CI 22-34; p<0.0001)(见下图)。
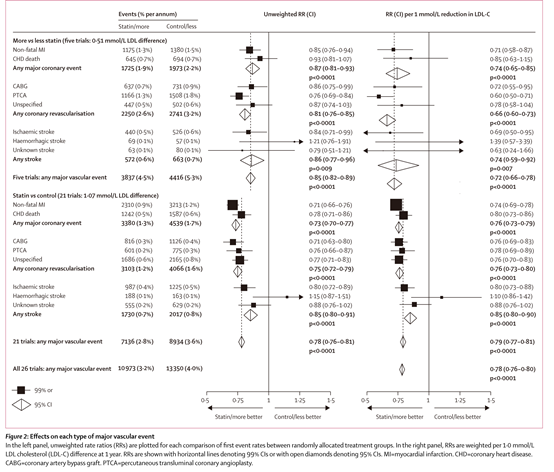
图源:Efficacy and safety of more intensive lowering of LDL cholesterol: a meta-analysis of data from 170 000 participants in 26 randomised trials
依折麦布是一种非他汀类的降脂药物,通过靶向作用于 Niemann-Pick C1-like 1 (NPC1L1) 蛋白减少肠道对胆固醇的吸收。在他汀类药物治疗的基础上加用依折麦布可进一步降低 LDL-C 23%-24%。为了考察依折麦布能否能否降低心血管事件,IMPROVE-IT研究2纳入18,144名急性冠脉综合征患者,将其随机分为联合用药组(阿托伐他汀40mg联合依折麦布10mg)和他汀单药治疗组(阿托伐他汀40mg联合安慰剂)。治疗期间,联合用药组LDL-C控制水平为53.7mg/dL,而他汀单药治疗组为69.6 mg/dL。随访7年后,联合用药组主要终点事件发生率为32.7%,而辛伐他汀单药治疗组为 34.7%(HR 0.936,95% CI 0.89-0.99)(Kaplan–Meier曲线见下图)。两组间肌肉、胆囊和肝脏系统不良反应及癌症的发生率无显著性差异。
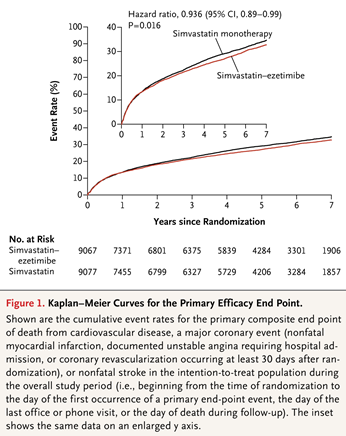
图源:Ezetimibe Added to Statin Therapy after Acute Coronary Syndromes
依洛尤单抗是一种已在我国上市的PCSK9i。在FOURIER研究3中 ,27,564 名接受他汀类药物治疗且LDL-C≥70mg/dL的动脉粥样硬化性心血管疾病(ASCVD)患者被随机分为依洛尤单抗组(每两周 140 mg或每月420 mg)或安慰剂组。主要研究终点是由心血管死亡、心肌梗死、卒中、因不稳定心绞痛或冠脉血运重建住院的复合终点。次要研究终点是心血管死亡、心肌梗死或中风的复合终点。
经过48周的治疗,依洛尤单抗组LDL-C水平从92mg/dL降至30mg/dL(中位数),与安慰剂相比下降59%(P<0.001),同时,依洛尤单抗显着降低了主要研究终点(9.8% vs. 11.3%;HR 0.85;95% CI 0.79-0.92; P<0.001)和次要研究终点(5.9% vs.7.4%; HR 0.80;95% CI,0.73 - 0.88;P<0.001)发生率(见下图)。
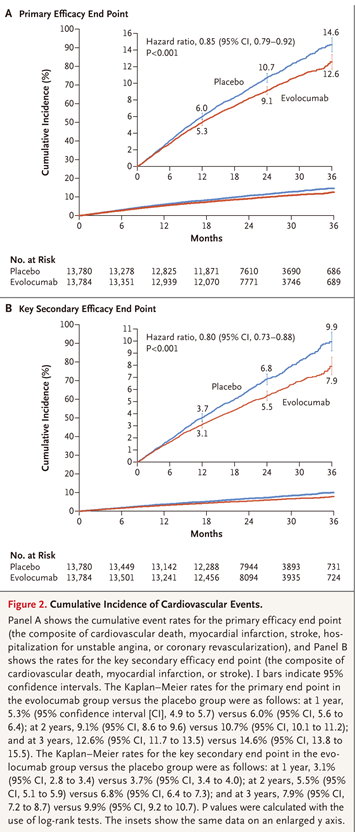
图源:FOURIER Steering Committee and Investigators. Evolocumab and clinical outcomes in patients with cardiovascular disease.
为了了解美国ASCVD患者LDL-C控制情况,Cannon CP等人开展了前瞻性的观察性研究GOULD4。该研究共纳入2016.12-2018.07期间符合纳排标准的ASCVD患者5006名,依据患者情况,将其分为三组:(1)PCSK9i组(接受了PCSK9i治疗);(2)LDL-C≥100mg/dL且未接受PCSK9i组;以及(3)LDL-C水平70-99mg/dL且未接受PCSK9i组。经过2年的治疗,仅有17.1%的患者接受了强化降脂治疗。在LDL-C≥100mg/dL及70-99mg/dL患者中,分别有22.4%和14.4%的患者接受了强化降脂治疗,6.4%和6.3% 的患者增加了他汀的使用剂量;6.8%和4.5%的患者加用了依折麦布;6.3%和2.2%的患者加用了PCSK9i。91.7%的PCSK9i的患者在两年后仍然接受PCSK9i治疗。在接受了血脂检测的患者中,LDL-C≥100mg/dL,70-99mg/dL以及PCSK9i组分别有21.0%、33.9%、52.4%的患者达到了LDL-C<70mg/dL的治疗目标。
虽然2018美国心脏病学会指南以及2020年欧洲心脏病学会/欧洲动脉粥样硬化学会最新指南均强调了ASCVD患者血脂达标的意义,但大部分血脂>70mg/dL的患者并未得到强化降脂治疗,三分之二的患者血脂仍然高于控制目标。相信这种情况在我国也同样存在,血脂达标仍将是未来我国公共卫生工作的重要内容。
参考文献:
1. Baigent C, Blackwell L, Emberson J, et al. Cholesterol Treatment Trialists’ (CTT) Collaboration. Efficacy and safety of more intensive lowering of LDL cholesterol: ameta-analysis of data from 170,000 participants in 26 randomised trials. Lancet 2010;376(9753):1670-1681.
2. Cannon CP, BlazingMA, Giugliano RP, et al. IMPROVE-IT Investigators. Ezetimibe added to statin therapy after acute coronary syndromes. N Engl J Med 2015;372(25):2387-2397.
3. Sabatine MS, Giugliano RP, Keech AC, et al. FOURIER Steering Committee and Investigators. Evolocumab and clinical outcomes in patients with cardiovascular disease. N Engl J Med 2017;376(18): 1713-1722.
4. Cannon CP, Lemos JA, Rosenson RS, et al. Use of Lipid-Lowering Therapies Over 2 Years in GOULD, a Registry of Patients With Atherosclerotic Cardiovascular Disease in the US. JAMA Cardiol 2020. doi: 10.1001/jamacardio.2021.1810. Online ahead of print.
京东健康互联网医院医学中心
作者简介:李丹丹,首都医科大学附属北京友谊医院,研究方向为循证药学。为患者提供专业的用药指导,同时为临床医护人员提供最佳用药参考。
-

妊娠期间急性肾损伤(AKI)是孕产妇以及胎儿发病和死亡的一个重要原因。AKI与慢性肾病(CKD)和终末期肾病(ESKD)、不良心血管事件的风险增加、住院时间更长相关。早期识别和治疗妊娠期AKI至关重要,是挽救生命的潜在措施。
由于产前诊疗的改善,发达国家妊娠相关AKI的发病率较低,但最近十年来,研究发现,美国的发病率几乎增加了3倍,可能是因为以下原因所致:孕妇年龄较大,合并症较多,AKI检出率较高,妊娠期高血压的发病率增加,肥胖率增加。相比之下,发展中国家近年来妊娠相关AKI总体上有所下降,但发病率仍然高于发达国家。在印度,住院女性中妊娠相关AKI从20世纪80年代的15%下降到21世纪初的1.5%。一项来自中国的研究显示,妊娠相关AKI的发病率下降了0.2%-1.8%。
妊娠期AKI的诊断
临床实践中,妊娠期AKI的诊断并未标准化,因为妊娠相关AKI的定义不一致。而且妊娠期肾小球超滤导致血清肌酐的生理性降低,会影响AKI的检测。 目前妊娠期AKI的诊断尚无明确的标准。应注意妊娠期血清肌酐水平的变化趋势,在特定的临床环境下,即使肌酐的微小变化也能敏感地反映早期肾损伤。例如,在新发高血压的女性患者中,伴随着血清肌酐增加0.3 mg/dL、肝酶增加以及血小板减少,就反映了AKI的可能,需要密切随访肾功能。对AKI的初步评估应包括,全面回顾患者的CKD、慢性高血压、糖尿病、先兆子痫、系统性红斑狼疮和肾小球疾病史。
妊娠剧吐和感染性流产是妊娠早期发生AKI的常见原因。大多数发生在妊娠中期和晚期的AKI,与先兆子痫、HELLP综合征(以溶血、肝酶升高和血小板减少为特点)、AFLP(急性妊娠脂肪肝)、TTP(血栓性血小板减少性紫癜)等血栓性微血管病和胎盘早剥等妊娠并发症有关。非典型溶血尿毒综合征 (aHUS)和非甾体抗炎药(NSAID)引起的肾损伤,是产后AKI的常见原因。
诊断评估应包括尿液分析、尿液显微镜检查、全面代谢检查、凝血检查、适当的血清学检查以及对用药史的全面检查。妊娠期血清补体水平升高是因为肝脏合成增加,这使得狼疮性肾炎的诊断变得复杂。 应当进行肾脏超声检查以排除梗阻性原因所致AKI,例如病理性肾积水。由于妊娠期高凝状态,如怀疑栓塞性疾病, 应行多普勒超声检查。妊娠中晚期AKI的常见原因,如先兆子痫、HELLP综合征、TTP、aHUS、AFLP和狼疮性肾炎,可能会有重叠表现,需要详细评估。
当实验室评估AKI无法下诊断时,可以考虑肾活检,因为明确诊断有助于采取合适的治疗,超过活检带来的风险。肾活检的决策要基于妊娠时期、可用的治疗方案和妊娠活力。妊娠晚期的活检有更高的并发症风险,尤其是妊娠25周后, 建议活检在妊娠早期和中期进行,最好避免在妊娠晚期进行活检,除非AKI治疗可显著改善母婴结局。
根据胎儿成熟度和肾功能下降对胎儿和母亲的影响,在可行的情况下,应 权衡提前分娩的可能性。对于妊娠晚期的孕妇来说,在活检前分娩可能是一个更为谨慎的选择,尤其是在胎儿已经达到存活能力的情况下。应与患者充分讨论并发症和风险,包括大出血需要输血、栓塞、严重产科并发症和胎儿死亡的风险。 AKI发生风险高的女性应在产后进行评估,定期监测血压、肾功能和蛋白尿情况,包括怀孕前患有CKD的女性和怀孕期间出现先兆子痫的女性。
妊娠期AKI的处理
妊娠期AKI的治疗应该由一个多学科团队来进行,由肾脏科医生、产科医生和新生儿医生组成。 治疗妊娠相关AKI的一般措施包括:确定肾损伤的原因,静脉液体复苏,必要时及时开始透析,必要时提前分娩。
静脉液体复苏对于肾前性AKI至关重要,但对于有先兆子痫的女性,因为有发生肺水肿的风险,因此应谨慎进行静脉液体复苏。肾损伤并发症的治疗方法与非妊娠患者相似,例如,对代谢性酸中毒使用补碱疗法,对容量超负荷使用袢利尿剂,对贫血患者输血,对高钾血症使用钾结合剂。
AKI的特异性治疗取决于肾损伤的根本原因。 肾小球肾炎的治疗包括类固醇和免疫抑制剂,当对孕妇使用时,应权衡风险和益处。抗代谢药物,如霉酚酸酯,由于其致畸性,在妊娠期间禁用。妊娠期间或可使用低剂量类固醇,但需监测妊娠期糖尿病的发生。 硫唑嘌呤和钙调神经磷酸酶抑制剂(环孢素和他克莫司)不是致畸药物,是妊娠期常用的免疫抑制药物。妊娠期间需要较高剂量的他克莫司和环孢素来达到治疗目标,因此应经常监测药谷浓度。
重度先兆子痫、HELLP综合征和AFLP的治疗,需要及时分娩。 如果在妊娠34周前分娩,则应给予糖皮质激素以降低新生儿呼吸窘迫综合征的风险。
血栓性微血管病(包括TTP)和非典型HUS的治疗,包括血浆置换和依库珠单抗(用于aHUS)。ADAMTS13缺乏性血栓性微血管病(TMA)的患者,治疗目标是通过血浆置换恢复酶活性,如果血浆置换失败, 利妥昔单抗是一种治疗选择。但妊娠相关TMA应谨慎使用利妥昔单抗,在不到10%的新生儿中观察到了胎儿毒性(血小板减少、嗜中性粒细胞减少和B细胞减少),短期获益还是存在的,目前还没有研究对利妥昔单抗在新生儿中的长期安全性进行评估。
总结
妊娠期AKI与孕产妇死亡率增加以及孕产妇和胎儿不良结局有关。在怀孕期间,应定期监测肾功能,特别是高危女性。妊娠期AKI的诊疗需要一个多学科团队来对孕妇进行管理,以改善产妇和胎儿结局。目前,妊娠期AKI仍然没有得到充分的认识,需要继续探索其长期影响。
参考文献:
Adv Chronic Kidney Dis. 2020;27(6):455-460.
京东健康互联网医院医学中心
作者:杨超,毕业于北京大学医学部,现在北京大学第一医院工作,研究方向为慢性肾脏病。
展开更多
展开更多





























