简称:
沐川县利店镇卫生院,成立于2020年,位于四川省乐山市,宗旨和业务范围是“为人民身体健康提供医疗与预防保健服务。常见病多发病诊治,院前急救,巡回医疗,计划生育服务.”。该事业单位开办资金64.4万人民币
-

心力衰竭患者管理中,针对残余充血的治疗是最大的难解决问题之一。袢利尿剂是缓解充血的基础疗法,可以减少循环血容量以减少血管内充血。然而,与无电解质的排水利尿药物相比,袢利尿剂可使循环血液的渗透性降低,这可能导致当超过血浆再灌注率时,液体从组织(肺、腹部和周围)到血液循环的转移较慢。循环血容量下降,但没有组织中类似容量的液体转移到血液中,会导致神经激素激活,可能进一步导致肾功能恶化,与此同时患者还伴随着持续的充血症状体征,如呼吸困难、肺部啰音和外周水肿。
流行病学
充血性心力衰竭定义为钠和水潴留导致心脏充盈压力增加,从而导致血管内腔室和间质内液体积聚。充血是急性(失代偿)心力衰竭患者住院的主要原因,但充血的严重程度因患者而异。
在一项大型、长期随访的欧洲注册登记研究中,83%的急性心力衰竭住院患者有充血的临床体征或症状。一项针对心力衰竭住院患者的大型全球队列研究发现,外周水肿的发病率从东南亚的39.2%到东欧的75.2%不等,肺部啰音的发生率从北美地区的23.9%到非洲地区的80.6%不等。
临床充血评分可以用来评估充血的程度。大多数临床充血评分是端坐呼吸、颈静脉充盈和肺部啰音严重程度的综合性评估。针对急性心力衰竭患者充血发生情况的临床试验表明, 临床显著充血(充血评分为3-18分)的发生率高达97%,然而,这些试验的纳入标准要求患者入组时的充血分数≥1,在分析中排除了无充血体征或症状的患者,得出的充血总发生率可能有误差。大约90%的充血患者会出现呼吸困难症状,针对大多数患者,需要开始或加强袢利尿剂治疗。
患者出院时伴有不完全充血与较高死亡率和心力衰竭再住院率相关。与无充血的患者相比,住院第7天有残留充血的患者,180天死亡率增加了两倍以上,心力衰竭再住院风险也几乎增加了两倍。
血管内充血的评估
目前,评估血管内充血的金标准是 测量右心房压(正常为2-6mmHg),以及右心导管测量肺毛细血管楔压(PCWP;正常为3-8mmHg)。但右心导管插管是侵入性的操作,因此,不推荐常规进行。为了评估充血的每天变化情况,需要进行无创测量,如颈静脉压的变化、患者报告症状、或入院到出院间的血浆利钠肽水平的变化。
组织充血的评估
组织充血可以根据患者症状和体格检查来评估,确定的指征包括出现肺部啰音、腹水和外周水肿。凹陷性水肿对于间质性水肿具有高度的特异性,但大多数临床体征和症状对于诊断心衰所致间质性水肿的特异性一般,敏感性也较差。组织充血也可以用生物标志物(如肾上腺髓质素血浆水平,可溶性CD146)和影像学检查(如胸片、肺部超声、胸部CT)进行评估。
充血的治疗
促进尿钠排泄增加的药物
袢利尿剂和噻嗪类利尿剂:心力衰竭指南目前推荐使用袢利尿剂和/或噻嗪类利尿剂来缓解慢性或急性心力衰竭患者的充血体征和症状,包括射血分数保留的心力衰竭患者。袢利尿剂和噻嗪类利尿剂降低(心血管)死亡率的作用尚未得到证实,但一项荟萃分析显示袢利尿剂和噻嗪类利尿剂可以降低心力衰竭恶化和死亡的风险,这些药物似乎还可以提高运动能力。
盐皮质激素受体拮抗剂:盐皮质激素受体拮抗剂有抑制醛固酮的作用,从而增加钠排泄和钾保留。两项大型随机临床试验表明,盐皮质激素受体拮抗剂对射血分数降低的慢性心力衰竭患者有疗效。在心梗后左心室功能不全的患者中,每天服用25-50mg依普利酮的患者比服用安慰剂的患者体重明显减轻,血药浓度明显升高,表明依普利酮具有利尿作用。然而,在针对严重慢性心力衰竭患者的RALES试验中,接受12.5-50.0 mg螺内酯(相当于25-100 mg依普利酮)的患者,钠排泄没有增加。其他研究表明每日≥100mg的螺内酯可增加钠排泄,但与标准治疗相比,并未使得急性心力衰竭患者的充血有更好的缓解。
促进液体重分布
加压素拮抗剂 :增加无电解质的水排泄。通过增加无电解质的水排泄而不是钠排泄,血管内渗透压升高,从而使体液从间质迁移到血管。EVEREST 试验是关于托伐普坦(一种V2受体拮抗剂)对心力衰竭患者影响的首个也是最大的试验,研究结果显示,与安慰剂相比,托伐普坦治疗对心力衰竭患者的主要终点(全因死亡率和心血管死亡或住院率)无改善。然而,在EVEREST和TACTICS-HF试验中,托伐普坦对呼吸困难、临床充血评分、体重变化和/或净液体流失有短期的有利影响,这些影响在低钠血症患者中最为显著,提示托伐普坦治疗对改变血浆渗透压的重要作用。托伐普坦治疗急性失代偿性心力衰竭患者的失水和呼吸困难的有益作用已在其他几项研究中得到证实。
SGLT2抑制剂:促进尿钠排泄并增加渗透性。研究显示,在射血分数降低的心力衰竭患者中,与安慰剂相比,SGLT2抑制剂达格列净治疗可降低心力衰竭患者的死亡率和住院率。尽管这一益处的机制仍有待阐明,但利尿钠作用通常被认为其中的关键。然而,有一项研究假设其对无电解质的水排泄的作用更大,这表明使用 SGLT2抑制剂或可治疗组织充血,类似于使用加压素拮抗剂。在心力衰竭患者中使用SGLT2抑制剂的其他试验的结果预计将很快公布。
高渗盐水:增加渗透压。从理论上讲,输注高渗盐溶液会增加血管内隔室的渗透压,从而吸引来自间质和细胞的液体;此外,人们认为肾脏血流量增加,可能导致利尿剂在其作用部位(如肾脏)的利用率会提高,也就是说会提高利尿剂的效果。一项初步研究显示,针对急性心衰患者,与单独使用袢利尿剂相比,袢利尿剂加上高渗盐水输注可使体重下降更多,改善肾脏功能,减少住院时间、再住院率和死亡率。但是,还有待高质量随机临床试验来验证。
参考文献:
Nat Rev Cardiol. 2020; 17(10):641-655.
京东健康互联网医院医学中心
作者:姚佑楠,就读于北京协和医院阜外医院。从事心力衰竭相关工作,研究方向为心衰管理、质量控制以及药物经济学。
-

-
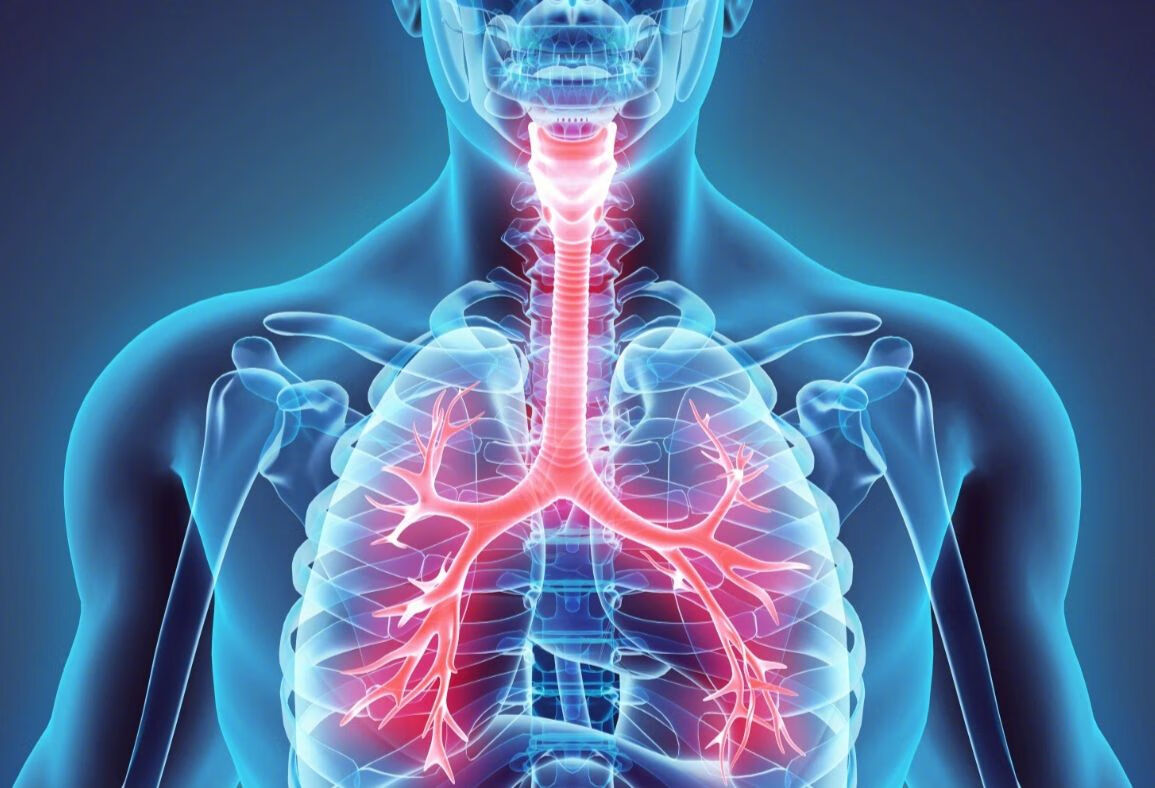



参考文献:
[1] 支气管扩张症专家共识撰写协作组, 中华医学会呼吸病学分会感染学组.中国成人支气管扩张症诊断与治疗专家共识 [J].中华结核和呼吸杂志 , 2021, 44(4): 311-321.
[2] 梁艳等. 支气管扩张症的治疗概述及进展[J]. 中西医结合心血管病杂志, 2018, 6(31):173-176
[3] 冯明发,张薇.支气管扩张症合并慢性阻塞性肺疾病的研究进展[J].临床与病理杂志,2021,41(10):2461-2467.
[4] 彭翠兰.成人支气管扩张症病原菌分布及咯血原因分析[J].中外女性健康研究,2019(03):119-120.
[5] 徐小勇,施毅.支气管扩张的诊断和治疗进展[J].中国呼吸与危重监护杂志,2017,16(02):186-190.
[6] 杨妹,霍建民.支气管扩张病因相关疾病的研究进展[J].临床肺科杂志,2022,27(04):607-611.
[7] 刘雪健,王佳贺.支气管扩张症微生物感染的研究进展[J].中国医科大学学报,2022,51(03):263-266.
-

要论当代「打工人」什么时候最有干劲,除了发工资,那干饭绝对当仁不让。
一句“走,干饭啊”能让年轻人瞬间提起精神。
干饭虽好,切莫太猛
现如今,短视频APP火爆,越来越多的年轻人走向「吃播」道路,不少播主为了博流量,用「吃了吐,吐了吃」办法,显示自己是大胃王。很多播主都是一顿吃饱,三天不饿。
然而,这样的吃法真的存在巨大风险。
前段时间,新闻报道了一位年仅19岁网红吃播脑溢血去世;两月后,又有新闻报道29岁的网红吃播于某某也不幸离世,他们都曾长期从事吃播工作,并且经常暴饮暴食,长期使用高热量、高碳水、油腻的食物。
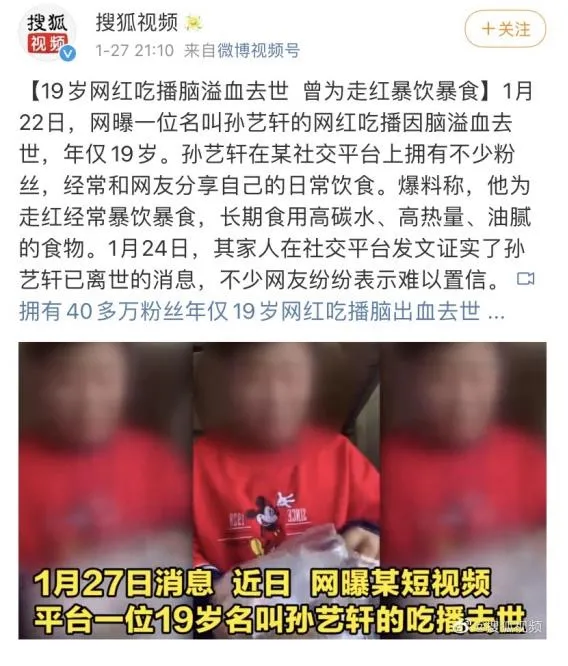
图片来源:微博截图
就在前些天,我们医院急诊来了一位年轻女性,体重80kg,15小时前在进食有油腻性食物后出现上腹胀痛,呈持续性、阵发性加重,向腰背部放射,伴有恶心呕吐,伴肛门排气排便停止。CT提示:胰腺及周围组织改变,考虑急性胰腺炎。给予重症监护、抑制胰液分泌、抗炎、抑酸、液体复苏、脏器支持等治疗。
当天下午,患者出现休克、严重呼吸急促、腹胀,腹压高达46cmH2O,诊断为SAP合并ARDS,给予手术、气管插管、抑酸、脏器支持、抗感染等治疗,由于病情过于严重,患者最终因休克伴严重感染伴ARDS抢救无效不幸身亡。
本以为暴饮暴食引发生命事故离自己很遥远,但真的发生在自己面前时,才真的感受到生命的有多么脆弱。
其实,医生们都知道,人们每一次的胡吃海喝,都是在「急诊科」的边缘试探!
贪吃一时爽,但是贪吃也会带来一系列的疾病,肥胖、疲劳、脂肪肝、胆囊炎、胃肠炎、胃出血、骨质疏松等,都可能与暴饮暴食有关。
暴饮暴食引发的这一疾病高发
有一种因暴饮暴食引发的疾病,近年来在年轻群体中尤其高发,这种疾病发展凶猛,让人措手不及,这就是急性胰腺炎。
急性胰腺炎是急诊常见的一种消化系统疾病,并且现在年轻人得这种病的越来越多。其中,每5个轻度急性胰腺炎的患者就有一人会发展为中度或重度胰腺炎,一旦病情加重,就会大大增加疾病死亡概率,最高可达到35%,相当于三分之一的患者会死亡(来自《急性胰腺炎急诊诊断及治疗专家共识(2021年)》)。不仅增加经济负担,更有可能会人财两空。
在我们食入大量的高蛋白高脂肪食物后,身体里的胰腺在接收到这种信号后,就会促使胰液的大量分泌,与此同时胰腺胰管如伴有排泄障碍,胰液在胰管内返流或阻塞,造成管内压力增高,胰液外溢,而胰液又含有丰富的消化酶,消化酶在胰腺自身内活化而产生自溶,从而引起胰腺炎。食入量越多,胰液也越多,疾病也就越严重,身体不舒服的现象也就越明显。
所以,在饱餐后,出现肚子疼、发热、恶心呕吐等不舒服时,一定要及时寻求医生帮助。
另外,吃得过饱也会影响血液的流动,血液会堆积在胃肠道,而造成大脑血液减少,不仅会造成大脑反应迟钝,经常暴饮暴食还会加速大脑衰老,甚至可能会诱发老年痴呆 [5-6]。
多数人都存在暴饮暴食
那么,怎样才算是暴饮暴食,有没有什么判断标准?
问:我比一个胖子吃得多,算不算暴饮暴食?
问:每天睡觉前,都要再吃点东西,算不算暴饮暴食?
问:我中午吃的火锅,晚上又吃的烤肉,算不算暴饮暴食?
其实,暴饮暴食的两个明显特点:
1. 吃进去的食物严重超量。我们每天吃进去的量肯定是严重超出自己平时吃进去的量。严重超量和我们平时说的「吃多了」不一样,必须是严重超出才是暴饮暴食,比如我们白天一天不吃饭,但晚上那一顿把这一天该吃的食物都吃了。
2. 短时间摄入大量食物。由于工作、学习等一些原因,不得不在很短的时间内,毫无节制、又猛又急、狼吞虎咽似的吃了大量的食物。
不得不说,当下很多年轻人以及中年人,因为高强度的生活节奏,不可避免的存在些许暴饮暴食现象。那么,想要避免暴饮暴食,该怎么做?
以下这三个方面是相对有效且容易做到的:
规律的生活方式。避免节假日期间的不规律饮食、过度酗酒等。健康的饮食规律基本是定时定量,一日三餐,少吃或不吃零食。做到“四低一高”,即低能量、低脂肪、低胆固醇、低糖、高纤维膳食。
有效的减压。运动已经成为不同年龄段首选的舒缓压力、强身健体的方式,可以帮助排遣压力和不快。随着时间的延长、强度的增加,运动效果逐渐体现。小强度的运动可以转移注意力,舒缓郁闷或紧张的情绪,达到减轻抑郁的效果。
摆脱情绪性进食。在吃东西前,先喝杯水,这让你能缓解情绪,而且感觉到肚子饱饱的。用低热量的食物,蔬菜和水果塞饱肚子。
参考文献:
[1]陈洋.别跟“吃播”学,暴饮暴食伤不起[J].大众健康,2020(10):86-87.
[2]急性胰腺炎急诊诊断及治疗专家共识(2021年)
[3]陕旦旦.浅谈暴饮暴食产生的原因及改善方式[J].当代体育科技,2020,10(10):27-28.
[4]韩真真.暴饮暴食提防胰腺炎[J].开卷有益-求医问药,2021(03):6-7.
[5]李端. 高脂饮食引发老年痴呆[J]. 中老年保健, 2009(1):7-7.
[6]宋红, 付霞, 陈博. 血糖、血脂异常对老年痴呆患者认知状况的影响[J]. 重庆医学, 2015, 44(020):2847-2849.
-

与未患癌症的急性冠状动脉综合症(ACS)患者相比,患有癌症的ACS患者是一个特别高危的群体。目前美国心脏病学会和美国心脏协会(ACC/AHA)指南建议,对ST段抬高型心肌梗死(STEMI)患者以及非ST段抬高型心肌梗死(NSTEMI)和不稳定型心绞痛(UA)的高危患者采取 早期侵入性血管造影诊断的策略,并计划进行血运重建。然而,考虑到较高的出血风险和手术风险,ACS伴癌症患者并没有接受侵入性治疗,也没有像非癌症患者那样接受抗凝和抗血小板治疗。
此外,许多癌症治疗包括化疗和放疗,都会增加ACS的发生风险,最终导致这些患者的死亡率非常高。随着癌症治疗以及与这些恶性肿瘤相关预期寿命的不断提高,越来越多的患者患上冠状动脉疾病,包括ACS。这凸显了更好管理这些复杂患者的重要性。
ACS癌症患者的预后
ACS伴癌症患者的死亡率非常高,一项回顾性分析发现,总体1年生存率为26%。ACS患者结局与转移性疾病、血栓形成和出血并发症相关,某些类型癌症患者也有很多与ACS相同的风险因素,包括肥胖、吸烟、年龄和糖尿病。
还有研究显示,在癌症诊断后的6个月内,新诊断冠心病(CAD)发生率更高,这支持了共同危险因素的理论。一项回顾性研究评估了456名诊断为急性心肌梗死的癌症患者的结局。结果显示,接受阿司匹林的患者死亡风险降低了23%,使用β阻断剂的患者死亡风险降低了36%,接受阿司匹林和β-阻断剂的患者人数分别为46.3%和48.5%。导管植入为基础的血运重建并未影响死亡风险,但只有2.8%的NSTEMI和5.7%的STEMI患者接受了血管重建。这项研究表明,心肌梗死伴癌症患者的治疗不足,这类患者可以从阿司匹林和β-阻断剂治疗中受益。
最近,一个多中心注册登记研究发现,在ACS患者中,与非癌症患者相比,合并癌症的患者的1年死亡和再次梗死的复合终点发生率更高。重要的是, 癌症患者确实可以从β-阻断剂、血管紧张素转换酶抑制剂(ACEI)和血管紧张素受体阻断剂(ARB)、他汀类药物和双重抗血小板治疗中获益。
癌症患者的冠状动脉造影建议
癌症患者常被排除在与抗血小板治疗、抗凝治疗和ACS侵入性治疗相关的随机临床试验之外,主要原因是 贫血和血小板减少。癌症患者中与PCI有关的出血风险,大部分源于血小板减少,这可能与恶性肿瘤本身或与治疗有关。然而,这种获得性血小板减少相关的出血风险,与使用抗血小板、糖蛋白(GP)IIb/IIIa抑制剂、肝素或溶栓治疗药物所致的出血风险不同。
事实上,存在矛盾的是,癌症患者的血小板减少还与血栓形成风险增加相关,对于那些血小板小于100 k/uL的患者,癌症患者使用阿司匹林治疗可显著改善ACS后7天生存率。荷兰支架血栓注册研究的数据显示,在所有病例中,活 动性恶性肿瘤与支架血栓的高发生率有关,在因稳定型心绞痛而进行PCI治疗的患者中风险更大。因此,需要谨慎选择患者,以帮助指导ACS癌症患者的侵入性策略。
2014年AHA/ACC非ST段抬高ACS患者管理指南指出,在ACS合并癌症的患者中,血运重建的风险和合并症可能超过血运重建的益处。由于癌症合并ACS患者的高死亡率以及缺乏随机临床试验数据,心血管血管造影和介入学会(SCAI)就这一人群的冠状动脉介入建议发表了共识声明。对于 血小板<50,000/mL的患者,可以用较低剂量(30-50U/kg)的肝素进行治疗。对于双重抗血小板的使用,如果血小板大于30,000/mL,可以考虑使用 氯吡格雷。
当 血小板<50,000/mL时,不应使用替格瑞洛、普拉格雷和糖蛋白IIb/IIIa抑制剂。对于大多数 血小板>10,000/mL的患者,可以安全地给予81mg阿司匹林。不建议在进行心导管手术前输注血小板,除非血小板计数<20000/mL,并伴有高热、白细胞增多、血小板快速下降或存在其他凝血病的患者。
对于 血小板计数<20,000/mL且正在接受膀胱、妇科或结直肠肿瘤、黑色素瘤治疗的患者,应考虑在导管手术前输注血小板。在进行心导管检查时,如果可能的话,应使用超声引导、微针穿刺针和桡动脉通路,以减少出血风险。
对于ACS伴癌症预后不佳的患者(估计生存期<12个月),由于1年死亡率极高,应对STEMI和NSTEMI患者提供PCI治疗。由于半衰期较短,在PCI过程中,比伐卢定可能是替代肝素的首选。稳定型心绞痛患者应最大限度地进行药物优化,对于持续难治性心绞痛患者,可以考虑PCI治疗,可以作为一种缓和的选择。在这些患者中,可以在导管检查时利用分数流量储备(FFR)或瞬时无波比(iFR),以确保对具有模式意义的病变进行干预。
对于多血管疾病、预期寿命大于12个月、可治愈的恶性肿瘤、血小板大于50,000/ml的手术候选者,冠状动脉搭桥手术可能是合理的。如果需要进行癌症相关手术的患者需要进行PCI手术,可以考虑采用球囊血管成形术或新一代药物洗脱支架,以将需要DAPT的时间长度分别减少到2-4周。
有研究者建议在患有ACS的癌症患者中使用 心肌梗死溶栓治疗(TIMI)风险评分,如果TIMI评分小于3分,进行一些药物治疗(阿司匹林、β-受体阻滞剂、他汀类药物、缺血评估)是合理的。在TIMI评分大于或等于3分的患者中,则建议进行冠状动脉造影,并计划进行血运重建。
总结
ACS伴癌症患者的最佳治疗方法目前还不清楚,也会因为合并症不同而产生差异。但根据目前可用的回顾性数据,许多伴有ACS的癌症患者目前治疗不足,可能会从阿司匹林中获益(血小板大于10,000/mL),氯吡格雷(如果血小板大于30,000/mL)、β-受体阻滞剂、他汀类药物和ACEI或ARB。伴有STEMI、NSTEMI、UA的所有癌症患者都应考虑进行侵入性治疗,除非有绝对的禁忌症。
参考文献:
Curr Cardiol Rep. 2020;22(12):159.
京东健康互联网医院医学中心
作者:刘山水,医学博士、副教授。研究疾病领域为老年疾病及常见慢病,已在国内外医学期刊发表署名论文80余篇。
-


说到减肥,就很容易能让人联想到运动,而说到运动,最先能与之“挂钩”的便是跑步。是的,放眼当前的“减肥大军”,跑步减肥已经成为了一种时尚和流行趋势,越来越多的人加入了跑步减肥或者跑步维持体重的行列。那么问题来了,运动的确有益健康,可对于当前体重处于肥胖状态的胖友们来说,跑步减肥真的健康吗?对于这个问题,骨科医生是这样说的。
跑步减肥损伤膝关节
骨骼,是人体最重要的组织之一,担负着人体负重、支持、保护、运动、造血等等重要的生理作用。不同的运动方式对于人体骨骼的影响也会截然不同,当人的运动强度太大或者运动量太大时,则极易引起关节软骨不可逆性的损伤。关节软骨,位处于关节处的骨头与骨头之间,可避免骨头间直接硬碰硬的摩擦和震动,具有缓冲震荡、保护关节骨面作用。在运动过程中,如果运动强度或者运动量超过软骨组织所承受的负荷,无论是超过临界值的单次冲击,还是小于临界值的多次大幅度的钝性刺激,均可能会造成关节软骨的损伤,而且人体的关节软骨在受损后多为不可逆性的伤害。
膝盖损伤发现之时已经晚了
需要注意的是,骨骼间的软骨就像薄薄的冰层那样光滑且脆弱,它不含血管、神经、以及淋巴组织,所需要的营养主要来源于滑液的弥散。因此,不但关节软骨的自我修复能力很弱,当关节软骨受损时,人们也通常不会有疼痛感,直至它被磨损殆尽,损伤直接延至骨头时,人们才会因骨骼上神经的疼痛引发注意,但往往这时的病情已经比较严重,甚至需要住院治疗。

肥胖的人不适合跑步减肥
当今社会,跑步已经是非常普遍的、被平民化的运动方式,但事实上跑步并非适合所有的人群,尤其对肥胖患者来说,跑步并非减肥良方。肥胖的人,即使在静止状态下,其膝关节所承受的压力也会高于体重正常的人,如果在身体负重较重的前提下,还经常跑步,则会给膝关节带来更大的压力。关节软骨处因为没有神经,无法对磨损和伤害及时做出应激反应并让人可以及时止损,只有在软骨被磨损到一定程度时,才会感到某种不适。因此,体重超重或者肥胖的人,如果因经常跑步而导致软骨受到损伤,被发现时通常伤害已经不可逆转,只能通过手术来解决问题了。
适合减肥的运动方式
运动减肥虽然能够让人健康的变瘦,但在减肥过程中却应该谨慎的选择运动方式,在身体的体重还不允许的前提下,应尽量避免用跑步的方式减肥。其实,有很多运动方式都比跑步更加适合消耗人体的能量,如游泳、骑单车等,如果实在喜欢行走的运动方式,在减肥初期也可以选择快走这一运动项目。快走与跑步属于同一类型的运动,同一时间段内虽然消耗的热量稍小于跑步,但其对关节处的伤害也远远小于跑步。减肥本就不是一朝一夕就能完成的事情,只有坚持下去才能看到成功的希望,从这个角度上来说,快走也比跑步更适合减肥者,您认为呢。
-

全球范围内,三分之一的女性死亡原因是缺血性心脏病(IHD)。虽然育龄女性IHD的患病率较低,但就目前的趋势而言,如孕妇年龄增加,孕妇糖尿病、肥胖和高血压患病率增加,可能导致了这类群体中冠状动脉疾病的患病率增加。此外,有研究证实,怀孕本身就会比同龄非怀孕女性的急性心肌梗死(AMI)风险更高。心脏病是孕产妇死亡的主要原因,IHD占心脏病病因的五分之一以上。
妊娠期心肌梗死的患病率
据报道, 妊娠期心肌梗死的发病率为6.2/10万妊娠。动脉粥样硬化仍然是妊娠期AMI的最主要原因,其他原因也比非妊娠人群更为常见。孕妇AMI的各种病因患病率如下:冠状动脉粥样硬化伴或不伴冠状动脉内血栓(27%–40%)、自发性冠状动脉夹层 (SCAD,27%–43%)、冠状动脉内血栓不伴动脉粥样硬化(8%–17%),冠状动脉痉挛 (2%)。
对2006-2011年间150例AMI患者的类型和时间进行分析发现,大多数患者表现为ST段抬高型心肌梗死(STEMI,75%),其余患者表现为非ST段抬高型心肌梗死(NSTEMI)。大多数事件发生在妊娠晚期(STEMI,25%;NSTEMI,32%)或产后(STEMI,45%;NSTEMI,55%)。梗死累及左室前壁(69%)、下壁(27%)、侧壁(4%)。
冠状动脉疾病的药物治疗和孕期安全性
大多数用于IHD的药物,不管是治疗AMI或用于心血管疾病的二级预防,可以在怀孕和哺乳期间继续使用,但有一些药物例外。如果有致畸性或其他对胎儿有害的影响,建议停止该药物。此外,可能需要调整药物剂量,因为妊娠期间的血流动力学变化会影响药代动力学。 他汀类药物在孕期和哺乳期禁用,但是这些女性在孕期和产后停药,发生AMI的风险可能会增加。
使用冠状动脉造影的注意事项
对于急性斑块破裂导致的STEMI,建议通过经皮冠状动脉介入治疗(PCI)和支架植入及时进行冠状动脉再灌注。基于妊娠期间事件发生的时间以及出血风险,选择药物洗脱支架(DES)还是裸金属支架(BMS)。DES再狭窄的风险较低;然而,与BMS相比,会需要更长时间的抗血小板药物治疗(12个月vs 1个月)。考虑到BMS可缩短抗凝治疗时间,BMS可能是有优势的,尤其是在分娩期间。
血管造影是妊娠期IHD诊断的金标准。然而,只有60%的AMI女性接受了冠状动脉造影,部分原因是担心会对胎儿产生危险。目前可接受的妊娠期辐射累积剂量为50mGy,一个重要影响因素是妊娠所处时期。在妊娠的头2周,无论辐射剂量多大,都可能导致自发流产。妊娠第3周到第8周,出生缺陷、流产或生长迟缓的风险较低,除非辐射量超过200 mSv。妊娠8至15周,对中枢神经系统(CNS)的风险较高,包括小头畸形和其他CNS畸形,辐射阈值为300 mSv。
重组组织型纤溶酶原激活剂进行溶栓
在无法进行PCI的情况下,必要时可考虑使用组织型纤溶酶原激活剂(TPA)。以前人们认为妊娠期间应禁止溶栓,但新数据表明,妊娠期使用TPA的风险并不高于非妊娠女性。要注意的是,在冠状动脉夹层所致心肌梗死患者中,溶栓可能会加重出血和夹层。
妊娠期自发性冠状动脉夹层
普通人群中,自发性冠状动脉夹层(SCAD)并不是AMI的常见病因; 但妊娠期AMI中 ,SCAD可占到27%-43%。SCAD的典型表现与AMI相似,伴有胸痛、呼吸困难和出汗。SCAD诊断通常比较困难,因为典型患者通常是年轻人,没有其他可识别的心血管危险因素。
基于研究的发现,对于患有纤维肌发育不良(25%–86%)、处于妊娠期(2%–8%)、有结缔组织疾病(1.2%–3%)、全身炎症(<1%–8.9%)、服用外源性激素(10.7%–12.6%)和诱发应激事件的患者,应怀疑SCAD的可能性。超过50%的患者会报告有促发因素,包括分娩、服用外源性激素、高强度运动。妊娠期SCAD的潜在机制尚不完全清楚,可能是妊娠期间动脉壁激素减弱时血液动力学压力增加的结果。
自发性冠状动脉夹层最初的临床表现为心源性休克(2%-5%)、STEMI(26%-87%)、室性心律失常或心源性猝死(3%-11%)。在一项包括168名患者的队列研究中,所有患者都出现了肌钙蛋白I水平升高。患者的左心室射血分数通常保持不变,但超声心动图或早期血管造影可发现左心室壁运动异常。
任何动脉都可能受到影响, 左前降支最常见,可占到32%-46%。与非孕期SCAD的管理类似,建议大多数孕妇采用 保守治疗并住院监测。在一项包括131例SCAD病例的观察性研究中,自发性愈合率为88.5%,35天后,所有患者的血管造影均观察到愈合。在需要做血管造影的病例中,需要注意球囊膨胀或支架扩张所产生的径向力可能导致夹层;在PCI前对SCAD提高警惕是有必要的。
在对孕期自发性冠状动脉夹层 (P-SCAD)与非孕期自发性冠状动脉夹层 (NP-SCAD)的比较中,P-SCAD更多表现为急症,包括STEMI (57% vs 36%),左主血管或多血管SCAD (24% vs 5%),以及左心室功能≤35% (26% vs 10%)。
P-SCAD最常发生在产后第一个月。在2000-2015年进行的一项荟萃分析中,有超过120例发生了妊娠期SCAD,超过87名患者(72.5%)发生在产后第3天至第210天之间。与NP-SCAD相比,P-SCAD患者伴有纤维肌发育不良和冠状动脉外血管异常的可能性更小。
临床诊疗建议
1. 已有IHD的女性应在怀孕前接受全面的心脏评估。
2. 现有的工具如CARPREG Ⅰ、CARPREG Ⅱ、ZAHARA和改良WHO分类,通常可用于先天性心脏病、瓣膜病和心肌病的评估,但在IHD女性的风险评估中作用有限。
3. 从现有趋势来看,如孕妇年龄偏大、合并症患病率增加,可能导致妊娠期IHD的发病率增加。
4. 识别和治疗妊娠期间自发性冠状动脉夹层和冠状动脉痉挛非常重要,因为其临床表现可能不典型。
5. 大多数用于IHD或心血管疾病二级预防的药物可以在怀孕期间继续使用,但某些药物除外。
参考文献:
Cardiol Clin. 2021;39(1):91-108.京东健康互联网医院医学中心
作者:龚志忠,首都医科大学硕士,研究生期间在北京安贞医院主要从事心血管病流行病学研究,已参与发表英文SCI论文2篇,中文核心期刊论文3篇,参与编写出版著作2部。
-
随着人们生活方式和工作条件的改变,用眼时间越来越多,如长时间看电脑、看电视玩电子游戏等,长期如此很容易导致视觉疲劳,出现眼睛干涩、眼红等症状。
为了避免这些问题,不少人将眼药水视为“居家必备”,但眼药水能长期使用吗?眼药水的正确使用方法是什么?眼药水勿长期使用,不少人会在熬夜,眼睛疲劳、有红血丝的情况下,使用抗疲劳眼药水,以保证眼睛清凉、通透。实际上,眼药水虽能缓解视觉疲劳,但也不能长期使用。
01 含有肾上腺素类药物,抗疲劳眼药水,一般都含有肾上腺素类药物,这类药物能起到收缩血管的作用,使用后,药效明显,可以让眼睛在短时间内,不再充血,眼红症状消失。不过,需要注意的是,类似肾上腺素类的药物药效过后,眼睛又将大范围充血,而且会红得更厉害。因此这类药物,不可长期使用,以免影响血管正常收缩。
02 含有缩小瞳孔、抗过敏的成分,抗疲劳眼药水中,还含有缩小瞳孔的成分,随着瞳孔缩小,使用者眼睛会更聚焦,看东西更清楚,但长期使用,则会影响瞳孔的舒张功能。抗疲劳眼药水中的,抗过敏成分,可适当缓解眼痒症状,宜短时间内使用。提醒大家,抗疲劳眼药水,虽然可以短时间使用,但在使用前也要获得医生许可。
03 患上干眼症,眼药水中大多含有防腐剂,若长期使用,会使眼睛的结膜杯状细胞发生损伤,导致患上干眼症,造成眼睛发红、干涩或疼痛。因此,使用不宜太过频繁,每天点眼药水3~4次较为合适。
眼药水的正确使用方法
01 检查眼药水,使用眼药水前,除了注意有效期和包装完整度,还需认真阅读说明书,了解成分、用法、用量,注意事项、有效时限等。
建议大家,在眼药水瓶或盒子上,标记开瓶日期,避免忘记哦!
02 正确滴眼步骤
第一步:清洁双手,打开瓶盖,避免瓶盖瓶嘴接触其他物品,以免污染;第二步:头部尽量向后仰或平躺下来,用食指将下眼睑下拉与眼球分开;第三步:将眼药水瓶嘴对准眼睛,点在结膜穹窿内,滴1~2滴即可。注意,眼药水瓶嘴尽量不要接触到眼睛或睫毛,以防药瓶受污染,点完药水后应立即盖上瓶盖。第四步:闭眼休息至少5分钟,避免眨眼。第五步:在睁开眼睛之前,用纸巾将流到眼睛周围的眼药水或泪水擦拭干净。提示:若需要点两~三种眼药水,每种应间隔5~10分钟;若需同时使用眼药水和眼药膏,应先点眼药水,隔5分钟再抹眼药膏。 -

经常有患者在门诊问我,自从生完孩子以后,腰一直都很痛,在我剖腹产的时候,麻醉医师在我腰部打了一针,是不是麻醉医师把我的腰给打坏了?
在这里,我可以很负责人的告诉大家,产后腰痛跟麻醉医生打麻醉一点关系都没有!
生孩子时打的麻醉叫“腰麻”,专业术语叫“硬膜外麻醉”,一般是在两个腰椎棘突间的韧带打一针,穿到腰部神经表面,再打入麻醉药!因为穿刺针非常的细,不会对我们的腰椎结构产生破坏,因此“腰麻”不是产后腰痛的罪魁祸首!那生完孩子后为什么会出现腰痛?原因比较多,我分析主要是以下3点:
1、10月怀胎,腰部承受更大的应力,导致腰骶部肌肉持续紧张,会产生腰肌劳损,这一点大家都能想得到!
2、此外,在怀孕期间,孕妇体内的雌激素、孕激素水平会发生变化,它们的变化会使全身韧带处于松弛状态,尤其是骨盆韧带的松弛,有利于分娩。但是它们也会导致腰部韧带(尤其是防止腰椎间盘突出的后纵韧带)松弛,使腰椎间盘容易突出,从而出现产后腰痛。
3、在生完孩子后,产妇喂奶姿势的不正确、抱孩子反复弯腰也会导致腰痛的加重。
那么如何解决产后腰痛呢?患者可以产后适当锻炼腰背部肌肉,保持喂奶姿势的正确(可参考我在好大夫写的文章:颈部及腰背肌锻炼(小燕飞和五点支撑)。
如果疼痛还是不缓解,而且没有母乳喂养,可以考虑吃点消炎止痛药,如果还在母乳喂养,尽量不要吃药,可以去正规的中医推拿科、康复理疗科做一些物理治疗等。

-

新生儿双侧永久性严重听力下降的患病率约为1.1例/1000新生儿;每1000名新生儿中可能还有1-2名发生双侧轻至中度听力下降或单侧听力下降。由于新生儿听力筛查策略的实施,目前听力下降检测出的年龄已大大降低。随着年龄的增长,儿童还会因多种病因失去听力,例如颞骨骨折、耳毒性药物、遗传性听力损失的延迟发作等,据估计,18岁以前儿童的听力下降患病率高达18%。早期识别儿童听力下降,进行早期干预,包括使用助听器和强化言语治疗,可带来更好的结局。
先天性听力下降
永久性先天感觉神经性和混合性听力下降的最常见原因是先天性巨细胞病毒感染,颞骨结构异常和遗传原因。先天性巨细胞病毒感染是导致听力下降的主要原因,也很常见。先天性感染,包括梅毒和风疹,也可能会导致听力下降。风疹曾经是先天性感觉神经性耳聋的最常见病毒原因,现在由于孕妇接种疫苗而变得罕见。
许多解剖异常也与遗传原因有关,包括腮-耳-肾综合征和CHARGE综合征。腮-耳-肾综合征是一种常染色体显性遗传性疾病,主要表现为听力下降、耳前瘘管、鳃裂发育异常、肾发育不良等。CHARGE综合征是一种罕见的常染色体显性遗传病,主要表现为:眼残缺、心脏病变、后鼻孔闭锁、生长发育障碍和/或中枢神经系统畸形、性腺发育不良、耳畸形和/或耳聋。
听力下降的发生率在早产儿中有所增加,并随胎龄和出生体重的增加而发生率下降。新生儿重症监护病房(NICU)中,1.2%至7.5%的婴儿会出现听力下降;出现以下情况时,NICU相关听力下降发生率会增加:高胆红素血症,败血症,新生儿细菌性脑膜炎,坏死性小肠结肠炎,长时间机械通气,耳毒性药物,使用体外膜肺氧合等。
迟发性听力下降
如果家长发现孩子的听力、说话或交流有些问题,需考虑到迟发性听力下降的可能性。如果存在围产期危险因素,例如先天性巨细胞病毒感染或体外膜肺氧合,也可能发生迟发性听力下降。超过119个基因与感觉神经性或混合性听力下降有关。其中,综合征占所有遗传原因的30%,常与迟发性或进行性听力下降有关,包括Pendred综合征,Usher综合征和Alport综合征。
Pendred综合征是遗传性感觉神经性听力下降的最常见综合征,与甲状腺功能不全、甲状腺肿、前庭导水管增大和Mondini内耳发育不全有关。 Usher综合征也是常染色体隐性遗传病,具有3种临床类型,可基于听力下降程度、前庭功能障碍和视力丧失发病年龄进行分型。 Alport综合征通常在儿童晚期发现,可出现肾功能衰竭、眼部异常和进行性感觉神经性听力减退。
一些非综合征性隐性基因也与进行性感觉神经性听力下降有关,这些儿童可能在新生儿听力筛查中表现正常,随着年龄增长而出现进行性耳聋。这些基因包括GJB2,MYO15A和STRC。进行性听力下降的常染色体显性基因包括TMC1和KCNQ4。
先天性感染后也可能发生迟发性听力下降。基于既往报道,产前暴露于弓形虫病、风疹、巨细胞病毒、疱疹病毒、梅毒等是先天性听力下降的常见原因。但是,这些微生物的流行病学已经改变,在许多国家,已剩下先天性巨细胞病毒感染是造成迟发性听力下降的主要原因。所有新生儿中先天性巨细胞病毒感染的患病率为0.4%至2.3%。在确诊为先天性听力下降的婴儿中,有6%至7%有先天性巨细胞病毒感染。但是,高达43%的先天性巨细胞病毒感染婴儿在新生儿听力筛查中正常,随后在婴儿期或儿童期出现感觉神经性听力下降。
前几年爆发了寨卡疫情,数据显示,先天性寨卡病毒感染可能导致听觉丧失。2019年对包含巴西、哥伦比亚和美国266名寨卡感染婴儿和儿童在内的10篇文章进行分析发现,听力下降发生率范围为6%至68%。还需要更多的研究来确定进行性听力下降的可能性,并更加明确听力下降的实际患病率。
获得性听力下降
出生后的获得性听力下降的原因包括创伤、感染、耳毒性药物使用或自身免疫性疾病。儿童听力下降中,大部分是由于获得性病因引起的。在导致儿童听力下降的可预防病因中,世界卫生组织将31%归因于感染,17%为产后并发症,4%为母婴使用耳毒性药物(如氨基糖苷类),8%为其他原因。
创伤可能导致传导性、混合性或感觉神经性听力下降,具体取决于颞骨损伤的部位和类型。鼓膜穿孔或听骨链损伤可导致传导性听力下降。颞骨骨折可损伤耳蜗、耳蜗神经或引起淋巴管瘘,这通常会导致严重的感觉神经性听力下降。颞骨震荡伤而没有骨折,也可能导致暂时性或永久性感觉神经性听力下降。
感觉神经性听力下降的感染原因包括麻疹、腮腺炎、水痘带状疱疹、莱姆病、细菌性脑膜炎等。与接种疫苗的儿童相比,未接种疫苗的儿童更容易患麻疹和腮腺炎并伴有听力下降。莱姆病可导致听力下降,但较罕见且可以治疗。听力下降常见病因为细菌性脑膜炎,可能是进行性的,最常见的是肺炎链球菌感染。
已知具有耳毒性并可能导致永久性听力损失的药物包括氨基糖苷类、抗肿瘤药(尤其是顺铂)、袢利尿剂;其他药物,例如水杨酸和大环内酯类药物(包括阿奇霉素),导致的听力损失通常是可逆的。密切监测药物剂量和血清水平可以减少内耳损伤的可能性。
自身免疫相关的听力下降原因包括局限于内耳的自身免疫功能障碍或系统性自身免疫疾病,例如Cogan综合征(间质性角膜炎、进行性听力损失和前庭功能障碍)。听力下降通常迅速进展,可能对免疫抑制剂有反应。
参考文献:
JAMA. 2020; 324(21):2195-2205.
京东健康互联网医院医学中心
作者:李延龙,北京协和医学院硕士,专业方向为慢性病的预防与控制。以第一作者或共同作者在国内外期刊发表论文10余篇。
展开更多
















