数月前,我在一篇文章中写了一个临床案例,一个IA期的男性肺腺癌病人,我的一个同事的父亲。这个患者在某省肿瘤医院手术后,由于分期很早,未行后续治疗,然而两年后出现锁骨上淋巴结转移,口服特罗凯半年后耐药,没多久就去世了。当时评论里很多网友在问,不是说早期肺癌治愈率很高吗?为何这么早期的肺癌却在短时间内发生了转移?
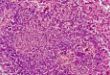
这个病人确实分期很早,在全省最好的肿瘤医院手术,手术方式也很正规,之所以这么快出现转移,主要原因是他的病理亚型是微乳头型。

以前讲过多次,肺腺癌的发展历程是腺瘤样增生—原位腺癌—微浸润腺癌—浸润腺癌。浸润腺癌根据术后病理分期分为I期、II期和III期,具体分期这里不再赘述。在浸润腺癌中又有许多的病理亚型,比如贴壁型、腺泡型、乳头型、实体型、微乳头型。不同的病理亚型中,具有不同的预后。一般来说,贴壁型的腺癌为低复发风险。腺泡型和乳头型为主的腺癌为中等复发风险;而微乳头与实体型腺癌则为有最高复发风险的病理亚型。
在肺腺癌的各种病理亚型中,微乳头成分被认为是最大的预后不良指标,常伴有转移,被认为是肺腺癌中预后最不好的病理亚型。有研究显示微乳头为主的腺癌,5年内复发概率较高。即使只有1%的微乳头成分,也会影响患者的生存。微乳头型肺腺癌常常在原发病灶很小时就容易出现广泛的淋巴管癌栓,更容易出现早期的远处转移,比如侵犯胸膜及骨转移。

2015年WHO肺部肿瘤分类中增加了微乳头为主腺癌作为主要的病理亚型。微乳头型腺癌发生率较低,我国统计资料其发生率不超过2%。其特点包括1.多见于中老年,病灶位于肺周边,以实性结节为主;2.具有小病灶,大转移的特点;3.多数发现时即为晚期,会表现为多发淋巴结转移,或者肺部广泛癌性淋巴管炎;4.即便早期,手术后的无复发生存时间在所有类型中最短。
通过上述分析,这个IA期病人两年后发生远处淋巴结转移也就不足为奇了。值得庆幸的是,微乳头型肺腺癌EGFR基因突变率很高,我国临床研究中高达85%。所以,这类病人最可能从EGFR靶向治疗中获益。
有微乳头型意味着预后不好,有些极早期含微乳头成分的病人就表现得很恐慌,那该怎么办?要不要化疗?要不要靶向治疗?该怎么预防?

按照最新版2021肺癌NCCN治疗指南,I期肺癌病人,无论IA期还是IB期,无论是不是微乳头型,都不推荐术后化疗。但也有专家认为,IB期年轻病人,如果有微乳头成分及其他高危因素,根据意愿可以进行4次术后化疗。而2021年NCCN指南也首次把三代靶向药奥希替尼作为IB-IIIB期患者术后辅助治疗推荐。所以,IB期含微乳头型腺癌也可以考虑靶向治疗,或者化疗后靶向维持治疗。
至于IA期的含微乳头成分的病人,由于完整切除后治愈率很高,术后不建议做任何治疗,也不需要使用任何药物预防复发转移,最重要的是术后的定期复查,摈弃不良生活习惯,增强体质,均衡营养,保持乐观心态。
原发性肺癌(以下简称肺癌)是我国最常见的恶性肿瘤之一。国家癌症中心2015年发布的数据显示,2006年-2011年我国肺癌5年患病率是130.2(1/10万)。其中男性84.6(1/10万),居恶性肿瘤第2位。女性45.6(1/10万),居恶性肿瘤第4位。
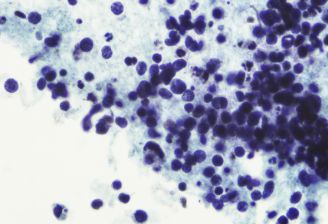
小细胞肺癌(small cell lung cancer, SCLC)是 一种起源于支气管黏膜上皮的Kulchitsky细胞的异源性神经内分泌肿瘤,是肺癌中侵袭性最强的亚型,约占肺癌的15%-20%[2、3],98%的SCLC归因于吸烟,其特点是恶性程度高、侵袭性很高、病情进展快、早期出现远处转移等。
上个世纪70年代CAV方案常用于治疗SCLC,而到了80年代,逐渐被EP方案所取代。一项比较EP方案与CEV(环磷酰胺+表柔比星+长春新碱)的Ⅲ期临床研究共纳入了436名局限期和广泛期的SCLC患者,结果显示IP明显延长了患者的OS(14.5个vs9.7个月,P=0.001),且其毒性更小。基于众多研究结果EP方案成为最常用的SCLC一线化疗方案。
广泛期SCLC应采用化疗为主的综合治疗。一线治疗推荐EP方案(依托泊苷联合顺铂)、EC方案(依托泊苷联合卡铂)、IP方案(伊立替康联合顺铂)、IC方案(伊立替康联合卡铂)。
2002年 JCOG9511的临床试验结果中发现 IP 方案(CPT-11联合 DDP)一线治疗广泛期 SCLC 有效率显著高于当时标准 EP 方案(12.8 个月比9.4个月, P = 0.002)。而在北美开展的两项Ⅲ期临床研究在比较 IP 方案与 EP 方案一线治疗 ES-SCLC 上的总生存期、疾病进展生存时间和有效率方面差异无显著性。造成结果不同的原因可能是试验给药剂量与时间上有差异,或者是人种之间的基因差异导致药物代谢不同。
如果化疗有效者,且远处转移病灶控制,一般情况尚好者可行胸部病变放疗。CREST研究显示全身化疗后达缓解的广泛期SCLC患者,给与胸部放疗联合预防性脑放疗,可降低50%胸部复方风险,提高2年总体生存率(13%vs3%)。化疗有效患者可考虑行预防性全脑照射(prophylactic cranial irradiation, PCI)。
IMpower 133 研究:III期、随机双盲、 安慰剂对照、 多中心的国际研究。
研究组:卡铂:AUC 5 mg/mL/min IV,d1 依托泊苷:100 mg/m2 IV, d1–3 阿特珠单抗 1200 mg IV d1,4周期后给与阿特珠单抗维持治疗,n=201 OS 12.3m PFS 5.2m
对照组给予卡铂:AUC 5 mg/mL/min IV,d1 依托泊苷:100 mg/m2 IV, d1–3 加安慰剂,4周期后给与安慰剂。1n=202 OS 10.3m PFS 4.3m
原发性肺癌(以下简称肺癌)是我国最常见的恶性肿瘤之一。国家癌症中心2015年发布的数据显示,2006年-2011年我国肺癌5年患病率是130.2(1/10万)。其中男性84.6(1/10万),居恶性肿瘤第2位。女性45.6(1/10万),居恶性肿瘤第4位。
小细胞肺癌(small cell lung cancer, SCLC)是 一种起源于支气管黏膜上皮的Kulchitsky细胞的异源性神经内分泌肿瘤,是 肺 癌中侵袭性最强的亚型,约占肺癌的15%-20%[2、3],98%的SCLC归因于吸烟,其特点是恶性程度高、侵袭性很高、病情进展快、早期出现远处转移等。
上个世纪70年代CAV方案常用于治疗SCLC,而到了80年代,逐渐被EP方案所取代。一项比较EP方案与CEV(环磷酰胺+表柔比星+长春新碱)的Ⅲ期临床研究共纳入了436名局限期和广泛期的SCLC患者,结果显示IP明显延长了患者的OS(14.5个vs9.7个月,P=0.001),且其毒性更小。基于众多研究结果EP方案成为最常用的SCLC一线化疗方案。
广泛期SCLC应采用化疗为主的综合治疗。一线治疗推荐EP方案(依托泊苷联合顺铂)、EC方案(依托泊苷联合卡铂)、IP方案(伊立替康联合顺铂)、IC方案(伊立替康联合卡铂)。
2002年 JCOG9511的临床试验结果中发现 IP 方案(CPT-11联合 DDP)一线治疗广泛期 SCLC 有效率显著高于当时标准 EP 方案(12.8 个月比9.4个月, P = 0.002)。而在北美开展的两项Ⅲ期临床研究在比较 IP 方案与 EP 方案一线治疗 ES-SCLC 上的总生存期、疾病进展生存时间和有效率方面差异无显著性。造成结果不同的原因可能是试验给药剂量与时间上有差异,或者是人种之间的基因差异导致药物代谢不同。
如果化疗有效者,且远处转移病灶控制,一般情况尚好者可行胸部病变放疗。CREST研究显示全身化疗后达缓解的广泛期SCLC患者,给与胸部放疗联合预防性脑放疗,可降低死亡率。
当地时间11月13日,美国食品药品监督管理局(FDA)加速批准了基因疗法KEBILIDI用于治疗AADC缺陷。这是美国有史以来第一个批准直接作用于大脑的基因疗法。AADC缺乏症是一种罕见的遗传疾病,这个病挺严重,还会缩短患者寿命。近年来,大家关注到我们大脑中含有多巴胺,多巴胺是一种对运动功能极其重要的物质,这种病会导致我们脑中无法合成多巴胺。
这种疗法是一种基因替代疗法,是通过外科手术的方式直接把药物注射到大脑。临床试验结果显示,在进行基因治疗后的12个月内,患者运动和认知功能就有了快速改善,并且这种改善效果的持续时间可以达到5年。
正电子发射断层扫描和神经递质分析也证实了患者体内多巴胺的产生增加。改善源头后,患者的各种症状(比如情绪、出汗、体温和眼动危象等方面)得到改善,患者的生活质量也提高了。回到这个神奇的基因疗法,KEBILIDI是一种基于重组腺相关病毒血清型2(rAAV2)的基因疗法,里面包含了人的功能基因。
注入大脑后,这种功能基因可以增加AADC酶的含量,从而恢复多巴胺的产生,以此来纠正潜在的遗传缺陷。但还需要注意的是,KEBILIDI禁用于通过神经影像学评估还没有达到颅骨成熟度的患者。
参考来源:
1.PTC Therapeutics Announces FDA Approval of AADC Deficiency Gene Therapy.
2.Tai CH, Lee NC, Chien YH, Byrne BJ, Muramatsu SI, Tseng SH, Hwu WL. Long-term efficacy and safety of eladocagene exuparvovec in patients with AADC deficiency. Mol Ther. 2022 Feb 2;30(2):509-518. doi: 10.1016/j.ymthe.2021.11.005. Epub 2021 Nov 8. PMID: 34763085; PMCID: PMC8822132.
当地时间11月13日,两款心电图相关的设备被美国食品药品监督管理局(FDA)批准,一款是可佩戴的贴片,可连续14天来监测我们的心电图,当发生心律失常的时便于直接通知医生。
另一款是心电图监护仪,也能直接佩戴在胸部,能及时识别心律失常的具体类型[1-2]。这两款设备有助于心血管疾病的早期筛查。
未来心电图监护仪还将引入人工智能算法,分析心电图以更早诊断不同类型的心脏病。这台心电图监护仪还可以生成24小时连续心电图,可以在锻炼的时候使用,还能检测心率等数据。而可佩戴的贴片由有7个心电图导联,在检测心律失常方面准确性高。
1.什么是心律失常?
心律失常是常见的心血管疾病,其中室性心律失常最为常见,包括室性早搏(室早)、室性心动过速(室速)、心室扑动(室扑)和心室颤动。有时室性心律失常的发生毫无征兆,这两个设备的获批有助于更早发现;有时会出现心悸或黑矇,甚至发生心脏性猝死。
据相关数据显示,我国大陆的年猝死人数可达54.4万[3]。且在全球范围内,心血管疾病盯上了年轻人,是导致过早死亡的主要原因之一。因此我们每个人都需要关注心律失常等疾病,保护好你的“小心脏”。
2.心律失常检查包括哪些?

近期,徐汇区市场监管局联合10家医疗机构在细胞和基因治疗药品创新与临床发展会上联合发布《医疗机构使用细胞治疗药品质量管理指南》,为CAR-T创新药品的使用提供了规范化的指导。

该《指南》首次提出“将CAR-T药品使用质量管理纳入统一的医疗机构药品管理体系,指导医疗机构组建多学科诊疗团队,由临床使用细胞治疗药品的科室负责人作为细胞治疗团队负责人 对细胞治疗项目的各环节进行监督,院内其他部门明确职责,协同配合参与,从而保障患者使用药品的质量安全和可追溯 。”
关于细胞治疗,你也许有很多问题,我们整理了5个常见问题,一起了解。
1.什么是CAR-T药品?
CAR-T药品也称细胞疗法,是一种用自身免疫系统细胞的癌症治疗方法。可以从我们自身或者其他人的外周血中收集T细胞,然后在体外进行改造以表达嵌合抗原受体(CAR)。改造后,经过体外扩增,再回输回体内,这些这些CAR-T细胞特异性识别靶抗原并迅速增殖以在体内发挥抗肿瘤作用。
CAR-T疗法会影响我们的免疫系统,可能出出现不良反应。如细胞因子释放综合征(CRS)。当CAR-T细胞开始攻击癌细胞并触发体内的免疫反应时,就会发生这种情况。对于某些患者来说,CRS可能感觉像是流感症状,也可能会像低血压,也可能出现高烧和呼吸困难等。
2.FDA批准了哪些CAR-T药?
目前FDA批准的CAR-T药包括以下7种,大多应用于骨髓瘤、淋巴瘤和白血病。

3.得了癌症再取免疫细胞来得及吗?
很多癌症一发现就是晚期,癌细胞会干扰我们身体自然产生的免疫细胞。因此,许多癌症患者无法获得足够的健康T细胞进行治疗。且随着年龄增长,我们体内免疫细胞的数量和活性都会降低。

为了应对未来这种情况,可以更早地储存健康的免疫细胞,储存免疫细胞的过程类似于抽血,先会抽150-200ml的血,然后送到细胞库去处理从而分离出包含免疫细胞的外周血单核细胞。分离完成后,再将细胞放在液氮瓶中长期储存,可以保存较长时间直到需要使用,且免疫细胞活力不会发生变化。
4.冻存免疫细胞可以冻存多久?
理论上,可以一直冻存。细胞达到冻存温度(如-196°C),细胞的新陈代谢就会失去活性,当细胞解冻时,再次恢复活性。
5.冻存后的免疫细胞有什么用?我的家人能用我冻存的免疫细胞?
可以恢复免疫力,以及用于前文提到的CAR-T细胞疗法。
但家人并不能使用你冻存的免疫细胞,这是因为不同个体之间会出现移植物排斥反应,因此每个人冻存的免疫细胞最好只用于自己。
参考来源:
1.上海徐汇发布《医疗机构使用细胞治疗药品质量管理指南》.
2.Zhang X, Zhu L, Zhang H, Chen S, Xiao Y. CAR-T Cell Therapy in Hematological Malignancies: Current Opportunities and Challenges. Front Immunol. 2022 Jun 10;13:927153. doi: 10.3389/fimmu.2022.927153. PMID: 35757715; PMCID: PMC9226391.
3.What Is CAR T-Cell Therapy?
4.FDA approves CAR-T cell therapy to treat adults with certain types of large B-cell lymphoma.
5.FDA approves obecabtagene autoleucel for adults with relapsed or refractory B-cell precursor acute lymphoblastic leukemia.
6.FDA approves tisagenlecleucel for relapsed or refractory follicular lymphoma.
7.FDA approves ciltacabtagene autoleucel for relapsed or refractory multiple myeloma.
8.FDA approves lisocabtagene maraleucel for relapsed or refractory large B-cell lymphoma.
9.FDA approves idecabtagene vicleucel for multiple myeloma.
10.FDA approves brexucabtagene autoleucel for relapsed or refractory mantle cell lymphoma.
展开更多
























