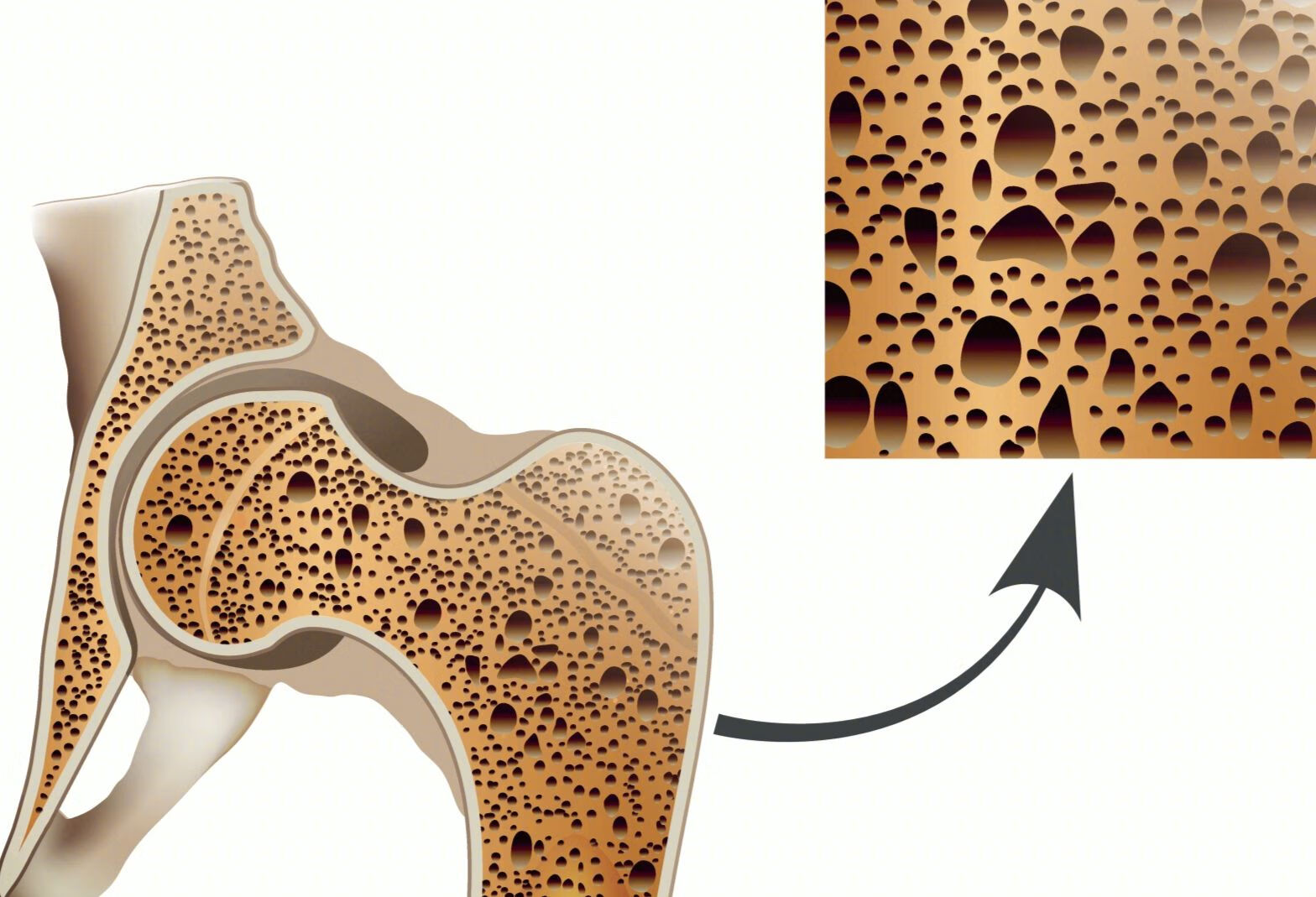
糖尿病是一种代谢性疾病。据统计,约有1/2至2/3的糖尿病患者存在骨密度减低,其中约1/3被诊断为骨质疏松症。骨质疏松症的最大危害是骨折。
一、糖尿病性骨质疏松症的发病原因
糖尿病患者比健康人更易发生骨质疏松症,主要原因包括以下几点:
钙质流失:糖尿病患者不仅通过尿液排出大量葡萄糖,还伴随钙、磷等矿物质的流失。若不注意补钙,就可能导致缺钙。低血钙会引发继发性甲状旁腺功能亢进,导致甲状旁腺素分泌增加,进而促进破骨细胞活跃,造成骨质脱钙和骨质疏松。
胰岛素缺乏影响成骨细胞功能:成骨细胞上有胰岛素受体,胰岛素可调节其功能。糖尿病患者体内胰岛素绝对或相对缺乏,导致成骨细胞活性下降,同时影响骨胶原蛋白的合成,骨基质减少,从而加剧骨质疏松。
肾功能受损:糖尿病患者肾功能受损时,1a-羟化酶的活性降低,导致活性维生素D合成减少,从而影响肠道对钙的吸收。
性激素缺乏:糖尿病患者常并发性腺功能减退,缺乏性激素会进一步加重骨质疏松。
微血管及神经病变:这些病变会影响骨骼的营养供给,导致骨骼营养不良和骨质疏松。
二、糖尿病性骨质疏松症的临床表现
骨质疏松症是一种全身性骨骼疾病,其特征是骨量减少、骨组织结构破坏,导致骨脆性增加,容易发生骨折。糖尿病性骨质疏松症兼具糖尿病与骨质疏松症的症状特点:
早期通常无明显症状,随着病情进展,患者可逐渐出现腰背和髋部疼痛、小腿抽筋、驼背、身高缩短等症状。严重者稍遇外力(如咳嗽、打喷嚏、弯腰等)即可骨折,且愈合缓慢。糖尿病患者的骨折多发生在腰椎、髋部和腕部。
三、糖尿病性骨质疏松症的防治
防治糖尿病性骨质疏松症需从以下三个方面入手:
积极治疗糖尿病:有效控制糖尿病是防治骨质疏松症的关键。单纯针对骨质疏松的治疗若未同时控制糖代谢,是不充分的。由于胰岛素对骨代谢有重要作用,因此糖尿病性骨质疏松症患者应优先考虑使用胰岛素治疗。
保持健康的生活方式:
- 纠正不良习惯:吸烟、酗酒、大量饮用咖啡或浓茶等行为会加速钙的流失,增加骨质疏松风险。糖尿病患者应戒除这些习惯。
- 合理饮食:既要控制血糖,又要保证钙、磷、镁等矿物质的摄入。一般来说,糖尿病患者每日钙摄入量不应低于1000毫克。每天饮用1~2袋牛奶,同时增加户外活动,必要时补充维生素D以促进钙吸收。
- 积极运动:如慢跑、步行、爬楼梯、太极拳等,有助于增强骨骼强度,提高骨密度,预防骨质疏松。
合理用药治疗:
- 钙剂:每日补充500~1000毫克元素钙,如钙尔奇D、乐力钙等。
- 维生素D:促进钙吸收。
- 雌激素:主要用于绝经后妇女,但对糖尿病患者应谨慎使用,以避免对血糖、血压的不良影响。可选用降钙素替代。
- 降钙素:有助于增加骨密度,降低骨折风险,同时具镇痛效果。
- 二膦酸盐:可抑制骨吸收、增加骨密度,需空腹服用,不能与钙剂同服。

生活中,糖尿病,高血压,痛风已经是常见的慢性疾病,相较于癌症等致命疾病,他们的病程缓慢,疼痛感相对较低,那为什么还要长期吃药控制呢?因为血糖,血压,包括尿酸值如果长时间超出正常值,就会引发机体的代谢问题,产生并发症,而且是牵一发而动全身相互影响,滚雪球一样,波及面越来越大。
引发“雪崩”
举个例子,血糖引起代谢紊乱,正常的“毒素”都排不出去,血压,尿酸都升高,最终累及各器官产生病变。
代谢性疾病主要包括三大类:糖尿病、高血压、痛风。
代谢性疾病可能会损害机体对代谢和炎症的调节,包括血糖和脂质稳态,以及脂肪组织和血管炎症等,这会导致骨骼重塑受损,滑膜和关节内脂肪炎症增加,软骨合成代谢活动受到抑制,分解代谢加快,从而增加患骨关节炎等骨科疾病的风险。
糖尿病并发症
糖尿病一项来自糖尿病和骨关节炎患者数据的分析显示,两者之间有很强的正相关性,有糖尿病的患者患骨关节炎的风险比没有糖尿病的高 40%。
糖尿病可以通过氧化应激、慢性高血糖和胰岛素抵抗所致的轻度慢性炎症两条主要途径对骨关节炎产生致病作用。糖尿病的存在与骨关节炎的进展、严重的临床症状和关节结构改变有关,而控制血糖可以延缓骨关节炎的进展。
另外,不仅是患病,对于治疗,糖尿病也会有影响。研究表明糖尿病对人工关节置换有负面影响,包括术后膝关节功能的恢复、伤口愈合及关节翻修或感染的概率增加等。
糖尿病足导致残(截肢)
糖尿病足是糖尿病患者因不同程度的下肢血管病变和局部神经异常所致的踝关节以远的皮肤感染、溃疡和/或深层组织破坏。其流行病学呈现高发病率、高致残率、高死亡率、高花费的特点。
中国最近的研究显示,45%的糖尿病足为 Wagner3 级以上;总截肢率介于 18-28%。糖尿病足的死亡率比大多数癌症还高,其死亡率最高达 11%。
糖尿病患者由于长期血液中的糖分过高侵蚀全身的血管,而足部离心脏最远,血管病变最早就会在足部爆发导致足部缺血,甚至发生长期溃炼的一种疾病,它是糖尿病全身血管病变的局部表现。
糖尿病足若治疗不及时,往往会发展为严重的感染或大面积坏疽。这时,坏死组织可产生大量毒素,威胁人的生命。截肢是没有办法的办法,常用的方法有小范围截肢(如截除单个脚趾)和大范围截肢(如踝以上小腿截肢)。目的在于把坏死或感染的组织彻底清除,可以起到防止感染扩散、挽救生命的作用。
高血压
高血压患者通常会出现动脉粥样硬化病理改变,而动脉粥样硬化的存在与骨关节炎风险的增加相关,这可能是由于动脉粥样硬化的改变,使软骨下骨的异常灌注,导致关节软骨缺少营养供应有关。
高血压患者体内脂质代谢紊乱,如血脂异常和较高水平的低密度脂蛋白胆固醇,而氧化型低密度脂蛋白有助于动脉粥样硬化,也与骨关节炎风险增加有关。
痛风
痛风是一种常见且复杂的代谢性疾病,各个年龄段均可能罹患此病,它通常由高尿酸血症导致,同时高尿酸也可以导致多种疾病的发生。
痛风性关节炎是最常见的炎性关节炎之一,临床表现出关节受累的特征性模式,尤其是第一跖趾关节有明显的受累倾向。它往往也会影响肢体远端的外周关节,如踝关节、膝关节、指间关节、腕关节和肘关节等,而髋关节、肩关节和脊柱等轴向关节则较少受到影响。
尿酸盐结晶沉积在关节,引发局部红肿疼痛;结晶堆积越来越多,形成结节乃至痛风石,侵蚀关节骨骼,引发疼痛,炎症,红肿发热;严重者会造成骨缺损,进一步导致关节力线改变等,影响行走站立,影响生活功能。
那么已经患有代谢疾病的朋友,怎么减缓骨科疾病的侵袭呢?要注意以下几点:
- 监测血糖,血压,按时规律吃药,不要自己停药或随便调整药量,只会引发更坏的影响。
- 如果有肥胖的情况,特别是腹部肥胖的苹果型身材,适当减重。少吃甜食,油炸,淀粉(米饭,馒头,面条一顿干 3 碗是不行的;长期拿主食顶饱,也是不对滴!)饭后或清晨进行适度的运动,从慢走开始,逐步增量。
- 少油,少盐,都对血压有益。
- 锻炼:是改善代谢的王律,毕竟自身代谢不下去,就得加大消耗,代谢出去。同时加强膝关节周围肌肉的锻炼,增加关节稳定性,保护关节,减缓退变磨损。
- 痛风的朋友,戒酒,少吃海鲜,规律吃药。
- 补充氨糖,营养软骨(糖尿病也能吃氨糖,此糖非彼糖,不是一回事)
病症: 胃癌 恶性黑色素瘤
患者:李女士
年龄:70岁
病症: 胃癌 恶性黑色素瘤
患者:李女士
年龄:70岁
罹患癌症,毫无疑问对每个人都是重大打击。而如果一位患者不幸同时罹患两种癌症,我们可以想象得出他的心情会是怎样的沉重。
但时至今日,癌症早已不再是什么“不治之症”,很多良好的治疗方法,可帮助患者迈过重重困境,预后得到极大提升。
不仅如此,在医疗全球化的今天,中国患者也能通过“海外二诊”服务,快速触达到国际权威专家资源,为自己的治疗保驾护航!
今天的案例主人公李女士,正是一位“海外二诊”的受益者。我们来一起看看她的故事。*为保护隐私,文中患者个人信息均已经脱敏处理。
70岁的李女士在去年年底,因脚底疼痛去医院看病,结果发现脚后跟有一个1厘米的黑色肿物。医生判断是冻疮,于是开了点外用药,李女士也就没有再放在心上。
大概4个月后,真正的噩梦降临:李女士通过影像检查,被诊断为胃癌,而且有了淋巴结转移。 她还出现了多次呕血,病情非常危急。很快,医生为她实施了全胃切除。令人意想不到的是,几天后通过检查,医生发现李女士后脚跟的肿物竟然也是癌症——恶性黑色素瘤。于是大概2个月后,医生又切除了她的足底肿瘤。
为了降低复发风险,李女士开始了3个周期的化疗联合免疫治疗(替吉奥联合纳武单抗)。
虽然该做的都已做完,但对于李女士来说,恐惧感还远未被消除。因为癌症最令人恐惧的,是其具有“复发转移”的能力 。一旦癌症再次袭来,李女士不知道自己该如何应对。另外,两种癌症的治疗以及术后辅助药物治疗,也让李女士遭遇了一些副作用。比如腹泻、味觉障碍还有体重明显下降的问题。这些对于已经70岁的李女士来说,都很影响生活质量,所以迫切需要解决。
在本次的国际专家“海外二诊”服务中,李女士预约的是来自日本某知名综合性医院肿瘤中心的外科部长医生,他的专长领域既包括肿瘤外科,又包括各类癌症药物疗法、姑息治疗,是一位“内外兼修”的权威专家。在充分了解了李女士既往的病情和治疗经过后,医生很快通过远程会诊的方式,为患者详细解答了当前她的所有问题。
1、 未来如果转移或复发了该怎么办?
医生:假如您未来不幸出现转移或复发,那么化疗是核心治疗手段。对于单发的孤立转移灶,可以选择手术、放疗来进行局部治疗。
具体化疗方案选择,我按使用的先后顺序列出了3类,当前面的方案失效后,可更换为后面的方案。
一类方案:化疗联合/不联合免疫方案
- CAPOX (卡培他滨+奥沙利铂)±O药(即免疫药物纳武单抗)
- SOX (替吉奥+奥沙利铂)±O药
- FOLFOX (5-FU+奥沙利铂)±O药
二类方案:化疗联合/不联合抗血管药物方案
- Taxane (紫杉醇/白蛋白结合型紫杉醇/多西紫杉醇)±雷莫芦单抗
三类方案:化疗方案
- 曲氟尿苷/盐酸替吡嘧啶
- 伊立替康
2、N K细胞疗法是否对我有帮助?副作用是否可控? X医生:目前尚没有证据表明NK细胞疗法对癌症有效,因此不予推荐。
3、口服替吉奥会腹泻,是否需要调整方案? II/III期胃癌患者术后采用辅助治疗方案,分别为:
- 替吉奥口服 1 年(口服 4 周,停药 2 周,共 8 个疗程或口服 2 周,停药 1 周,共 16个疗程)
- CAPOX (卡培他滨+奥沙利铂) 共半年(每 3 周一次,共 8 个疗程)
- SOX (替吉奥+奥沙利铂) 共半年(每 3 周一次,共 8 个疗程)
这三种方案中,替吉奥方案和CAPOX方案等效,但SOX要优于替吉奥。另外,胃癌术后直接使用纳武单抗免疫治疗无意义。
替吉奥确实会出现腹泻等代表性不良反应,患者可以考虑对症治疗,比如调节肠道的药物、止泻药等缓解副作用。如果副作用太严重,那么可以考虑减少药物剂量。
替吉奥的标准用药剂量为120mg,但用量低于80mg无法达到预期效果。如果当前患者用药为100mg,那么为了降低副作用,可以减少剂量到80mg;但如果目前剂量已经是80mg,则无法进一步降低剂量,此时考虑更换方案为CAPOX方案替代。 如果不良反应严重到干扰日常生活,则患者可以选择停药,持续观察病情变化。
对于无淋巴结转移的II期B和II其C的患者,可选择使用1年帕博丽珠单抗免疫治疗。
4 、术后患者很瘦,味觉障碍,如何调理改善? 通常,手术后患者体重会减轻20%左右。这是患者消化吸收能力低下、促食欲的胃肠激素减少引起的。大约6个月到1年时间,患者可以恢复正常。
味觉障碍可能是抗癌药的副作用引起的,也可能是饮食减少导致缺乏锌等微量元素引起的。建议患者采用少食多餐的方式饮食,每天分5-6次吃饭。在日本,我们有时也会给患者用一些营养补充剂。
另外,也可以考虑采用中草药的对症治疗,改善症状,比如十全大补汤、六君子汤。 会诊结束后,李女士的心情得到了极大的平复。她对自己未来要走的路更清晰了,也对日本专家的细致指导和会诊的快速响应非常满意。
中国是消化道癌症发病数量较多的国家,根据国家癌症中心发布的《2022年中国恶性肿瘤疾病负担情况》数据,2022年我国胃癌新发病例约为35.87万例,死亡人数26.04万人。
总体来说,胃癌属于严重威胁我国国民生命健康的蕞常见癌症之一。胃癌如能在早、中期发现,还是有很大机会通过手术实现根治的,患者仍有一定机会得到临床治愈(术后5年不复发即为临床治愈)。
但在胃癌患者中,一部分人会因为【年龄较高】、伴有诸多【基础病】等问题,对手术存有疑虑,担心“下不来手术台”,甚至会放弃手术机会,选择吃药等姑息治疗。这样的选择真的正确吗?现如今的技术能否支持这类老年患者安全手术呢?接下来,我们一起看一个真实案例。
01七旬老人遭遇中期胃癌
一位七十多岁的“老胃病”项女士,因短时间体重骤降(8斤)前往就医。血液检测显示,她有一项指标异常升高。进一步检查发现,她的食道和胃连接的地方(贲门)以及胃的“外墙”(胃壁)都变得异常的厚,而且形状不均匀——这正是胃癌常见的表现。
医生随后通过胃镜检查和病例活检(取一小块组织观察上面的细胞),确诊了老人患有胃癌。由于还没有出现胃以外的远处其他器官的转移,也没有附近淋巴结转移,因此项女士的胃癌分期为中期。虽不是早期,但中期胃癌通常是可以手术的。为项女士提供诊疗的医生也表示,可以通过全胃切除手术实现根治。
但一来项女士已经七十多岁,二来她有20多年的糖尿病(手术伤口会更慢愈合、感染风险高、术后并发症风险高)、右肺还有一枚1.2厘米的肺结节。种种问题让老人和家人们都比较犹豫,担心扛不住治疗,最终“越治越糟”。在这样的背景下,项女士决定找一位足够权威的外科专家,来为自己进行全面评估,看看能不能兼顾好肿瘤根治以及手术的安全性。
不久后,项女士预约了来自日本癌研有明医院消化中心胃外科部长布部创也医生为自己提供指导。
02日本专家咨询内容分享
在充分了解了项女士的病情信息和全部资料后,布部创也医生给出了如下指导建议:首先,患者此前接受的是普通CT而非增强CT,胃镜也没有清晰展示食道上肿瘤具体侵犯的程度,因此很难得出精准的分期判断。
后面患者来癌研有明医院就医时,医疗团队会在治疗前为她做一套非常精细、全面的检查,此后就可以明确肿瘤情况了。届时如果发现患者的分期、肿瘤侵犯的范围确实和现在的结果相同,那么可以通过一个腹腔镜微创手术实现根治,损伤会非常小;如果届时发现肿瘤侵犯食道过多,则需要消化道联合食道外科共同进行胸腔镜手术治疗。
但无论是哪一种情况,患者都可以耐受手术,并且保留一部分胃。癌研有明医院是一家极为擅长肿瘤微创手术的知名癌症专科医院。在胃癌方面,2005年,医院开始导入腹腔镜,2019年又引入了达芬奇手术机器人,患者术后并发症更少了。如今,癌研有明医院98%的外科手术都采用微创。
受益于此,很多在别的医院需要胃全切的胃癌患者,到癌研有明后可以保留一部分胃,还能兼顾临床治愈。这对于术后患者的长期营养摄入和体重维持都很有帮助。布部创也医生所在科室的主要目标之一,正是在做到根治性切除的前提之下,将原本的胃全切术式变为次全胃切除术,尽可能为患者保留一些胃,让他们未来的生活质量得到提升。
那么项女士的糖尿病问题,会不会影响到手术呢?对此,布部创也医生认为完全不必担心,因为对于这类患者,癌研有明医院会进行详细的术前评估,并且有专业团队介入,从生活方式调整和专业治疗入手,帮助患者控制好血糖,让血糖水平达到符合手术的标准,从而降低术后愈合不良风险。
关于肺部的1.2厘米结节,布部医生认为可以暂不处理,无论它到底是良性还是恶性。因为这枚结节属于纯磨玻璃结节,即便是恶性,进展也非常缓慢,并不会快速出现转移扩散。而胃癌根治手术虽然会采用微创方式,但依然会给患者带来一定的负担,如果同时处理肺结节,会导致负担过重、患者难以承受。所以当前蕞好的处理办法,是先集中精力解决胃癌肿瘤,术后安排呼吸科专家为患者进行肺结节诊断,给出随访或手术或根治性放疗的建议。
03项女士术后,是否需要化疗来降低复发风险、争取更大治愈希望?
对此,布部创也医生表示,是否化疗现在还不能判断。因为术后患者能获得蕞精准的分期判断,有可能患者术前被认为是2期,但实际上术后成了1期(无需化疗);有时也可能患者术前是1期,但术后成了2-3期。假如是2-3期,则患者术后需要坚持1年的辅助化疗,大概可以降低10%的复发风险。
当地时间10月29日礼来宣布了Ⅲb期临床试验(TRAILBLAZER-ALZ 6)的积极结果,对于早期症状性阿尔茨海默病成人患者,用改良滴定方案接受donanemab治疗的患者在24周主要终点时,伴水肿/积液的淀粉样蛋白相关影像学异常(ARIA-E)有所减少。
donanemab这个新药在今年7月获批于美国,又在之后获日本厚生劳动省、英国药品和医疗产品监管局批准,用于轻度阿尔茨海默病、轻度认知功能障碍的治疗。donanemab在国内2023年取得突破性治疗药物认定,并纳入优先审评审批程序,目前还在审评审批过程中。
 CDE官网截图
CDE官网截图
但在FDA说明书中有黑框警告,大意是应用该药时应注意淀粉样蛋白相关影像学异常(ARIA),表现为ARIA-E和ARIA伴含铁血黄素沉积(ARIA-H),通常发生在治疗早期,且无症状,很少发生严重和危及生命的事件。本次试验的积极结果和这个黑框警告相关。一起来看详情。

FDA说明书截图
给药方式有哪些改变?会不会影响效果?
TRAILBLAZER-ALZ 6是一项多中心随机双盲Ⅲb期研究,主要研究donanemab的不同给药方案对早期症状性AD患者ARIA-E和淀粉样蛋白清除率的影响,这里的早期AD指的是轻度认知障碍(MCI)和轻度痴呆疾病阶段。

给药方式和既往不同,既往标准给药方案是在前三次输注时接受2瓶(700mg)donanemab,然后再接受4瓶(1400mg);改良滴定方式是患者第一次输注1瓶(350mg),第二次输注2瓶(700mg),第三次输注3瓶(1050mg),此后每次输注4瓶(1400mg)。
研究的主要终点是第24周时患者出现ARIA-E占总参与者的比例,结果显示接受改良滴定方式的患者ARIA-E发生率为14%,而标准给药方案为24%,相对风险降低41%。载脂蛋白E(APOE)是已知的阿尔茨海默病遗传风险因素的携带者,在这些患者中,19%患者在改良滴定时患有ARIA-E,而标准给药方案中为57%,相对风险降低67%。
看到这里你或许也有疑问,虽然ARIA-E的发生风险降低了,但改良滴定方案会不会影响疗效?答案是不会。
与接受标准给药方案的患者相比,改良滴定患者淀粉样斑块和p-tau217减少。改良滴定的患者的淀粉样斑块水平较基线平均降低 67%,而标准给药组患者为69%。
参考来源
1.Modified Titration of Donanemab Demonstrated Reduction of ARIA-E in Early Symptomatic Alzheimer's Disease Patients in Phase Ⅲb study.
2.CED官网.
3.A Study of Different Donanemab (LY3002813) Dosing Regimens in Adults With Early Alzheimer's Disease (TRAILBLAZER-ALZ 6).
当地时间10月29日,阿西米尼(asciminib)获美国食品药品管理局(FDA)加速批准[1] ,用于慢性期新诊断的费城染色体阳性慢性粒细胞白血病(Ph+CML)成年患者。CML是一种骨髓和血细胞癌症,通常由费城染色体的异常染色体引起。在一线治疗中,约1/3的患者会出现下列问题:由于不良反应或者治疗无效而停止酪氨酸激酶抑制剂(TKI)治疗。
为了解决这一问题,需要开发新的药物,asciminib就是解决这一困境的新药。早在2022年8月,加拿大药物和卫生技术局(CADTH)建议[2] :“若满足条件,可通过公共药物计划报销asciminib用于治疗费城染色体阳性慢性粒细胞白血病。”
asciminib为何得到FDA的青睐?
本次获批基于一项III期多中心随机研究,研究目的是比较每日80mg的asciminib与TKI治疗的疗效。TKI治疗是接受伊马替尼、尼洛替尼、达沙替尼或博舒替尼任意一种治疗。
共有405名患者被随机分配(1:1)进两组治疗。主要疗效结局指标是48周时的主要分子反应(MMR)率。这个指标是慢性髓性白血病的关键指标,这个比例越高,说明该治疗在基因水平上对疾病的控制效果越好,能够更有效地抑制疾病相关基因的表达,进而有望更好地控制疾病的进展、改善患者的症状和预后。
研究结果显示,48周时MMR率方面,asciminib组中为68%(95% CI: 61, 74),TKI组为49%(95% CI: 42, 56),二者相差19%。细看具体的TKI,入组伊马替尼和其他TKI药物入组比例为1:1;asciminib组的MMR率为69%(95% CI: 59, 78),而伊马替尼组为40%(95% CI: 31, 50),相差近30%(95% CI: 17, 42)。
这个新药安全吗?每周需要打几次药?
根据FDA数据显示,在新诊断和既往接受过治疗的患者,应用新药最常见的不良反应(≥20%)是肌肉骨骼疼痛、皮疹、疲劳、上呼吸道感染、头痛、腹痛和腹泻。若只看新诊断的患者,最常见的实验室异常(≥40%)是淋巴细胞计数降低、白细胞计数降低、血小板计数降低、中性粒细胞计数降低等。
根据FDA已批准的asciminib说明书,用药期间还需要注意一下事项:
1.骨髓抑制 :用药期间可能因出现骨髓抑制,发生血小板减少症、中性粒细胞减少症和贫血。用药应在治疗的前3个月,需要每两周进行一次全血细胞计数,此后每月进行一次检测,从而判断患者有无骨髓抑制症状。根据严重程度,咨询医生是否需要停药。
2.胰腺毒性 :患者可能出现血清脂肪酶和淀粉酶无症状升高,每月需评估血清脂肪酶和淀粉酶水平,如果您有胰腺炎,则注意主动告知医生,需要进行频率更高的检测。
3.高血压风险 :可能出现3级或4级高血压风险,应注意检测血压。
4.超敏反应 :可能出现3级或4级超敏反应,包括皮疹、水肿和支气管痉挛。如果出现这些症状,需及时反馈医生,医生会根据超敏反应的体征和症状,开始适当的治疗。
5.心血管毒性 :如果您有心血管病史,需要告知医生;对于3级或更高级别的心血管毒性,医生会考虑暂停用药、减少剂量或永久停药。
6.胚胎/胎儿毒性 :若您在怀孕期间用药或在服用药物期间怀孕,可能对孩子有潜在风险。这个新药是口服药,需要根据不同的给药剂量(80mg或40mg)每天/或每两天用药。
近些年来,还有哪些白血病药物获批FDA?
根据FDA肿瘤学/血液系统恶性肿瘤批准通知,白血病相关新药整理如下表。
另外可以看出21年时asciminib已获批白血病治疗,但限定既往接受过两种或更多TKIs治疗,本次获批属于扩大适应证。

参考来源:
1.FDA grants accelerated approval to asciminib for newly diagnosed chronic myeloid leukemia. 2.Asciminib(Scemblix):CADTHReimbursementRecommendation:Indication:ForthetreatmentofadultpatientswithPhiladelphiachromosome-positivechronicmyeloidleukemia(Ph+CML)inchronicphase(CP)previouslytreatedwith2ormoretyrosinekinaseinhibitors.Ottawa(ON):CanadianAgencyforDrugsandTechnologiesinHealth;2022Aug.PMID:38713779. 3.AStudyofOralAsciminibVersusOtherTKIsinAdultPatientsWithNewlyDiagnosedPh+CML-CP. 4.Product information:SCEMBLIX-asciminibtablet,filmcoated.UpdatedAugust7,2024. 5.Oncology(Cancer)/HematologicMalignanciesApprovalNotifications.

以下内容来源于新英格兰医学杂志。
Presentation of Case

Differential Diagnosis
Movement Disorders
Seizures
Functional Movement Disorder
Dyskinesia
Limb-Shaking TIAs
Clinical Impression and Initial Management

Clinical Diagnosis
Dr. Albert Y. Hung’s Diagnosis
Pathological Discussion

Pathological Diagnosis
Additional Management
Final Diagnosis

以下内容来源于新英格兰医学杂志。
Presentation of Case
Dr. Christine M. Parsons (Medicine): A 75-year-old woman was evaluated at this hospital because of arthritis, abdominal pain, edema, malaise, and fever.
Three weeks before the current admission, the patient noticed waxing and waning “throbbing” pain in the right upper abdomen, which she rated at 9 (on a scale of 0 to 10, with 10 indicating the most severe pain) at its maximal intensity. The pain was associated with nausea and fever with a temperature of up to 39.0°C. Pain worsened after food consumption and was relieved with acetaminophen. During the 3 weeks before the current admission, edema developed in both legs; it had started at the ankles and gradually progressed upward to the hips. When the edema began to affect her ambulation, she presented to the emergency department of this hospital.
A review of systems that was obtained from the patient and her family was notable for intermittent fever, abdominal bloating, anorexia, and fatigue that had progressed during the previous 3 weeks. The patient reported new orthopnea and nonproductive cough. Approximately 4 weeks earlier, she had had diarrhea for several days. During the 6 weeks before the current admission, the patient had lost 9 kg unintentionally; she also had had pain in the wrists and hands, 3 days of burning and dryness of the eyes, and diffuse myalgias. She had not had night sweats, dry mouth, jaw claudication, vision changes, urinary symptoms, or oral, nasal, or genital ulcers.
The patient’s medical history was notable for multiple myeloma (for which treatment with thalidomide and melphalan had been initiated 2 years earlier and was stopped approximately 1 year before the current admission); hypothyroidism; chikungunya virus infection (diagnosed 7 years earlier); seropositive erosive rheumatoid arthritis affecting the hands, wrists, elbows, and shoulders (diagnosed 3 years earlier); vitiligo; and osteoarthritis of the right hip, for which she had undergone arthroplasty. Evidence of gastritis was reportedly seen on endoscopy that had been performed 6 months earlier. Medications included daily treatment with levothyroxine and acetaminophen and pipazethate hydrochloride as needed for cough. The patient consumed chamomile and horsetail herbal teas. She had no known allergies to medications, but she had been advised not to take nonsteroidal antiinflammatory drugs after her diagnosis of multiple myeloma.
Approximately 5 months before the current admission, the patient had emigrated from Central America. She lived with her daughter and grandchildren in an urban area of New England. She had previously worked in health care. She had no history of alcohol, tobacco, or other substance use. There was no family history of cancer or autoimmune, renal, gastrointestinal, pulmonary, or cardiac disease.
On examination, the temporal temperature was 37.1°C, the heart rate 106 beats per minute, the blood pressure 152/67 mm Hg, and the oxygen saturation 100% while the patient was breathing ambient air. She had a frail appearance and bitemporal cachexia. The weight was 41 kg and the body-mass index (the weight in kilograms divided by the square of the height in meters) 15.2. Her dentition was poor; most of the teeth were missing, caries were present in the remaining teeth, and the mucous membranes were dry. She had abdominal tenderness on the right side and mild abdominal distention, without organomegaly or guarding. Bilateral axillary lymphadenopathy was palpable. Infrequent inspiratory wheezing was noted.
The patient had swan-neck deformity, boutonnière deformity, ulnar deviation, and distal hyperextensibility of the thumbs (Fig. 1). Subcutaneous nodules were observed on the proximal interphalangeal joints of the second and third fingers of the right hand and on the proximal interphalangeal joint of the fourth finger of the left hand. Synovial thickening of the metacarpophalangeal joints of the second fingers was noted. There was mild swelling and tenderness of the wrists. She had pain with flexion of the shoulders and right hip, and there was subtle swelling of the shoulders and right knee. Pitting edema (3+) and vitiligo were noted on the legs. No sclerodactyly, digital pitting, telangiectasias, appreciable calcinosis, nodules, nail changes (including pitting), or tophi were present. The remainder of the examination was normal.

The blood levels of glucose, alanine aminotransferase, aspartate aminotransferase, bilirubin, globulin, lactate, lipase, magnesium, and phosphorus were normal, as were the prothrombin time and international normalized ratio; other laboratory test results are shown in Table 1. Urinalysis showed 3+ protein and 3+ blood, and microscopic examination of the sediment revealed 5 to 10 red cells per high-power field and granular casts. Urine and blood were obtained for culture. An electrocardiogram met (at a borderline level) the voltage criteria for left ventricular hypertrophy.

Dr. Rene Balza Romero: Computed tomography (CT) of the chest, abdomen, and pelvis, performed after the intravenous administration of contrast material, revealed scattered subcentimeter pulmonary nodules (including clusters in the right middle lobe and patchy and ground-glass opacities in the left upper lobe), trace pleural effusion in the left lung, coronary and valvular calcifications, and trace pericardial effusion, ascites, and anasarca. The scans also showed slight enlargement of the axillary lymph nodes (up to 11 mm in the short axis) bilaterally and a chronic-appearing compression fracture involving the T12 vertebral body.
Dr. Parsons: Morphine and lactated Ringer’s solution were administered intravenously. On the second day in the emergency department (also referred to as hospital day 2), the blood levels of haptoglobin, folate, and vitamin B12 were normal; other laboratory test results are shown in Table 1. A rapid antigen test for malaria was positive. Wright–Giemsa staining of thick and thin peripheral-blood smears was negative for parasites; the smears also showed Döhle bodies and basophilic stippling. Antigliadin antibodies and anti–tissue transglutaminase antibodies were not detected. Tests for hepatitis A IgG and hepatitis C antibodies were positive. Tests for hepatitis B core and surface antibodies were negative. A test for human immunodeficiency virus type 1 (HIV-1) and type 2 (HIV-2) was negative.
Findings on abdominal ultrasound imaging performed on the second day (Fig. 2A and 2B) were notable for a small volume of ascites and kidneys with echogenic parenchyma. Ultrasonography of the legs showed no deep venous thrombosis. An echocardiogram showed normal ventricular size and function, aortic sclerosis with mild aortic insufficiency, moderate tricuspid regurgitation, a right ventricular systolic pressure of 39 mm Hg, and a small circumferential pericardial effusion. Intravenous hydromorphone was administered, and the patient was admitted to the hospital.

On the third day (also referred to as hospital day 3), nucleic acid testing for cytomegalovirus, Epstein–Barr virus, and hepatitis C virus was negative, and a stool antigen test for Helicobacter pylori was negative. An interferon-γ release assay for Mycobacterium tuberculosis was also negative. Oral acetaminophen and ivermectin and intravenous hydromorphone and furosemide were administered.
Dr. Balza Romero: Radiographs of the hands (Fig. 2C through 2F) showed joint-space narrowing of both radiocarpal joints and proximal interphalangeal erosions involving both hands. Radiographs of the shoulders showed arthritis of the glenohumeral joint and alignment suggestive of a tear of the right rotator cuff. A radiograph of the pelvis showed diffuse joint-space narrowing of the left hip, without osteophytosis, and an intact right hip prosthesis.
Dr. Parsons: Diagnostic tests were performed, and management decisions were made.
Differential Diagnosis
Cancer
Infectious Disease
Autoimmune Disease
Hypocomplementemia
Dr. Beth L. Jonas’s Diagnosis
Pathological Discussion
Pathological Diagnosis
Discussion of Management
Follow-up
Final Diagnosis
Overlap syndrome of rheumatoid arthritis and systemic lupus erythematosus complicated by proliferative lupus nephritis, superimposed on amyloid A amyloidosis.
展开更多























