京东健康互联网医院
京东健康互联网医院
 网站导航
网站导航
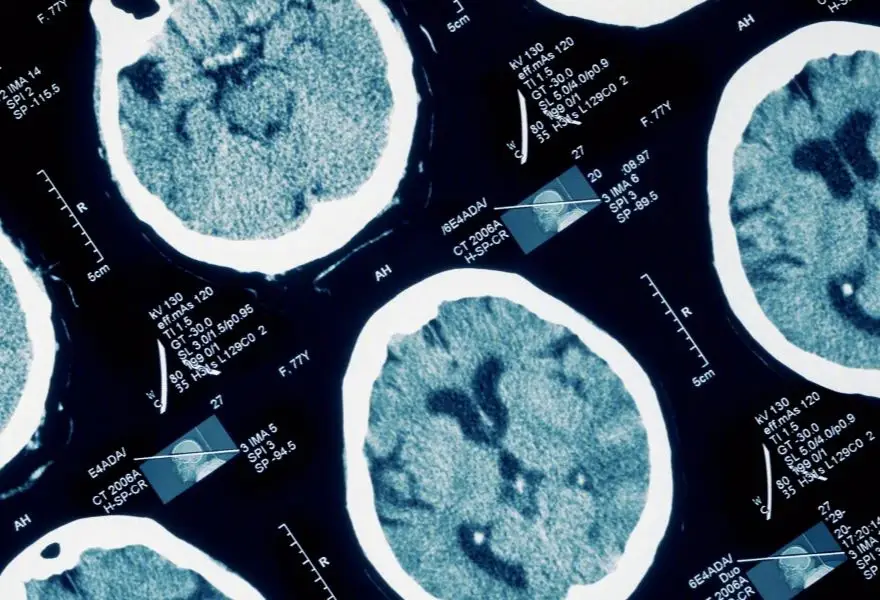
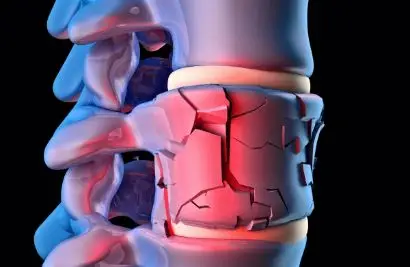
清华大学附属北京清华长庚医院是由清华大学与北京市共建共管的大型综合性公立医院,建设和运营过程中得到了台塑企业和台湾长庚纪念医院的无私捐助和援建。医院坐落于北京市昌平区天通苑地区,总规划床位1500床。于2014年11月28日开业,一期开设1000张床位。2015年11月正式为医保患者服务;2017年6月,实现异地医保直接结算;2019年12月30日,医院二期工程正式奠基,规划新增500张床位;2021年11月25日,医院正式成为北京市基本医疗保险A类定点医疗机构,北京市医保人员无需选择定点即可实时结算。北京清华长庚医院秉承“医疗服务以患者为中心,医院运营以医师为核心,医院发展以员工为重心”的宗旨,创立并践行精准医疗、精诚服务、精益管理的“三精医疗”理念,着力打造现代健康医疗服务体系。医院致力于建构卓越医师培养体系和先端健康科技创新体系,塑造医教研三位一体的国际化学术型医院(Academichospital)。医院开业之初即确立以国际一流医学中心为目标的“三步走”十年发展规划,即2014—2017年,“综合建构,奠定基础”;2018—2020年,“特色发展,塑造品牌”;2021—2025年,“卓越品质,成就一流”。北京清华长庚医院借鉴并在地化台湾长庚纪念医院管理模式,构建现代医院管理体制和运营模式,实行党委领导下的院长负责制,专业化医疗团队与职业化行政团队分工协同治理,提高医院管理的效率和效益。医院以优越的事业平台、舒心的工作环境和体面的薪酬待遇,从海内外引进了一批优秀的专家,组成高水平医疗团队。首任院长董家鸿为国际著名肝胆胰外科和肝脏移植专家,于2017年当选中国工程院院士。医院实行Attending医师负责制、全责护理制和全人照护模式,并全面推行以患者为中心、以疾病为导向的整合式医疗,持续优化医疗流程,为各类病患提供高效、优质、经济的诊疗服务,不断提升疾病治愈率和康复水准。医院已经形成了涵盖内科部、外科部、妇儿部、专科部、急重症部、医技部、全科与健康医学部的7大医疗部和50余个临床医技专科,初步建成综合实力雄厚、专科阵容强大、名医名家汇聚、医院治理良善、医疗品质一流,在业界和社会享有美誉的综合性精品医院;形成了肝胆胰中心、器官移植中心、心血管中心、消化中心、神经中心等优势发展中心,重点建设感染疾病中心、急重症中心、肿瘤中心三大中心,涌现出耳鼻咽喉头颈外科、妇产科、泌尿外科、康复医学科、骨科、内分泌与代谢科、皮肤科、放射诊断科、血管外科、眼科等重点专科。医院开展国内外领先的医疗技术百余项,创下多项世界记录,以先进技术和优质服务成功救治了大批来自海内外的复杂危重病患,并在全国三级公立医院绩效考核中连续获得A+。医院充分借鉴台湾长庚纪念医院和国际顶尖学术型医院的先进医学教育理念和成功经验,创新医学教育模式和方法,业已建立了完善的住院医师-专科医师一体化培训体系,启动了基于器官系统的临床医学MD教育体系建设。医院作为清华大学临床医学博士(MD和PhD)学位授权点,先后开展临床医学全日制专业型硕士生、医工交叉硕士生、卓越医师-科学家八年制、卓越学者型医师(4+4)、临床医学全日制和非全日制专业型博士生等人才培养项目;医院已有国家和北京市认证住院医师、专科医师培训基地15个,是爱丁堡皇家外科学院普通外科医师培训基地,肝胆胰外科成为国际临床专科Fellowship培训中心;神经外科成为华盛顿大学神经外科培训基地;泌尿外科成为世界腔内泌尿外科学会(EndourologySociety)Fellowship培训基地,同时获批欧洲泌尿学会“Setup”泌尿外科内镜手术标准化培训项目。2018年12月,医院获批为首批国家临床教学培训示范中心。2022年9月获批为国家卫健委首批外科基础技能提升培训基地。医院以解决临床问题和满足社会健康需求为引擎,依托清华大学雄厚的综合性学科优势,以医工交叉为突破点建立临床问题驱动的健康科技创新体系,是国家药物临床试验机构、国家医疗器械临床试验机构。2021年获批成为智慧健联体关键技术北京市工程研究中心。2022年9月,清华大学器官移植与仿生医学研究院依托医院成立。借鉴台湾长庚纪念医院经验,北京清华长庚医院建立起完善的社会服务工作体系,设立志愿服务团队,为患者提供暖心服务。设立清华长庚发展基金和社会服务基金,募集社会善款发展临床医学并救助困难患者。响应健康中国行动,医院每年举办近百场健康公益讲座和义诊活动。自2015年始,医院积极参与医疗脱贫攻坚与乡村振兴工作,派员援疆援藏,开展精准医疗帮扶。具有自主知识产权的清华长庚远程医疗系统于2017年9月正式上线,开展线上学术交流和远程会诊业务。作为诞生于国家医疗改革背景下、成长于健康中国战略推展进程中的新型医院,北京清华长庚医院秉持“人本、济世、厚德、至善”的价值观,以“提供健康守护、培养医学精英、创新临床研究、追求卓越管理”为使命,坚持创新(Innovation)、整合(Integration)、国际化(Internationalization)、特色(Identity)的“4I”发展战略,努力建设成为国际一流的医学中心。是头面部遭受较强暴力所造成的牙槽骨结构破坏或连续性中断,主要是由于外部暴力作用所引起,牙槽骨,对症治疗,抗感染治疗,手术治疗,根据损伤史、临床特点和X线摄片检查而明确诊断,避免生冷、辛辣、刺激性、需用力咀嚼的食物,忌烟酒,X线检查,CT检查,MRI检查,口腔检查,。


 172
172

 13
13
 27
27

 54
54
 0
0
 0
0
 0
0

 0
0
 0
0
 0
0