简称:
托克托县医院是托县唯一一所集医疗、教学、康复、保健和预防为一体的县级综合性医院。医院1950年始建,1991年新建。1995年10月晋升为国家二级乙等医院,1996年评为爱婴医院。市级文明单位。2010年1月被中国医院协会评为:全国百姓放心示范医院。现有正式职工281人,聘用临时人员90人。其中卫生技术人员258人(高级职称14人,中级职称58人,初级职称186人)。注册资金1000万元。医院占地面积13958平米,建筑面积21970平米。实际开放病床数400张。医院设有内科、外科、骨科、儿科、妇(产)科、脑外科、中医科、皮肤科、眼科、口腔科、急诊科、手术室、麻醉科、检验科、放射科、心电(B超)、CT室、病理科、儿保科、中(西)药房等临床医技科室21个。配备有东芝16排CT、飞利浦1.5T超导核磁、日立630MA胃肠机、富士CR、美国GE公司vivid7多维星彩超、日本奥林巴斯电子胃镜、结肠镜、腹腔镜、奥林巴斯AU400全自动生化分析仪等现代化医疗服务设施。并设有内科保健病房和妇产科家庭病房等特色服务项目。托县医院先后通过北京军区驻河北保定市252医院、内蒙古自治区医院、内蒙古医学院附属医院、内蒙古武警总队医院、北京协和医院等知名大医院的对口帮扶和大力支持,使医院整体服务水平有了很大提高。2012年,医院门诊就诊人数56058人次,其中急诊1494人,日均门诊量达到226人次。病房共收治住院患者12873人次,全院病床使用率达到68.73%。完成手术2280例。截止2012年11月底,医院业务量达到6100万元。现在,托县医院的服务条件已有了很大改善,全院具备了为就医患者提供一定水准、不同层次医疗保健服务的能力。医院始终坚持“以患者为中心”,进一步规范全院的各项管理工作,更好地为当地经济建设和社会发展做出新的贡献。
-
*喜兵回复质量:暂无服务态度:暂无回复速度:暂无functions/format.html此用户未填写评价内容图文问诊
-
*同兆回复质量:暂无服务态度:暂无回复速度:暂无functions/format.html此用户未填写评价内容图文问诊
-
*莲香回复质量:暂无服务态度:暂无回复速度:暂无functions/format.html此用户未填写评价内容图文问诊
-
*志英回复质量:暂无服务态度:暂无回复速度:暂无functions/format.html此用户未填写评价内容图文问诊
-
*国和回复质量:暂无服务态度:暂无回复速度:暂无functions/format.html此用户未填写评价内容图文问诊
-
*建回复质量:暂无服务态度:暂无回复速度:暂无functions/format.html此用户未填写评价内容图文问诊
-
*振黎回复质量:暂无服务态度:暂无回复速度:暂无functions/format.html此用户未填写评价内容图文问诊
-
*广合回复质量:暂无服务态度:暂无回复速度:暂无functions/format.html此用户未填写评价内容图文问诊
-
*华有回复质量:暂无服务态度:暂无回复速度:暂无functions/format.html此用户未填写评价内容图文问诊
-
*永秀回复质量:暂无服务态度:暂无回复速度:暂无functions/format.html此用户未填写评价内容视频问诊
展开更多
-

近日,美国糖尿病协会(ADA)发布了2021版《糖尿病诊疗标准指南》,新指南中关于儿童糖尿病的流行病学、病理生理学以及治疗与成人糖尿病不同,为此,指南特别发布了针对儿童和青少年糖尿病的标准诊疗推荐。
营养治疗
建议儿童和青少年1型糖尿病患者进行个性化的营养治疗。
监测碳水化合物摄入是实现最佳血糖控制的一项关键。
由经验丰富的注册营养师开展全面的营养教育,每年更新一次,建议营养师评估与体重状况和心血管疾病风险因素有关的热量和营养摄入,并告知患者应该选择哪些营养素。
运动
推荐所有儿童和青少年1型糖尿病患者进行运动,每天进行60分钟中到高强度的有氧运动,每周至少进行3天高强度肌肉强化和骨骼强化活动。
确保患者运动前的血糖水平为90-250 mg/dL(5.0-13.9mmol/L),运动前、运动中、运动后可补充碳水化合物,根据计划的活动类型或强度进行个性化锻炼。
应教育患者在运动期间和运动后预防低血糖的策略,包括运动前减少餐时胰岛素剂量,减少基础胰岛素剂量,增加碳水化合物摄入,使用持续血糖监测等。
运动前、运动中、运动后的频繁血糖监测对于预防、检测和治疗运动期间低血糖和高血糖很重要。
血糖控制
儿童和青少年1型糖尿病患者应尽可能接受强化胰岛素治疗方案,即每日多次注射或持续皮下注射胰岛素。
所有儿童和青少年1型糖尿病患者每天应该多次自我监控血糖水平(每天6-10次),包括进食前,入睡前,以及一些特殊情况下,如锻炼、驾驶、出现低血糖症状等。
实时连续血糖监测+胰岛素治疗是降低和维持糖化血红蛋白水平或缓解低血糖的有效策略。
某些情况下,间歇性扫描式持续血糖监测+胰岛素治疗可以有效地取代自我血糖监测。
自动化胰岛素输送系统可被考虑用于改善血糖控制。
糖化血红蛋白目标必须个性化,并随着时间的推移进行重新评估。对于许多儿童来说,糖化血红蛋白水平<7%是合适的。
较不严格的糖化血红蛋白目标(如<7.5%)可能适合:不能明确表达出低血糖症状的患者;未察觉到的低血糖;无法获取胰岛素类似物、先进的胰岛素给药技术或连续血糖监测;不能定期检查血糖。
较不严格的糖化血红蛋白目标(<如8%)可能适用于有严重低血糖史、预期寿命有限或治疗弊大于利的患者。
如果进一步降低目标时,患者没有严重的低血糖,未对健康造成负面影响或增加诊疗负担,可以合理地为个别患者建议更严格的A1C目标(例如,<6.5%)。
建议将最近14天内的连续葡萄糖监测指标(血糖变化幅度较大的患者应更长时间),尽可能与糖化血红蛋白结合使用。
筛查和诊断
对于超重或肥胖且有一个或多个糖尿病危险因素的儿童和青少年中,应考虑在青春期开始或10岁时(以较早者为准),对糖尿病前期或2型糖尿病进行筛查。
如果检测结果正常,则应至少每3年进行一次重复检查,如果BMI增加,则检查频率增加。
空腹血糖、75g口服糖耐量试验2小时血糖和糖化血红蛋白可用于检测儿童和青少年的糖尿病前期或糖尿病。
儿童糖尿病管理
生活方式因素
应向超重/肥胖的2型糖尿病儿童青少年及家属提供综合生活方式干预计划,并与糖尿病治疗相结合,以实现减重7-10%的目标。
与所有儿童和青少年一样,应鼓励有糖尿病前期和2型糖尿病的儿童青少年每天至少参加60分钟的中到高强度的体育活动(每周至少3天肌肉和骨骼力量训练),并减少久坐行为。
与所有儿童一样,有糖尿病前期和2型糖尿病的儿童青少年的饮食应侧重于健康饮食模式,减少摄入高热量、缺乏营养的食品,特别是含糖饮料。
血糖目标
家庭血糖监测方案应个体化,并考虑到患者的药物治疗情况。
每3个月评估一次血糖状况。
对于大多数儿童和青少年2型糖尿病患者来说,仅口服药物治疗的情况下,合理A1C目标为<7%。更严格的A1C目标(如<6.5%)可能适合个别患者,例如进一步降糖没有出现显著低血糖或其他治疗不良反应。
如果低血糖风险增加,可能需要制定较不严格的A1C目标(如7.5%)。
药物治疗
诊断为2型糖尿病后,除了进行营养干预和体育活动等行为外,还应进行药物治疗。
偶然发现糖尿病或代谢稳定的患者(糖化血红蛋白<8.5%,无症状),如果肾功能正常,二甲双胍是首选的初始治疗药物。
有明显的高血糖血症(血糖≥250 mg/dL [13.9 mmol/L],糖化血红蛋白≥8.5%),诊断时无酸中毒,且有多尿、多饮、夜尿或体重减轻症状的青少年,应在开始使用二甲双胍时,先用基础胰岛素治疗。
对于酮症酸中毒患者,应开始皮下或静脉注射胰岛素治疗,以迅速纠正高血糖和代谢紊乱。一旦酸中毒缓解,可开始使用二甲双胍,同时继续皮下胰岛素治疗。
对于出现严重高血糖(血糖≥600 mg/dL [33.3 mmol/L])的患者,考虑评估高血糖高渗非酮症综合征。
如果没有甲状腺髓样癌病史或2型多发性内分泌肿瘤家族史的10岁或以上儿童,用二甲双胍(加或不加基础胰岛素)不能达到血糖目标时,则应考虑使用利拉鲁肽(GLP-1受体激动剂)。
接受基础胰岛素治疗但未达到血糖目标的患者,应改为每日多次注射基础胰岛素和餐前大剂量胰岛素。
初始使用胰岛素和二甲双胍的患者,根据家庭血糖监测结果达到血糖目标,超过2-6周的时间内,可以每隔几天减少10-30%的胰岛素剂量。
不建议使用未经FDA批准的药物治疗儿童青少年2型糖尿病患者。
手术
对于严重肥胖(BMI>35 kg/m2)、生活方式干预和药物干预后仍无法控制血糖和/或有严重合并症的2型糖尿病青少年,可以考虑进行代谢手术治疗。
参考文献:
Diabetes Care. 2021 Jan; 44(Suppl 1):S180-S199.
京东健康互联网医院医学中心
作者:肖靖,2009-2012年就读于301医院内分泌学硕士,2012年毕业后工作于北京博爱医院内分泌科。
-

新生儿双侧永久性严重听力下降的患病率约为1.1例/1000新生儿;每1000名新生儿中可能还有1-2名发生双侧轻至中度听力下降或单侧听力下降。由于新生儿听力筛查策略的实施,目前听力下降检测出的年龄已大大降低。随着年龄的增长,儿童还会因多种病因失去听力,例如颞骨骨折、耳毒性药物、遗传性听力损失的延迟发作等,据估计,18岁以前儿童的听力下降患病率高达18%。早期识别儿童听力下降,进行早期干预,包括使用助听器和强化言语治疗,可带来更好的结局。
先天性听力下降
永久性先天感觉神经性和混合性听力下降的最常见原因是先天性巨细胞病毒感染,颞骨结构异常和遗传原因。先天性巨细胞病毒感染是导致听力下降的主要原因,也很常见。先天性感染,包括梅毒和风疹,也可能会导致听力下降。风疹曾经是先天性感觉神经性耳聋的最常见病毒原因,现在由于孕妇接种疫苗而变得罕见。
许多解剖异常也与遗传原因有关,包括腮-耳-肾综合征和CHARGE综合征。腮-耳-肾综合征是一种常染色体显性遗传性疾病,主要表现为听力下降、耳前瘘管、鳃裂发育异常、肾发育不良等。CHARGE综合征是一种罕见的常染色体显性遗传病,主要表现为:眼残缺、心脏病变、后鼻孔闭锁、生长发育障碍和/或中枢神经系统畸形、性腺发育不良、耳畸形和/或耳聋。
听力下降的发生率在早产儿中有所增加,并随胎龄和出生体重的增加而发生率下降。新生儿重症监护病房(NICU)中,1.2%至7.5%的婴儿会出现听力下降;出现以下情况时,NICU相关听力下降发生率会增加:高胆红素血症,败血症,新生儿细菌性脑膜炎,坏死性小肠结肠炎,长时间机械通气,耳毒性药物,使用体外膜肺氧合等。
迟发性听力下降
如果家长发现孩子的听力、说话或交流有些问题,需考虑到迟发性听力下降的可能性。如果存在围产期危险因素,例如先天性巨细胞病毒感染或体外膜肺氧合,也可能发生迟发性听力下降。超过119个基因与感觉神经性或混合性听力下降有关。其中,综合征占所有遗传原因的30%,常与迟发性或进行性听力下降有关,包括Pendred综合征,Usher综合征和Alport综合征。
Pendred综合征是遗传性感觉神经性听力下降的最常见综合征,与甲状腺功能不全、甲状腺肿、前庭导水管增大和Mondini内耳发育不全有关。 Usher综合征也是常染色体隐性遗传病,具有3种临床类型,可基于听力下降程度、前庭功能障碍和视力丧失发病年龄进行分型。 Alport综合征通常在儿童晚期发现,可出现肾功能衰竭、眼部异常和进行性感觉神经性听力减退。
一些非综合征性隐性基因也与进行性感觉神经性听力下降有关,这些儿童可能在新生儿听力筛查中表现正常,随着年龄增长而出现进行性耳聋。这些基因包括GJB2,MYO15A和STRC。进行性听力下降的常染色体显性基因包括TMC1和KCNQ4。
先天性感染后也可能发生迟发性听力下降。基于既往报道,产前暴露于弓形虫病、风疹、巨细胞病毒、疱疹病毒、梅毒等是先天性听力下降的常见原因。但是,这些微生物的流行病学已经改变,在许多国家,已剩下先天性巨细胞病毒感染是造成迟发性听力下降的主要原因。所有新生儿中先天性巨细胞病毒感染的患病率为0.4%至2.3%。在确诊为先天性听力下降的婴儿中,有6%至7%有先天性巨细胞病毒感染。但是,高达43%的先天性巨细胞病毒感染婴儿在新生儿听力筛查中正常,随后在婴儿期或儿童期出现感觉神经性听力下降。
前几年爆发了寨卡疫情,数据显示,先天性寨卡病毒感染可能导致听觉丧失。2019年对包含巴西、哥伦比亚和美国266名寨卡感染婴儿和儿童在内的10篇文章进行分析发现,听力下降发生率范围为6%至68%。还需要更多的研究来确定进行性听力下降的可能性,并更加明确听力下降的实际患病率。
获得性听力下降
出生后的获得性听力下降的原因包括创伤、感染、耳毒性药物使用或自身免疫性疾病。儿童听力下降中,大部分是由于获得性病因引起的。在导致儿童听力下降的可预防病因中,世界卫生组织将31%归因于感染,17%为产后并发症,4%为母婴使用耳毒性药物(如氨基糖苷类),8%为其他原因。
创伤可能导致传导性、混合性或感觉神经性听力下降,具体取决于颞骨损伤的部位和类型。鼓膜穿孔或听骨链损伤可导致传导性听力下降。颞骨骨折可损伤耳蜗、耳蜗神经或引起淋巴管瘘,这通常会导致严重的感觉神经性听力下降。颞骨震荡伤而没有骨折,也可能导致暂时性或永久性感觉神经性听力下降。
感觉神经性听力下降的感染原因包括麻疹、腮腺炎、水痘带状疱疹、莱姆病、细菌性脑膜炎等。与接种疫苗的儿童相比,未接种疫苗的儿童更容易患麻疹和腮腺炎并伴有听力下降。莱姆病可导致听力下降,但较罕见且可以治疗。听力下降常见病因为细菌性脑膜炎,可能是进行性的,最常见的是肺炎链球菌感染。
已知具有耳毒性并可能导致永久性听力损失的药物包括氨基糖苷类、抗肿瘤药(尤其是顺铂)、袢利尿剂;其他药物,例如水杨酸和大环内酯类药物(包括阿奇霉素),导致的听力损失通常是可逆的。密切监测药物剂量和血清水平可以减少内耳损伤的可能性。
自身免疫相关的听力下降原因包括局限于内耳的自身免疫功能障碍或系统性自身免疫疾病,例如Cogan综合征(间质性角膜炎、进行性听力损失和前庭功能障碍)。听力下降通常迅速进展,可能对免疫抑制剂有反应。
参考文献:
JAMA. 2020; 324(21):2195-2205.
京东健康互联网医院医学中心
作者:李延龙,北京协和医学院硕士,专业方向为慢性病的预防与控制。以第一作者或共同作者在国内外期刊发表论文10余篇。
-


说到减肥,就很容易能让人联想到运动,而说到运动,最先能与之“挂钩”的便是跑步。是的,放眼当前的“减肥大军”,跑步减肥已经成为了一种时尚和流行趋势,越来越多的人加入了跑步减肥或者跑步维持体重的行列。那么问题来了,运动的确有益健康,可对于当前体重处于肥胖状态的胖友们来说,跑步减肥真的健康吗?对于这个问题,骨科医生是这样说的。
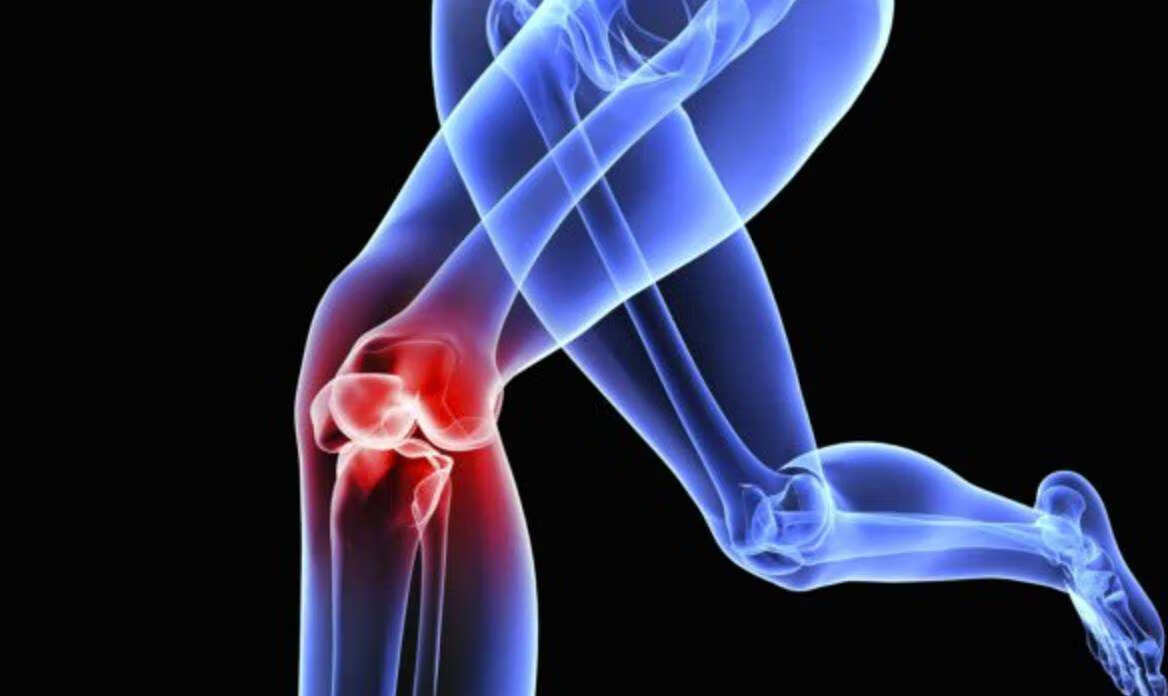
跑步减肥损伤膝关节
骨骼,是人体最重要的组织之一,担负着人体负重、支持、保护、运动、造血等等重要的生理作用。不同的运动方式对于人体骨骼的影响也会截然不同,当人的运动强度太大或者运动量太大时,则极易引起关节软骨不可逆性的损伤。关节软骨,位处于关节处的骨头与骨头之间,可避免骨头间直接硬碰硬的摩擦和震动,具有缓冲震荡、保护关节骨面作用。在运动过程中,如果运动强度或者运动量超过软骨组织所承受的负荷,无论是超过临界值的单次冲击,还是小于临界值的多次大幅度的钝性刺激,均可能会造成关节软骨的损伤,而且人体的关节软骨在受损后多为不可逆性的伤害。
膝盖损伤发现之时已经晚了
需要注意的是,骨骼间的软骨就像薄薄的冰层那样光滑且脆弱,它不含血管、神经、以及淋巴组织,所需要的营养主要来源于滑液的弥散。因此,不但关节软骨的自我修复能力很弱,当关节软骨受损时,人们也通常不会有疼痛感,直至它被磨损殆尽,损伤直接延至骨头时,人们才会因骨骼上神经的疼痛引发注意,但往往这时的病情已经比较严重,甚至需要住院治疗。

肥胖的人不适合跑步减肥
当今社会,跑步已经是非常普遍的、被平民化的运动方式,但事实上跑步并非适合所有的人群,尤其对肥胖患者来说,跑步并非减肥良方。肥胖的人,即使在静止状态下,其膝关节所承受的压力也会高于体重正常的人,如果在身体负重较重的前提下,还经常跑步,则会给膝关节带来更大的压力。关节软骨处因为没有神经,无法对磨损和伤害及时做出应激反应并让人可以及时止损,只有在软骨被磨损到一定程度时,才会感到某种不适。因此,体重超重或者肥胖的人,如果因经常跑步而导致软骨受到损伤,被发现时通常伤害已经不可逆转,只能通过手术来解决问题了。
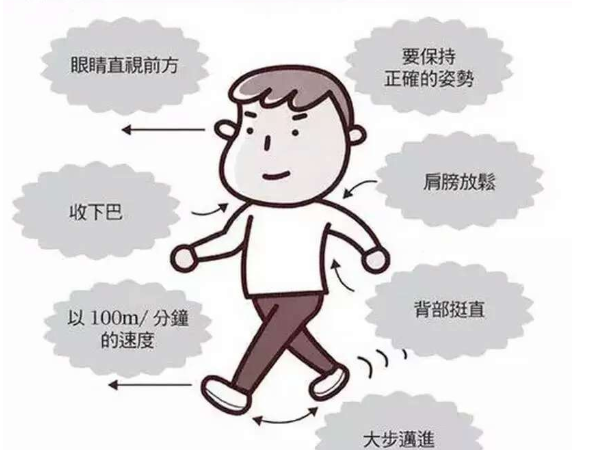
适合减肥的运动方式
运动减肥虽然能够让人健康的变瘦,但在减肥过程中却应该谨慎的选择运动方式,在身体的体重还不允许的前提下,应尽量避免用跑步的方式减肥。其实,有很多运动方式都比跑步更加适合消耗人体的能量,如游泳、骑单车等,如果实在喜欢行走的运动方式,在减肥初期也可以选择快走这一运动项目。快走与跑步属于同一类型的运动,同一时间段内虽然消耗的热量稍小于跑步,但其对关节处的伤害也远远小于跑步。减肥本就不是一朝一夕就能完成的事情,只有坚持下去才能看到成功的希望,从这个角度上来说,快走也比跑步更适合减肥者,您认为呢。
-
 孩子瘦的标准是什么?孩子瘦是指体重不足,常常在同龄、同性别儿童平均体重的两个标准差以下。或者是体重低于同性别、同身高参照人群值的均值两个标准差以上。首先是要查出孩子瘦的病因是什么,然后治疗病因的同时,逐渐给予营养支持治疗,直到达到标准体重。主要的是要学会合理的喂养,在孩子不同的发育阶段给予足量的营养物质,以满足婴儿生长的需要。婴儿期要按照正确的比例配置奶粉,保证足够的乳量。按时给孩子添加饮食,从小要养成孩子良好的饮食习惯,及时的纠正孩子偏食、挑食以及爱吃小食品的不良饮食习惯。始终要保证营养均衡,糖,蛋白质,脂肪,维生素,矿物质等要遵循一定的比例。并且要定期监测孩子的体重,身高。孩子瘦的病因有哪些?1.孩子摄入的营养物质不足造成。在婴儿期多由于喂养量不足或者人工喂养的宝宝奶粉配制的浓度过稀,以及没有及时的添加辅食,或者添加辅食的营养成分不能满足婴儿生长的需要;对于稍大一点的孩子,由于存在偏食、挑食、爱吃零食等不良的饮食习惯而导致营养摄入不足。2.存在消化系统的疾病而导致消化吸收不良。常见的疾病有先天性的消化道畸形,反复迁延的腹泻,(食物过敏、乳糖不耐受)等,影响消化吸收功能。3.婴幼儿对营养的需要量增加而引起营养的相对不足。如存在慢性疾病(糖尿病肾病,发热性疾病,甲亢,恶性肿瘤等),在急慢性传染病的恢复期,生长发育快速阶段,早产和双胎在追赶生长等等。
孩子瘦的标准是什么?孩子瘦是指体重不足,常常在同龄、同性别儿童平均体重的两个标准差以下。或者是体重低于同性别、同身高参照人群值的均值两个标准差以上。首先是要查出孩子瘦的病因是什么,然后治疗病因的同时,逐渐给予营养支持治疗,直到达到标准体重。主要的是要学会合理的喂养,在孩子不同的发育阶段给予足量的营养物质,以满足婴儿生长的需要。婴儿期要按照正确的比例配置奶粉,保证足够的乳量。按时给孩子添加饮食,从小要养成孩子良好的饮食习惯,及时的纠正孩子偏食、挑食以及爱吃小食品的不良饮食习惯。始终要保证营养均衡,糖,蛋白质,脂肪,维生素,矿物质等要遵循一定的比例。并且要定期监测孩子的体重,身高。孩子瘦的病因有哪些?1.孩子摄入的营养物质不足造成。在婴儿期多由于喂养量不足或者人工喂养的宝宝奶粉配制的浓度过稀,以及没有及时的添加辅食,或者添加辅食的营养成分不能满足婴儿生长的需要;对于稍大一点的孩子,由于存在偏食、挑食、爱吃零食等不良的饮食习惯而导致营养摄入不足。2.存在消化系统的疾病而导致消化吸收不良。常见的疾病有先天性的消化道畸形,反复迁延的腹泻,(食物过敏、乳糖不耐受)等,影响消化吸收功能。3.婴幼儿对营养的需要量增加而引起营养的相对不足。如存在慢性疾病(糖尿病肾病,发热性疾病,甲亢,恶性肿瘤等),在急慢性传染病的恢复期,生长发育快速阶段,早产和双胎在追赶生长等等。 -
 很多白血病患者的亲人,因为对捐献造血干细胞心存疑虑而拒绝捐献,使患者失去了生命延续的机会。如果大家对于捐献造血干细胞能多一点了解,很多患者会得到及时、有效的治疗。捐献造血干细胞,其实就是老百姓常说的「捐献骨髓」。在以前,为了获得造血干细胞,需要采集供者(即捐献造血干细胞的人)的骨髓,过程比较痛苦;现在,只需要像献血那样,从血管中收集造血干细胞即可,无需进行骨髓穿刺。对于白血病人来说,最好的造血干细胞来源是同父同母、配型相合的兄弟姐妹,其次是配型相合的没有血缘关系的志愿者。捐献造血干细胞的过程高分辨确认:在捐献之前,供者需要再次与患者进行配型,确定是否配型成功。身体检查:供者需要进行查体,必须查体合格,并且确定愿意捐献,才能进入下面的流程。动员骨髓:造血干细胞主要存在于骨髓,血液中含量极低。「动员」就是给供者皮下注射药物,促进骨髓产生更多的造血干细胞,并释放至血液循环中。这个过程需要 4~5 天。动员过程中需每天检测血常规,保证供者的白细胞在安全范围内。采集干细胞:用机器采集供者的静脉血,机器将有效成分收集后,其余成分再输回供者体内。一般采集需 3~5 小时,每次分离 200~400 mL 全血,经若干次循环后,最终采出有效成分 150~250 mL 左右。如果采集出的造血干细胞数量不足,需第二天再次采集。经过检验,确定采集到足够移植的造血干细胞数量后,由工作人员会将采集物在最短的时间内送至患者所在医院,并立即输至患者体内。供者休息 3~5 天后可以恢复正常工作、生活,无需特别补充保健品、营养品。捐献造血干细胞有什么不良反应吗?捐献造血干细胞的过程整体上是安全的,发生严重不良事件,如血栓、脾破裂的概率仅为 1.1%。动员阶段不良反应超过半数的供者会有骨骼酸痛感,这是由于骨髓的造血干细胞快速增殖分化而引起;少数供者会出现燥热、兴奋、乏力等类似普通感冒的情况;极少数供者有过敏、左上腹饱胀感(脾脏肿大)等现象。这些不良反应绝大部分供者能耐受,仅需对症处理,比如口服止痛药物、安眠镇静药物等;采集结束后,这些症状可能自行消失。采集阶段不良反应采集过程中,供者可能出现手足、嘴唇麻木感,这是由于缺钙引起。口服葡萄糖酸钙或静脉使用钙剂即可缓解,采集前适当喝点高钙牛奶也可以减少此症状的发生。少数供者可能出现头晕、乏力、心慌、血压偏低的情况,这是由于采集过程导致了轻度脱水。减慢采集速度,或者静脉补充生理盐水,即可缓解。采集管路均为一次性无菌产品,故发生血液污染、获得传染病的概率几乎为零。完成采集过程后,供者血常规检测会有白细胞偏高、血小板偏低的现象,1~2 周后可恢复至正常,不影响正常生活。目前还没有由于捐献造血干细胞造成长期身体健康损害的事情发生,那些所谓影响生育功能、影响寿命的说法更是无稽之谈。希望大家能正视造血干细胞捐献,为白血病患者再次点燃生命的希望!
很多白血病患者的亲人,因为对捐献造血干细胞心存疑虑而拒绝捐献,使患者失去了生命延续的机会。如果大家对于捐献造血干细胞能多一点了解,很多患者会得到及时、有效的治疗。捐献造血干细胞,其实就是老百姓常说的「捐献骨髓」。在以前,为了获得造血干细胞,需要采集供者(即捐献造血干细胞的人)的骨髓,过程比较痛苦;现在,只需要像献血那样,从血管中收集造血干细胞即可,无需进行骨髓穿刺。对于白血病人来说,最好的造血干细胞来源是同父同母、配型相合的兄弟姐妹,其次是配型相合的没有血缘关系的志愿者。捐献造血干细胞的过程高分辨确认:在捐献之前,供者需要再次与患者进行配型,确定是否配型成功。身体检查:供者需要进行查体,必须查体合格,并且确定愿意捐献,才能进入下面的流程。动员骨髓:造血干细胞主要存在于骨髓,血液中含量极低。「动员」就是给供者皮下注射药物,促进骨髓产生更多的造血干细胞,并释放至血液循环中。这个过程需要 4~5 天。动员过程中需每天检测血常规,保证供者的白细胞在安全范围内。采集干细胞:用机器采集供者的静脉血,机器将有效成分收集后,其余成分再输回供者体内。一般采集需 3~5 小时,每次分离 200~400 mL 全血,经若干次循环后,最终采出有效成分 150~250 mL 左右。如果采集出的造血干细胞数量不足,需第二天再次采集。经过检验,确定采集到足够移植的造血干细胞数量后,由工作人员会将采集物在最短的时间内送至患者所在医院,并立即输至患者体内。供者休息 3~5 天后可以恢复正常工作、生活,无需特别补充保健品、营养品。捐献造血干细胞有什么不良反应吗?捐献造血干细胞的过程整体上是安全的,发生严重不良事件,如血栓、脾破裂的概率仅为 1.1%。动员阶段不良反应超过半数的供者会有骨骼酸痛感,这是由于骨髓的造血干细胞快速增殖分化而引起;少数供者会出现燥热、兴奋、乏力等类似普通感冒的情况;极少数供者有过敏、左上腹饱胀感(脾脏肿大)等现象。这些不良反应绝大部分供者能耐受,仅需对症处理,比如口服止痛药物、安眠镇静药物等;采集结束后,这些症状可能自行消失。采集阶段不良反应采集过程中,供者可能出现手足、嘴唇麻木感,这是由于缺钙引起。口服葡萄糖酸钙或静脉使用钙剂即可缓解,采集前适当喝点高钙牛奶也可以减少此症状的发生。少数供者可能出现头晕、乏力、心慌、血压偏低的情况,这是由于采集过程导致了轻度脱水。减慢采集速度,或者静脉补充生理盐水,即可缓解。采集管路均为一次性无菌产品,故发生血液污染、获得传染病的概率几乎为零。完成采集过程后,供者血常规检测会有白细胞偏高、血小板偏低的现象,1~2 周后可恢复至正常,不影响正常生活。目前还没有由于捐献造血干细胞造成长期身体健康损害的事情发生,那些所谓影响生育功能、影响寿命的说法更是无稽之谈。希望大家能正视造血干细胞捐献,为白血病患者再次点燃生命的希望! -
 我们将迎来冬至在《月令七十二候集解》里写到:冬至,十一月中。终藏之气至此而极也。冬至并不是指冬天到了“至”表示极,最古人认为此时阴极之至,阳气始生它有一点物极必反,否极泰来的意思也就是指冬至时天地之间的阴气到达极点,最大但,同时也迎来转机阳气开始复苏萌芽冬至是我们所在的北半球全年中白天最短夜晚最长的一天过了这一天后白天开始慢慢变长夜晚慢慢开始变短所以你也可以把冬至理解为一年中真正的开始老规矩先来看冬至三侯冬至一候:蚯蚓结古人认为蚯蚓是阴曲阳伸的动物冬至时一阳初生阳气刚刚露出个小苗苗此时阴气仍然十分强盛所以地里的蚯蚓依然蜷缩着身体弯弯曲曲像打了结一般冬至二候:麋[mí]角解鹿是山兽属阳糜是水泽之兽属阴此时阳气开始冒头糜感到阳气之后头上的角开始脱落冬至三候:水泉动山中的泉水也感受到阳气的温热冰面之下泉水开始流动从立秋开始天地间的阳热之气开始下沉冬至时阳热降极而升但是阳气升得很微弱微弱到蚯蚓仍蜷曲着身体不能完全舒展开来到二候时麋鹿的角也开始一点点脱落三候时山中的泉水开始一点点流动这说明什么冬至时阴气仍非常强盛,阳气还十分微弱这种状态好比在一片漆黑的房间中只有一根蜡烛在散发着微弱的烛光(阳气)这时候我们应该怎么做?尽量让身边的人和事安静下来以免惊扰到这微弱的烛光(阳气)甚至会用手遮挡在它四周以免它被周围的风吹灭人与天地相应对于人来说也是一样的要尽量让自己心平气和守静养心养阳此时养生应该注意什么呢?一,藏身,藏精,藏汗——静待阳生藏身就是不该露的不露用衣服把自己身体藏起来从冬至开始我们就要进入最冷的三九严寒寒气是最伤阳气的藏精就是能少啪就少啪能不熬夜就不熬夜内经里有句话叫:冬不藏精,春必病温冬天本来就是养精蓄锐的时间我们敛阴护阳还来不及所以要避免过度消耗肾精藏汗就是不该出的汗尽量少出不要过度剧烈大汗淋漓运动因为汗随气出大量流汗的伤阴又伤气这时候要少做惊扰阳气的事情二,冬至后适当养阳前面说了冬至时阴气极重,一阳初生此时阳气很微弱除了藏身,藏精,藏汗我们还可以做一些养阳的事比如常晒背,多泡脚背部是人体的阳中之阳冬天晒晒后背有助于补益身体阳气另外“寒从脚起”冬天泡脚不仅可以温煦双脚还可以帮我们调理体质我曾经有个患者用温胆汤泡脚一个月后整整瘦了六斤她没有做任何运动,没有改变任何饮食为什么?因为温胆汤可以健脾助运可以祛湿,消水肿如果想祛寒湿助阳的话可以用我们的补肾通络包它可以补肾阳,舒筋通络,引火归元祛风、寒湿,活血通络三,谨慎温补冬至仍是进补的好时机但是今年冬至后进补要谨慎温补今年冬天外有寒湿,内有燥热关于这点我之前已经分析过好几次了昨天门诊我就碰到一个8岁的小朋友爷爷说冬天要补一补给他买了白切羊肉吃完后身上发了红疹这个孩子本来就阴虚内热再吃性温的羊肉等于火上浇油热有余就要散全身发红疹就是“散热”的表现切记饮食宜清淡多吃一些滋阴润肺的百合,银耳,石斛不宜过食辛辣燥热,肥腻的食物最后说一下,今天的土木相合,土星、木星、地球连城一线。其实今年3月火星,木星与土星就有黎明时分相遇;10月初,又出现火星冲日;还有10月底,石家庄出现双日同天,11月初时,沈阳天空中出现“三个太阳”11月15日商洛又出现双日。。。庚子年还出现很多自然大事和预言澳大利亚森林大大火,新冠,东非蝗灾,南极出现历史高温,红色积雪,加州大火,9月拉尼娜现象。。。要不要担心那些可怕的预言?木是生命之机,木主仁义,代表观念,伦理;土主信,象征着法度,社会制度,权威木克土,加上庚子年,是会有变革之象子月,对应的本来就是地雷复卦木土变革,在一阳来复的时刻发生,这代表着变革中有净化的力量发生。什么是净化?好的留下,坏的去掉什么是好?什么是坏?老子早就把答案告诉我们了——执大象,天下往无论环境如何,无论经历什么黑暗,天道不改,正道不移与人为善,顺应天道得以善终与人为恶,倒行逆施,私欲者这必将自食恶果坚定这一点信念后正气存内,邪不可干,精神内守,病安从来。
我们将迎来冬至在《月令七十二候集解》里写到:冬至,十一月中。终藏之气至此而极也。冬至并不是指冬天到了“至”表示极,最古人认为此时阴极之至,阳气始生它有一点物极必反,否极泰来的意思也就是指冬至时天地之间的阴气到达极点,最大但,同时也迎来转机阳气开始复苏萌芽冬至是我们所在的北半球全年中白天最短夜晚最长的一天过了这一天后白天开始慢慢变长夜晚慢慢开始变短所以你也可以把冬至理解为一年中真正的开始老规矩先来看冬至三侯冬至一候:蚯蚓结古人认为蚯蚓是阴曲阳伸的动物冬至时一阳初生阳气刚刚露出个小苗苗此时阴气仍然十分强盛所以地里的蚯蚓依然蜷缩着身体弯弯曲曲像打了结一般冬至二候:麋[mí]角解鹿是山兽属阳糜是水泽之兽属阴此时阳气开始冒头糜感到阳气之后头上的角开始脱落冬至三候:水泉动山中的泉水也感受到阳气的温热冰面之下泉水开始流动从立秋开始天地间的阳热之气开始下沉冬至时阳热降极而升但是阳气升得很微弱微弱到蚯蚓仍蜷曲着身体不能完全舒展开来到二候时麋鹿的角也开始一点点脱落三候时山中的泉水开始一点点流动这说明什么冬至时阴气仍非常强盛,阳气还十分微弱这种状态好比在一片漆黑的房间中只有一根蜡烛在散发着微弱的烛光(阳气)这时候我们应该怎么做?尽量让身边的人和事安静下来以免惊扰到这微弱的烛光(阳气)甚至会用手遮挡在它四周以免它被周围的风吹灭人与天地相应对于人来说也是一样的要尽量让自己心平气和守静养心养阳此时养生应该注意什么呢?一,藏身,藏精,藏汗——静待阳生藏身就是不该露的不露用衣服把自己身体藏起来从冬至开始我们就要进入最冷的三九严寒寒气是最伤阳气的藏精就是能少啪就少啪能不熬夜就不熬夜内经里有句话叫:冬不藏精,春必病温冬天本来就是养精蓄锐的时间我们敛阴护阳还来不及所以要避免过度消耗肾精藏汗就是不该出的汗尽量少出不要过度剧烈大汗淋漓运动因为汗随气出大量流汗的伤阴又伤气这时候要少做惊扰阳气的事情二,冬至后适当养阳前面说了冬至时阴气极重,一阳初生此时阳气很微弱除了藏身,藏精,藏汗我们还可以做一些养阳的事比如常晒背,多泡脚背部是人体的阳中之阳冬天晒晒后背有助于补益身体阳气另外“寒从脚起”冬天泡脚不仅可以温煦双脚还可以帮我们调理体质我曾经有个患者用温胆汤泡脚一个月后整整瘦了六斤她没有做任何运动,没有改变任何饮食为什么?因为温胆汤可以健脾助运可以祛湿,消水肿如果想祛寒湿助阳的话可以用我们的补肾通络包它可以补肾阳,舒筋通络,引火归元祛风、寒湿,活血通络三,谨慎温补冬至仍是进补的好时机但是今年冬至后进补要谨慎温补今年冬天外有寒湿,内有燥热关于这点我之前已经分析过好几次了昨天门诊我就碰到一个8岁的小朋友爷爷说冬天要补一补给他买了白切羊肉吃完后身上发了红疹这个孩子本来就阴虚内热再吃性温的羊肉等于火上浇油热有余就要散全身发红疹就是“散热”的表现切记饮食宜清淡多吃一些滋阴润肺的百合,银耳,石斛不宜过食辛辣燥热,肥腻的食物最后说一下,今天的土木相合,土星、木星、地球连城一线。其实今年3月火星,木星与土星就有黎明时分相遇;10月初,又出现火星冲日;还有10月底,石家庄出现双日同天,11月初时,沈阳天空中出现“三个太阳”11月15日商洛又出现双日。。。庚子年还出现很多自然大事和预言澳大利亚森林大大火,新冠,东非蝗灾,南极出现历史高温,红色积雪,加州大火,9月拉尼娜现象。。。要不要担心那些可怕的预言?木是生命之机,木主仁义,代表观念,伦理;土主信,象征着法度,社会制度,权威木克土,加上庚子年,是会有变革之象子月,对应的本来就是地雷复卦木土变革,在一阳来复的时刻发生,这代表着变革中有净化的力量发生。什么是净化?好的留下,坏的去掉什么是好?什么是坏?老子早就把答案告诉我们了——执大象,天下往无论环境如何,无论经历什么黑暗,天道不改,正道不移与人为善,顺应天道得以善终与人为恶,倒行逆施,私欲者这必将自食恶果坚定这一点信念后正气存内,邪不可干,精神内守,病安从来。 -
 乳腺恶性肿瘤在临床上是属于比较常见的,可以分为乳腺癌和乳腺肉瘤,其中以乳腺癌的发病率最高。乳腺肉瘤在临床上并不多见,但是其恶性程度是比较高的。常见的临床症状有乳房肿块、乳头溢液、乳房皮肤的改变、局部腋窝淋巴结肿大、体重减轻、全身乏力、持续性低热等。从临床上来看,乳腺肉瘤也是可以治愈的,但是需要结合肉瘤具体的分期以及治疗效果来进行全面的评估。对于早期的乳腺肉瘤患者,通过局部的手术切除时可以达到根治的,术后在辅助以放化疗可以达到临床治愈的标准。对于中晚期乳腺肉瘤患者主要的治疗方案包括手术切除、放化疗、靶向治疗、免疫治疗等。通过合理的治疗方法来尽可能的控制病情的发展。中晚期乳腺肉瘤患者的临床治愈率是比较低的,通过合理的治疗方案来尽可能的延长患者的生存期,同时提高其生存质量。总之,虽然乳腺肉瘤在临床上的发病率是比较低的,但是在日常生活中发现有乳腺肿块,特别是无痛性的肿块是需要引起警惕的。积极地进行乳腺肿块的弹性彩超来明确具体的分期,通过局部的穿刺活检病理诊断明确具体的病理类型,然后选择合适的治疗方案来控制病情。同时在治疗过程中要注意患者可能出现的相关药物不良反应,及时对症治疗来保证治疗的顺利进行,才能有效的提高乳腺肉瘤的治愈率。
乳腺恶性肿瘤在临床上是属于比较常见的,可以分为乳腺癌和乳腺肉瘤,其中以乳腺癌的发病率最高。乳腺肉瘤在临床上并不多见,但是其恶性程度是比较高的。常见的临床症状有乳房肿块、乳头溢液、乳房皮肤的改变、局部腋窝淋巴结肿大、体重减轻、全身乏力、持续性低热等。从临床上来看,乳腺肉瘤也是可以治愈的,但是需要结合肉瘤具体的分期以及治疗效果来进行全面的评估。对于早期的乳腺肉瘤患者,通过局部的手术切除时可以达到根治的,术后在辅助以放化疗可以达到临床治愈的标准。对于中晚期乳腺肉瘤患者主要的治疗方案包括手术切除、放化疗、靶向治疗、免疫治疗等。通过合理的治疗方法来尽可能的控制病情的发展。中晚期乳腺肉瘤患者的临床治愈率是比较低的,通过合理的治疗方案来尽可能的延长患者的生存期,同时提高其生存质量。总之,虽然乳腺肉瘤在临床上的发病率是比较低的,但是在日常生活中发现有乳腺肿块,特别是无痛性的肿块是需要引起警惕的。积极地进行乳腺肿块的弹性彩超来明确具体的分期,通过局部的穿刺活检病理诊断明确具体的病理类型,然后选择合适的治疗方案来控制病情。同时在治疗过程中要注意患者可能出现的相关药物不良反应,及时对症治疗来保证治疗的顺利进行,才能有效的提高乳腺肉瘤的治愈率。 -
非小细胞肺癌 (NSCLC) 占所有肺癌病例的 85%,其中 15-30% 是肺鳞状细胞癌。许多研究已经深入探索了NSCLC的致病基因,基于基因分型的靶向治疗已经成为非常成功的治疗方法。近年来,PD-1/ PD-L1抑制剂已逐渐成为NSCLC患者一线或二线治疗的标准疗法。
两种抗PD-1 抗体(纳武单抗和派姆单抗)以及两种抗PD-L1抗体(阿特珠单抗和德瓦鲁单抗)已被批准用于治疗NSCLC。本文旨在概述PD-1/PD-L1 抑制剂用于 NSCLC 患者的一线、二线和三线治疗的最新进展。
目前NSCLC的治疗方案很多,包括放疗、铂类化疗、手术切除和分子靶向治疗等,但长期疗效仍然不甚理想,5年生存率低于18%。因此,迫切需要具有较低毒性和较高疗效的新型临床疗法,进一步延长患者的生存时间。目前,部分抗PD-1/PD-L1抗体已获得批准用于晚期NSCLC的治疗。
PD-1/PD-L1 抑制剂用于一线治疗
多项 KEYNOTE 试验正在研究各种肿瘤类型中使用 PD-1/PD-L1 抑制剂的效果,NSCLC患者是关注的重点人群。在开放标签的 Ib 期 KEYNOTE-001 试验中,肿瘤组织表达PD-L1的晚期 NSCLC 患者, 接受派姆单抗治疗后,客观缓解率 (ORR) 为 27%,中位无进展生存期(mPFS)为 6.2 个月,中位总生存期 (mOS) 为 22.1 个月。PD-L1 肿瘤比例评分 (TPS) ≥ 50% 的患者,ORR、1 年 mPFS 和 1 年 mOS 均显著高于总体人群。结果表明,派姆单抗耐受性良好。
对于晚期鳞状 NSCLC 患者,KEYNOTE-407 试验表明,与单独传统化疗(卡铂+紫杉醇)相比,卡铂加紫杉醇和派姆单抗联合治疗组的 mOS 和 mPFS更长。KEYNOTE-407最终分析的疗效结果显示,在中位随访 14.3个月后,与安慰剂联合化疗相比,派姆单抗联合化疗的 mOS(17.1 个月 vs. 11.6 个月)和 mPFS(8.0 个月vs. 5.1 个月)均得到明显改善。
在 CheckMate 012 试验中,52 名患者接受纳武单抗治疗,直至出现疾病进展或出现毒性。整体来讲,患者的 ORR 为 28%,mPFS 和 mOS 分别为 3.6 个月和 19.4 个月。
另一项开放标签的 I 期试验CheckMate 012中,对 78 名接受纳武单抗(两周一次)加伊匹单抗(12周一次),或纳武单抗(两周一次)加伊匹单抗(6周一次)的患者进行了评估。 纳武单抗加伊匹单抗作为一线治疗获得了良好的耐受性和安全性,临床疗效令人鼓舞,每组都有较好的 ORR。在CheckMate 227试验中,相比单独化疗,纳武单抗联合伊匹单抗作为一线治疗晚期NSCLC患者的mPFS明显延长。
阿特珠单抗和德瓦鲁单抗是针对 PD-L1 免疫球蛋白 G1的单克隆抗体,可与 PD-L1 结合阻断PD-1/PD-L1介导的信号通路。BIRCH试验旨在衡量阿特珠单抗作为一线、二线和三线疗法在晚期 NSCLC 中的疗效。 在接受阿特珠单抗一线治疗的 139 名晚期 NSCLC 患者中,ORR、mPFS 和 mOS 分别为 22%、5.4 个月和 20.1 个月。
IMpower150是一项开放标签的III期研究,旨在评估阿特珠单抗联合贝伐珠单抗和化疗用于晚期NSCLC患者一线治疗的疗效。患者接受阿特珠单抗+卡铂+紫杉醇(ACP),或贝伐珠单抗+卡铂+紫杉醇(BCP),或阿特珠单抗+贝伐珠单抗+卡铂+紫杉醇(ABCP)治疗。结果显示,无论PD-L1的表达水平和遗传状态如何,与ACP或BCP组相比,ABCP组中转移性非鳞状NSCLC患者的mPFS和mOS均显著改善。
在 Ib 期试验中,德瓦鲁单抗和抗 CTLA-4 抗体替西木单抗被用于治疗晚期 NSCLC 患者。整体来讲,德瓦鲁单抗联合替西木单抗组的 ORR 为 23%。MYSTIC 试验是一项开放标签的 III 期试验,在晚期 NSCLC 患者中比较德瓦鲁单抗联合或不联合替西木单抗与单独铂类化疗用于一线治疗的效果。在肿瘤细胞 PD-L1 表达⩾25%的患者中,与单独化疗相比,德瓦鲁单抗组在 mOS 方面出现明显改善。
PD-1/PD-L1 抑制剂用于二线治疗
抗 PD-1抗体 纳武单抗是第一个被批准作为 IV 期 NSCLC 的二线治疗药物。CheckMate 017,一项随机、开放标签、III 期研究,评估了纳武单抗治疗晚期鳞状NSCLC的疗效和安全性;在一线化疗期间或之后获得了更大的疗效。无论 PD-L1 表达水平如何,纳武利尤单组的 mOS、ORR 和 mPFS 均明显优于多西他赛组。
KEYNOTE-010 是一项开放标签、随机 II/III 期试验,纳入接受过派姆单抗或多西他赛治疗的肿瘤细胞中PD-L1表达水平⩾1% 的NSCLC 患者。研究表明,派姆单抗治疗可显著延长既往接受过治疗的晚期 NSCLC 患者的 mOS,尤其是那些 PD-L1 表达水平高的患者。
一项随机 III 期临床试验 OAK研究表明,无论 PD-L1 的表达水平如何,与多西他赛相比,阿特珠单抗治疗后的生存率都有明显提高。基于 OAK 的研究结果, 阿特珠单抗已被 FDA 和EMA 批准用于治疗先前接受过其他疗法的晚期 NSCLC 患者。研究显示,阿特珠单抗组的患者,ORR为14%,mOS为13.8 个月。
PD-1/PD-L1 抑制剂用于三线治疗
BIRCH 研究检查了阿特珠单抗作为晚期 NSCLC 的三线或更后线治疗的临床疗效。阿特珠单抗作为三线治疗,mOS、mPFS和ORR分别为13.2个,2.8个月和18%,表明 阿特珠单抗作为三线治疗晚期NSCLC具有良好的临床疗效。
ATLANTIC试验,旨在评估德瓦鲁单抗用于晚期 NSCLC患者的三线或更后线治疗的疗效。PD-L1表达水平⩾25%的EGFR阳性和ALK阳性患者接受德瓦鲁单抗治疗的ORR为12.2%, PD-L1表达水平⩾25%的EGFR阴性和ALK阴性患者的ORR为16.4%,PD-L1表达水平 ⩾ 90% 的患者为30.9%。三组的 mPFS分别为1.9个月、3.3个月和2.4个月。
ARCTIC试验在晚期NSCLC患者中评估了德瓦鲁单抗联合或不联合替西木单抗作为三线以后治疗的疗效。对于 PD-L1⩾25%的患者,与标准治疗相比,德瓦鲁单抗可显著改善 mOS 和 mPFS。对于PD-L1表达<25%的患者,与标准治疗相比,德瓦鲁单抗联合替西木单抗可显著改善mOS。
总结
迄今为止,四种抗PD-1/PD-L1药物,包括纳武单抗、派姆单抗、阿特珠单抗和德瓦鲁单抗,已被批准用于NSCLC的新辅助、一线和二线治疗。随着免疫检查点抑制剂的获批,基于调节PD-1/PD-L1信号的免疫检查点疗法为晚期NSCLC患者的治疗提供了更多选择。
参考文献:
Ther Adv Med Oncol. 2021; 13:1758835921992968.
京东健康互联网医院医学中心
作者:刘山水,医学博士、副教授。研究疾病领域为老年疾病及常见慢病,已在国内外医学期刊发表署名论文80余篇。
展开更多












