粘液肉瘤是一种较为复杂的疾病,对于是否需要切除,应由医生根据患者的具体情况进行综合判断,对于放疗和化疗不敏感,手术彻底切除可能是唯一选择。粘液肉瘤是一种恶性肿瘤。粘液肉瘤因成纤维细胞内含有大量的粘液为特征,是一种会反复“野蛮生长”的肿块,极少远处转移,对放疗和化疗不敏感,具有较高的复发率。如果能够通过手术彻底切除,可以显著降低肿瘤的复发几率,提高患者的生活质量。
如果患有粘液肉瘤,建议及时就医并咨询医生,以获得专业的治疗意见。

心脏粘液肉瘤是一种较为少见的良性肿瘤,通常需要通过手术治疗。手术采用低温体外循环下阻断心脏循环的方法,在直视下切除肿瘤,常用胸骨正中切口。未阻断前主动脉,应避免搬动心脏、心内以及心外进行探查。在肿瘤摘除后,心腔已经彻底的冲洗,以防肿块遗留于心腔内。最后修补房间隔缺损与缝合切口。单纯心脏黏液瘤患者若无全身反应,可作常规择期手术对待,但须最优先安排,不得延误。
全身反应严重、病情发展快且有凶险征象者、排除非黏液瘤因素后,应作急诊手术安排。反复发作动脉栓塞有死亡威胁者、长期发热,大量抗生素治疗一段时间无效,而又不能排除高热系由黏液瘤本身引起者,应在继续应用抗生素同时,急诊手术,不要拖延。有慢性心衰表现,身体衰弱,夜间不能平卧、端坐呼吸、肝大、腹水、下肢浮肿病例,应在查明无其它因素,积极控制心衰,待病情平稳后安排手术治疗。
有心脏粘液肉瘤的患者建议找专业医生进一步判断制定合理的治疗方案。

怀孕后乳头上有肉瘤可能是蒙氏结节、皮脂腺增生、乳腺纤维瘤等原因导致。
1.蒙氏结节:在女性怀孕期间,由于激素的刺激,乳晕周围的皮脂腺会增生,形成小肉粒,有助于散发异味,使新生儿更容易找到乳头。
2.皮脂腺增生:怀孕后雌孕激素刺激会导致皮脂分泌增多,毛囊口不能及时排出导致阻塞,引起皮脂腺增生,乳头部位表现出小肉粒。长期肉粒物质堆积会形成炎症,严重时可能形成肉瘤。
3.乳腺纤维瘤:这是一种乳腺良性病变,通常是由于内分泌紊乱和乳腺腺体结构改变引起。在孕期阶段,乳腺管在发育,有时会形成小肉粒状物质。
在怀孕期间,乳房上的肉瘤需要关注和治疗。如果肉瘤较小、无异常表现,可以在医生的指导下观察;如果肉瘤较大、生长迅速或伴有疼痛、瘙痒等异常表现,建议及时就医进行详细检查和治疗,以免影响胎儿哺乳或乳腺健康。
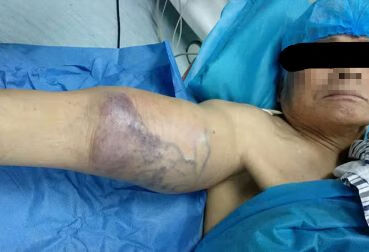
75岁的朱爷爷,发现右上臂肿胀10余年,摸摸里面有一个包块,只是不痛不痒,于是朱爷爷也从来没有去医院看过。但是最近包块增大得非常明显,导致现在朱爷爷手臂发麻,胀痛感非常明显,晚上都已经睡不着觉了。

这个时候朱爷爷才想到来医院看病,他也才把这个事情告诉两个儿子。儿子们很孝顺,带着朱爷爷看了好几家医院。无奈朱爷爷的身体条件很不好,有严重的肺气肿及哮喘,氧分压只有60mmHg,经评估后确实不具备全麻及手术的条件,而局麻根本完不成手术,各家医院都在打退堂鼓。但是矛盾的是如果不做手术,病人实在是疼痛难忍,即使是最强力的止痛药,已经毫无作用,他和两个儿子甚至要求截肢。

于是经朋友介绍,家属找到了南京医科大学第二附属医院骨科的王国栋主任,王主任介绍说:从患者的症状及影像学的资料来看,患者的肿瘤考虑为恶性,恶性肿瘤周围血管非常丰富,没有完整的界限,术中需要注意保护神经血管,分离肿瘤耗时较多,失血较多,虽然困难,但是手术切除肿瘤本身不是最大的问题,只是怕患者身体条件不行,耐受不了麻醉及手术创伤失血。

由于患者和家属的强烈要求,王主任给患者积极进行术前准备,他说如果他再不争取,病人已经没有治疗的机会了,这种病人就应该放宽适应症。但是,放宽适应症不是说随便乱手术,必须制定好完备的手术方案。首先将病人转到了呼吸科,进行肺部的正规治疗,同时做右上肢的血管造影及CT检查。

检查提示肿瘤周围血管丰富,王主任请医院的介入科,用微创的办法将肿瘤周围的血管先堵掉,以减少术中的出血。然后术中切取了一部分组织送快速的病理检查,结果提示是恶性的肉瘤,能保住肢体尽量不截肢,王主任继续迎难而上。可喜的是,肿瘤全部切除,历时2个小时,患者苏醒后也成功返回病房。目前病情稳定,术后恢复的非常不错。

什么是肉瘤?
肉瘤是一种恶性肿瘤,来源于间叶组织(包括结缔组织和肌肉),多发生于皮肤、皮下、骨膜及长骨两端。有骨肉瘤、平滑肌瘤、淋巴肉瘤、滑膜肉瘤等,其发展快,恶性程度普遍较高,早期即可发生血行转移,治疗手段也复杂,治愈难度大。有肿胀、疼痛等临床表现,也可见病理性骨折。
怎么诊断?
肉瘤的诊断“金标准”是:病理检查。
X线检查、CT扫描、MRI检查,骨扫描检查等可作为初步诊断的依据。
怎么治疗?
手术治疗:主要是涉及需要不需要截肢。
放疗:根据情况可以考虑采取局部放疗,但有效率并不高。
化疗:术前、术后可以进行化疗,提高生存率。
其他:中医等其他治疗方法及对症处理。
王国栋主任最后还介绍:朱爷爷后续可能还要根据正式的病理报告结果,选择是否进行放化疗,但是放化疗都有其副作用,到时候还需要重新评估朱爷爷的身体情况。
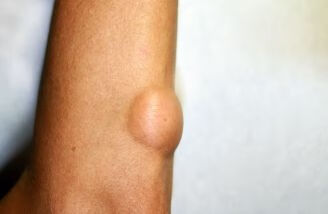
骨与软组织肉瘤发病率较低,人们对其认识不足,很多肢体肉瘤患者就诊时肿瘤体积已经长得很大,临床诊断已是局部晚期,其中一部分患者在接受全身化疗后肿瘤仍然进展体积进一步增大,这些患者往往面临截肢的风险,极大影响了患者的生存质量。其次很多发生在颌面部的骨与软组织肉瘤患者在初次手术时往往很难达到R0切除,局部复发风险高,二次手术创伤大,面临毁容风险,对患者的心理造成很大的创伤。所以在肉瘤治疗过程中,要以人为本,既要追求生存时间也要追求生活质量, 降低复发, 保肢和保容貌已经成为提高肉瘤患者生存质量最重要的努力方向。
1.介入治疗的原理:选择股动脉或桡动脉进行穿刺,将微导管超选择性插入到骨与软组织肉瘤供血靶动脉后,进行局部灌注抗肿瘤药物,极大地提高病灶局部的血药浓度从而提升抗肿瘤效果,然后注入合适的栓塞剂,阻断肿瘤滋养动脉的血供,引起肿瘤组织的缺血坏死,同时改变了肿瘤的微环境利于肿瘤细胞抗原的释放,可能有利于肿瘤免疫的激活。或者可以直接使用荷载抗肿瘤药物的载药微球进行栓塞可起到持续释放药物的栓塞作用,使局部的药物浓度维持更久。
2.介入治疗的优点:(1)对于局部晚期肢体肉瘤,术前行介入治疗±术前全身治疗,可以缩小肿瘤体积,利于肿瘤完整切除(R0)并达到理想的安全外科边界, 降低局部复发,提高保肢率。(2)对于颌面部肉瘤,术前介入±术前全身治疗,可以缩小肿瘤体积,消灭一些肉眼看不见的局部卫星转移病灶,明显提高R0切除率, 降低复发风险,减少毁容风险。(3)对于局部复发的肉瘤或发生寡转移的肉瘤病灶,行介入治疗±其他全身治疗,缩小复发/寡转移病灶,可以为二次R0切除复发/寡转移病灶创造机会。(4)TACE可以缓解部分肉瘤患者的局部疼痛,减少术中出血量,减少手术时间,诱导肿瘤周边形成假包膜便于手术切除,从而降低手术风险。
3.介入治疗前准备工作:评估患者的全身病情,排除介入禁忌症,一般需要患者具有良好的体力评分0-2分,血常规、肝肾功能、凝血功能无明显异常,心电图无明显异常,无造影剂过敏史,无动脉疾病(动脉炎,动脉狭窄、动脉闭塞,动脉斑块形成,明显动静脉畸形)等。完善病灶部位的磁共振(MR)或CT灌注成像、血管彩超,初步评估肿瘤的血供情况,具体的肿瘤血供情况需要术中在DSA下血管造影实时动态查看。
4.介入术后常见不良反应:部分病人出现一过性发热,主要考虑与肿瘤坏死释放致热源有关,病灶部位出现一过性酸胀疼痛,考虑与肿瘤发生坏死诱发炎性水肿有关,可以使用止痛药物或脱水对症处理,部分病人出现恶心呕吐,主要为化疗药物不良反应,通过止吐对症处理即可。部分病人在栓塞病灶部位的皮肤有一过性发红及灼热感,辅以局部冷敷,外涂尤卓尔炉甘石洗剂。一般术后2-3天逐渐改善。
5.介入治疗的疗程:具体要根据患者治疗的反应,有的患者只做了一次介入治疗,就产生肿瘤明显坏死和缩小。有部分患者肿瘤偏大,为了避免产生严重的不良反应,需要酌情分次进行介入治疗,才能到达理想效果。平均1-3次介入治疗基本能够看到理想的治疗效果。每次住院介入治疗,一般平均需要3天,两次介入的时间间隔一般在10-14天左右。
本中心介入成功病例分享 :
本中心依托上海市第六人民医院骨科(国家临床重点专科)和介入影像科(国家临床重点专科)两大平台,在复杂和疑难骨与软组织肉瘤诊治方面具有丰富的临床经验,也是国内最早开展骨与软组织肉瘤诊治的中心之一 。
(1) 右股骨骨肉瘤 介入治疗前后对比 :
介入前右侧股骨骨质破坏伴巨大软组织肿块形成,介入治疗后软组织肿块 强化明显减弱 ,并发生坏死,患者最后成功实现了保肢:
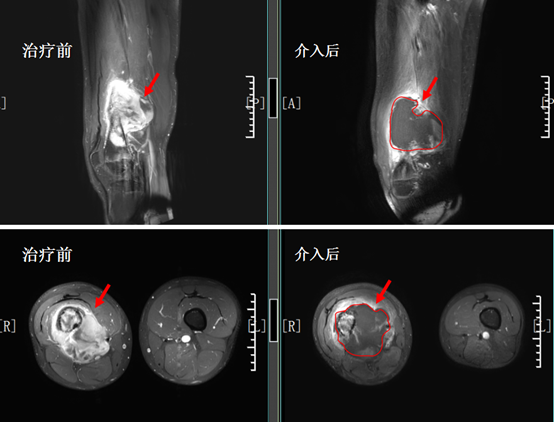
(2) 下颌骨骨肉瘤 介入治疗前后对比:
介入前左侧下颌骨骨质破坏伴软组织肿块形成,介入治疗后软组织肿块强化明显减弱,发生 坏死伴空洞形成 ,该患者目前已经在颌面外科R0切除:
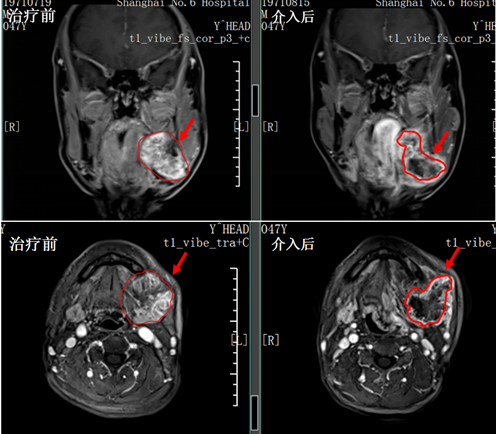
(3)左大腿 脂肪肉瘤 复发病灶介入治疗:
介入治疗后病灶发生 坏死形成空洞,肿块体积也变小 ,该患者目前已经至外科二次R0切除。
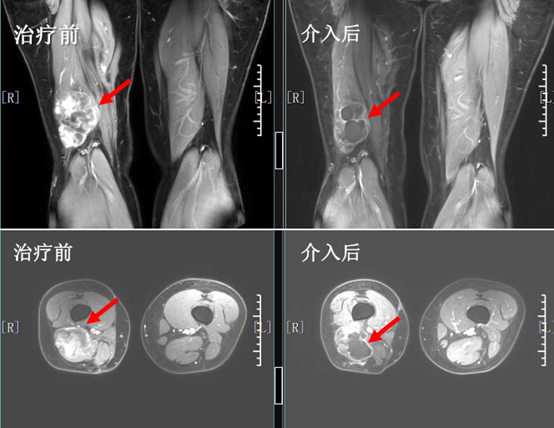
(4)左侧髋部 侵袭性纤维瘤病 复发病灶介入治疗:
介入治疗后病灶中央发生明显 坏死形成空洞 ,如下图所示
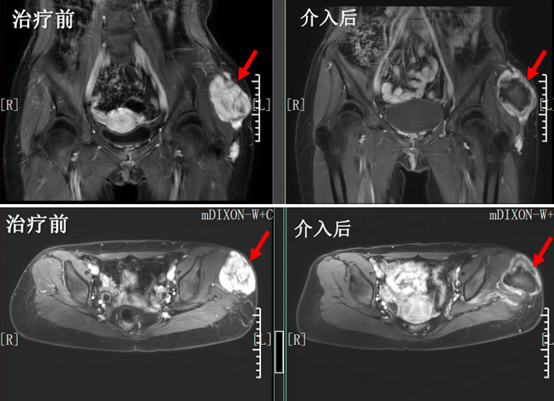
就医信息:
上海交通大学附属第六人民医院是国内最早开展骨和软组织肉瘤诊治的临床中心之一,每年诊治的复杂和疑难骨与软组织肉瘤病例数量位居全国前三位,如果有肉瘤介入治疗方面需求,可以通过京东医生平台咨询我或请至于上海交通大学附属第六人民医院当面咨询,地点:上海市宜山路600号。
世上行路本艰难,人生漫长孰能无病,但有家人,朋友和医护的共同陪伴,请坚信我们一定能够乘长风破万里浪,高挂云帆在沧海中勇往前行,
请为你爱的人和爱你的人加油!!!
当地时间9月12日,FDA批准首个皮下注射抗PD1免疫疗法,用于特定类型肺癌、肝癌、黑色素瘤、软组织癌。这个皮下疗法组合包括两部分组成:一部分是阿替利珠单抗;另一个是 Halozyme公司自己研制的重组人透明质酸酶rHuPH20[1]。
皮下疗法应用Halozyme的ENHANZE药物递送技术,可将原本30mim的静注时间缩短为7min。让我们一起来看支撑这项研究背后的临床试验结果。
相似的血药浓度、有效性和安全性
该获批基于一项随机多中心 Ib/III 期的试验,研究的主要目的要看看阿替利珠单抗这个药,打在皮下和打在静脉里在一些特定患者身上效果有什么不一样。这些特定患者为局部晚期或者已经转移的非小细胞肺癌患者,他们之前没做过癌症免疫治疗,而且之前用含铂类的药治疗也没效果。
试验的主要结果显示,皮下注射atezolizumab和静脉注射 atezolizumab 的几何平均比值 (GMR) 为1.05 (90% CI,0.88-1.24),AUC 0-21 天为 0.87 (90% CI,0.83-0.92),这表明皮下注射可以达静脉注射相当的血药浓度。有效性方面,皮下和静脉的总缓解率 (ORR) 、无进展生存期 (PFS) 和总生存期 (OS) 数据相似[2]。
安全性方面,最常见的任何级别不良反应是疲劳、肌肉骨骼疼痛、咳嗽、呼吸困难和食欲下降。
关于阿替利珠单抗
根据FDA获批信息,该药适应证如下,本次的获批主要是制剂类型的不同。
适应证[3]
1. 非小细胞肺癌(NSCLC):
- 单药用于经手术及含铂化疗后的Ⅱ至ⅢA期NSCLC成人患者辅助治疗(肿瘤细胞PD-L1表达≥1%)。
- 单药一线治疗高表达PD-L1、无EGFR或ALK畸变的转移性NSCLC成人患者。
- 与贝伐珠单抗等联合用于无EGFR或ALK畸变的转移性非鳞状NSCLC成人患者一线治疗。
- 单药治疗含铂化疗期间或后进展的转移性NSCLC成人患者(有EGFR或ALK畸变患者应在对应FDA批准疗法进展后使用)。
2. 小细胞肺癌(SCLC):与卡铂和依托泊苷联合用于广泛期SCLC成人患者一线治疗。
3. 肝细胞癌(HCC):与贝伐珠单抗联合用于未接受全身治疗的不可切除或转移性HCC成人患者。
4. 黑色素瘤:与考比替尼和维莫非尼联合用于BRAF V600突变阳性的不可切除或转移性黑色素瘤成人患者。
5. 肺泡软组织肉瘤(ASPS):单药用于2岁及以上不可切除或转移性ASPS成人及儿童患者。
关于Halozyme[4]
Halozyme 是一家生物制药公司,致力于提供颠覆性解决方案,以改善新兴和成熟疗法的患者体验和结果。作为采用专有酶 rHuPH20 的 ENHANZE药物输送技术的创新者,Halozyme 经过商业验证的解决方案用于促进注射药物和液体的皮下输送,目的是通过快速皮下输送和减轻治疗负担来改善患者体验。
Halozyme 已在全球 100 多个市场的 8 种商业化产品中触及超过 800,000名患者的上市后使用,其 ENHANZE技术已授权给领先的制药和生物技术公司,包括罗氏、武田、辉瑞、杨森、艾伯维、礼来等。
参考文献:
1.Halozyme Announces FDA Approval of Roche's Tecentriq Hybreza™ With ENHANZE® for Multiple Types of Cancer
2.FDA Approves Subcutaneous Atezolizumab and Hyaluronidase-tqjs for Use in All Indications of IV Atezolizumab
3.Product information:.TECENTRIQ- atezolizumab injection, solution
4.https://ir.halozyme.com/news/news-details/2024/Halozyme-Announces-FDA-Approval-of-Roches-Tecentriq-Hybreza-With-ENHANZE-for-Multiple-Types-of-Cancer/default.aspx

2024年9月10日,诺和诺德一项减肥研究登顶《新英格兰医学杂志(NEJM)》,公布了胰高血糖素样肽-1(GLP-1)受体激动剂利拉鲁肽在儿童中的减重数据:利拉鲁肽组近一半参与者BMI降低 5%以上。让我们一起来看看这项儿童减肥药的研究。
火锅烤肉、奶茶饮料等诱惑层出不穷,让不做选择的成年人慢慢走上了肥胖之路。而我们祖国的花朵,面对这些,也茁壮成长成了“小胖子”。据统计,我国6~17岁、6岁以下儿童和青少年超重/肥胖率分别达到19.0%和10.4%[1]。
孩子肥胖与很多疾病息息相关,如2型糖尿病、脂肪性肝炎、多种癌症。除了引导健康饮食和规律的生活方式[2],一些药物选择对于超重儿童提供了选择。
虽然经常提到司美格鲁肽、利拉鲁肽,但是其在儿童中的安全性一直引人担忧,于是就有了NEJM这个研究。这个研究是一项双盲随机对照试验。试验分为利拉鲁肽组和对照组,参与者每日一次注射药物,在4-5周内每周剂量递增,直至达到最终剂量[3]。试验有效性结果主要看参与者BMI变化百分比。
共有 82 名参与者接受了随机分组;56 人被分配至利拉鲁肽组,26 人被分配至安慰剂组。
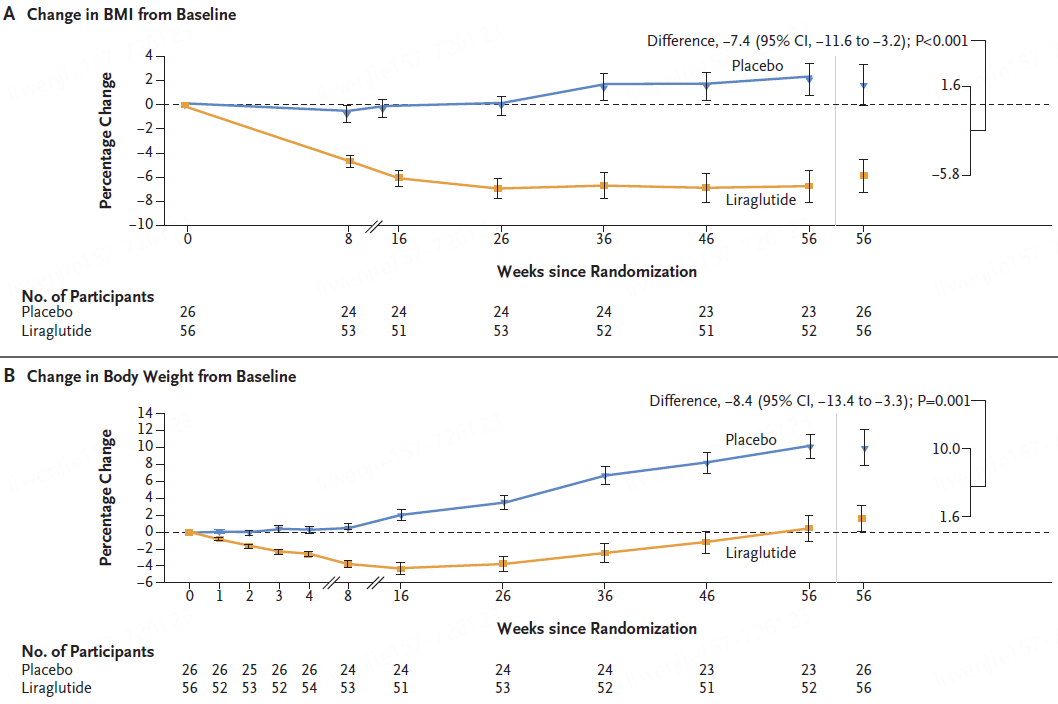
试验结果表明,在第 56 周时,利拉鲁肽组BMI较基线的平均变化百分比为 - 5.8%,安慰剂组为 1.6%。
利拉鲁肽组体重的平均变化百分比为 1.6%,安慰剂组为 10.0%。
利拉鲁肽组46%的参与者BMI降低至少5%,而安慰剂组为 9%(调整后的优势比为 6.3 [95% CI,1.4 至 28.8];P = 0.02)。
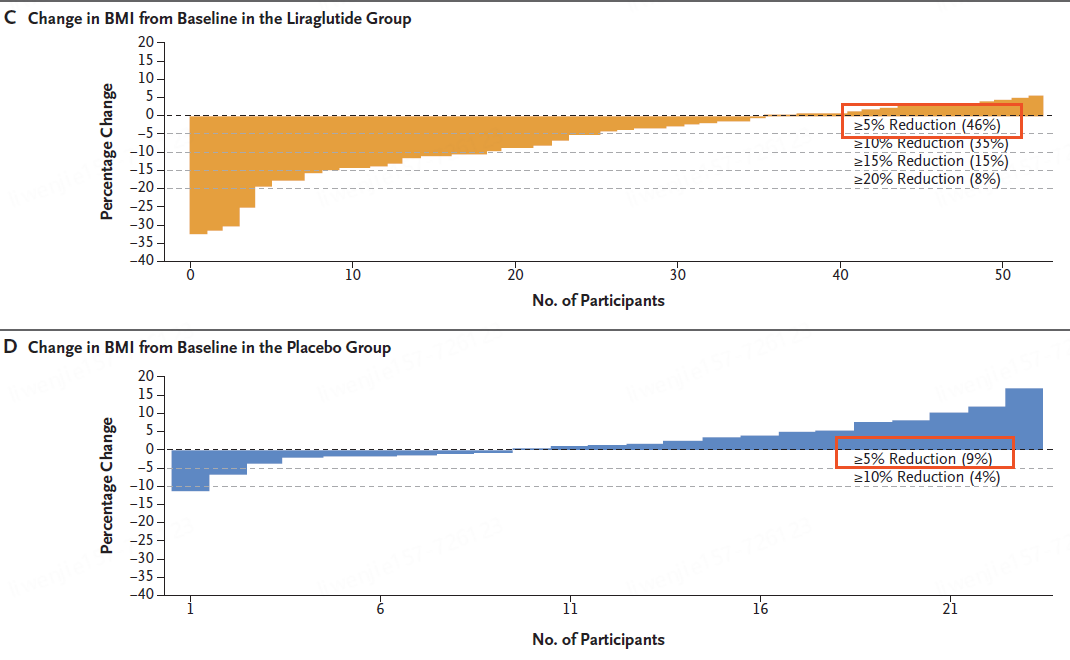
利拉鲁肽组和安慰剂组分别有 89% 和 88% 的参与者发生不良事件。胃肠道不良事件在利拉鲁肽组更为常见(80% vs 54%);利拉鲁肽组和安慰剂组分别有 12% 和 8% 的参与者报告了严重不良事件。
关于利拉鲁肽
利拉鲁肽(VICTOZA)的已获批适应症包括:
作为饮食和运动的辅助手段,用于改善 10 岁及以上成人和儿童 2 型糖尿病患者的血糖控制。
降低已确诊心血管疾病的成人 2 型糖尿病患者发生主要不良心血管事件(心血管死亡、非致命性心肌梗死或非致命性中风)的风险。
说明书也也发布了黑框警告信息:
本品禁用于有甲状腺髓样癌个人或家族史的患者以及患有 2 型多发性内分泌腺瘤综合征(MEN 2)的患者。应告知患者使用本品可能存在的甲状腺髓样癌风险,甲状腺肿瘤的症状包括颈部肿块、吞咽困难、呼吸困难、持续性声音嘶哑。
关于诺和诺德[5]
诺和诺德是一家全球领先的医疗保健公司,成立于1923年,总部位于丹麦。其的宗旨是在糖尿病领域的传统基础上,推动变革以战胜严重的慢性疾病。诺和诺德通过开创科学突破、扩大药品的可及性以及致力于预防并最终治愈疾病来实现这一目标。诺和诺德在80个国家拥有约 69,000名员工,产品在大约170个国家销售。
参考文献:
1.中国超重/肥胖医学营养治疗指南(2021)
2.Fox CK, Barrientos-Pérez M, Bomberg EM, Dcruz J, Gies I, Harder-Lauridsen NM, Jalaludin MY, Sahu K, Weimers P, Zueger T, Arslanian S; SCALE Kids Trial Group. Liraglutide for Children 6 to <12 Years of Age with Obesity - A Randomized Trial. N Engl J Med. 2024 Sep 10. doi: 10.1056/NEJMoa2407379. Epub ahead of print. PMID: 39258838.
3.SCALE KIDS: Research Study to Look at How Well a New Medicine is at Lowering Weight in Children With Obesity
4.Product information:VICTOZA- liraglutide injection
5.https://www.novonordisk.com/

在 2024 年世界肺癌大会上,一项关于局部晚期或转移性 ROS1 阳性非小细胞肺癌(NSCLC)的试验公布了数据,这是一项多中心Ⅱ期试验,试验药物是新一代酪氨酸激酶抑制剂(ROS1 TKI)taletrectinib,在试验中的代码是AB - 106[1]。
总体缓解率达85.2%,亚洲患者达87.9%
试验的主要结果是客观缓解率(ORR),最长时间为 4 年,入组患者根据既往接收ROS1 TKI治疗的情况分为两组,一组既往胃接受,另外一组接受过[2]。从试验的结果来看,未接收过这类药物治疗ORR比例更好,达85.2%。详细数据如下所示:
- 先前未接受过 ROS1 TKI 治疗的患者(n = 54),经过中位随访 15.8 个月(范围 3.6 - 29.8),taletrectinib 展现出了较好疗效,确认总体缓解率(cORR)高达 85.2%(95%CI,72.88% - 93.38%)。值得一提的是,亚洲患者(n = 33)与非亚洲地区患者的 cORR 相近,分别为 87.9%(95%,71.80% - 96.60%)和 81.0%(95%CI,58.09% - 94.55%)。
- 先前接受过 ROS1 TKI 治疗的患者中(n = 47),中位随访 15.7 个月(范围 3.9 - 29.8),taletrectinib 的 cORR 也达到了 61.7%(95%CI,46.38% - 75.49%)。亚洲患者(n = 21)与其他地区患者(n = 26)的 cORR 分别为 57.1%(95%CI,34.02% - 78.18%)和 65.4%(95%,44.33% - 62.79%)。
- 在基线时有可测量脑转移的患者中,评估颅内反应显示,初治组(n = 9)的颅内客观缓解率(IC - ORR)为 66.7%(95%CI,29.93% - 92.51%),其中完全缓解(CR)率为 22.2%,部分缓解(PR)率为 44.4%[1]。
最常见不良反应为肝药酶升高
导致剂量减少的治疗出现的不良事件(TEAEs)发生在 37.1%的患者中,其中 16.4%是由于肝酶升高。导致治疗中断的 TEAEs 报告在 7.5%的患者中;其中 1.3%被认为与治疗相关。没有报告导致死亡的 TEAEs。
其他不良反应发生率如下:
- 至少 15%的患者(n = 159)中最常见的 TEAEs 是丙氨酸氨基转移酶升高(任何级别,67.9%;≥3 级,15.1%),天冬氨酸氨基转移酶升高(67.3%;6.9%),腹泻(56.6%;0.6%),恶心(51.6%;1.9%),呕吐(33.3%;1.3%),便秘(25.2%;0.0%),贫血(20.1%;4.4%),味觉障碍(19.5%;0.0%),血肌酸磷酸激酶升高(18.2%;3.8%),头晕(17.0%;0.0%)和 QT 延长(15.1%;3.1%)[2]。
Taletrectinib是何许药物?
最后再回到taletrectinib,这个药作为新一代 ROS1 TKI 药物,在TRUST - II 试验中表现确实亮眼。
由于对 ROS1+肿瘤有着更高的效力,taltrectinib 能够提升患者无进展生存期(PFS),同时这个药物的中枢神经系统(CNS)渗透率也更高,药理机制上,可以有选择性地抑制 ROS1 野生型以及其对 TRKB 的耐药突变;与其他 ROS1+抑制剂相比,taltrectinib 的安全性更优,并且与中枢神经系统相关的不良事件(AE)极少[3]。
参考文献
1.Taletrectinib Shows Consistent Efficacy, Safety in ROS1+ NSCLC Independent of Prior TKI Exposure
2.Taletrectinib Phase 2 Global Study in ROS1 Positive NSCLC (TRUST-II)
3.Nagasaka M, Brazel D, Ou SI. Taletrectinib for the treatment ofROS-1positive non-small cell lung cancer: a drug evaluation of phase I and II data. Expert Opin Investig Drugs. 2024 Feb;33(2):79-84. doi: 10.1080/13543784.2024.2305131. Epub 2024 Jan 29. PMID: 38224083.

近期Merck宣布其正在进行的IDeate-Lung01 Ⅱ 期试验结果积极,试验主角ifinatamab deruxtecan(I-DXd)用于治疗广泛期小细胞肺癌(ES-SCLC),在入组患者中,12mg/kg I-DXd 1的客观缓解率(ORR)为 54.8%[1]。

IDeate-Lung01是一个多中心随机开放研究,主要结果:在广泛期小细胞肺癌(ES-SCLC)患者中,使用I-DXd治疗后的客观缓解率(ORR)百分比,试验最长约 36 个月[2]。
这里的客观缓解率就是在参与试验的人中,达到最佳总体缓解的人所占的百分比,“总体缓解”指的是经确认的完全缓解或者部分缓解。对于所有的靶病灶、非靶病灶和新出现的病灶来说,完全缓解就是所有的病灶都消失了;部分缓解就是所有病灶直径的总和至少减少了 30%。
疾病控制率高达90.5%,客观缓释率达54.8%
经盲态独立中心审查(BICR)评估,在接受I-DXd治疗的广泛期小细胞肺癌患者中,12mg/kg 队列(n = 42)的确认客观缓解率(ORR)为 54.8%(95%置信区间:38.7 - 70.2),8mg/kg 队列(n = 46)为 26.1%(95%置信区间:14.3 - 41.1)[1]。

在 12mg/kg 队列中观察到 23 个部分缓解(PR)。在 8mg/kg 队列中观察到 1 个完全缓解(CR)和 11 个部分缓解。
在 12mg/kg 和 8mg/kg 队列中,分别观察到中位缓解持续时间(DoR)为 4.2 个月(95%置信区间:3.5 - 7.0)和 7.9 个月(95%置信区间:4.1 - 未确定),疾病控制率(DCR)为 90.5%(95%置信区间:77.4 - 97.3)和 80.4%(95%置信区间:66.1 - 90.6)。
12mg/kg 剂量的中位治疗持续时间为 4.7 个月(0.03 - 15.2),8mg/kg 剂量为 3.5 个月(0.03 - 13.9)。在 12mg/kg 和 8mg/kg 队列中,分别观察到中位无进展生存期(PFS)为 5.5 个月(95%置信区间:4.2 - 6.7)和 4.2 个月(95%置信区间:2.8 - 5.6),中位总生存期(OS)为 11.8 个月(95%置信区间:8.9 - 15.3)和 9.4 个月(95%置信区间:7.8 - 15.9)。
12mg/kg 剂量已被选定用于试验的剂量第二部分。截至 2024 年 4 月数据截止时,12mg/kg 队列的中位随访时间为 15.3 个月(95%置信区间:13.6 - 16.2),8mg/kg 队列为 14.6 个月(95%置信区间:13.4 - 16.5)。 在有脑靶病灶的患者中,经中枢神经系统(CNS)BICR 评估,在 12mg/kg 队列(n = 10)和 8mg/kg 队列(n = 6)中分别观察到颅内客观缓解率为 50.0%(95%置信区间:18.7 - 81.3)和 66.7%(95%置信区间:22.3 - 95.7)。在这些患者中,每个队列中均观察到两个颅内完全缓解。
安全性数据
12mg/kg 队列中 50.0% 患者发生 3 级或更高等级治疗中出现的不良事件,8mg/kg 队列中 对应比例达43.5% 。两种剂量下常见治疗相关不良事件有恶心、食欲下降、贫血、中性粒细胞减少、白细胞减少和乏力等。
12mg/kg 和 8mg/kg 剂量下分别有五例和四例间质性肺病、肺炎事件被确认为与治疗相关,多数为低级别。12mg/kg 和 8mg/kg 队列中因不良事件导致的治疗中断分别为 16.7% 和 6.5%。
关于I-Dxd
I-Dxd是一种首创 B7-H3 靶向抗体药物偶联物(ADC),与第一三共开发的其他抗体药物偶联物(一样,向癌细胞递送相同的毒性有效载荷。I-Dxd靶向一种B7-H3 的蛋白质,该蛋白质在包括前列腺癌和食管癌在内的多种癌症中过度表达[3]。
参考来源:
1.Ifinatamab Deruxtecan Continues to Demonstrate Promising Objective Response Rates in Patients with Extensive-Stage Small Cell Lung Cancer in IDeate-Lung01 Phase 2 Trial
2.Ifinatamab Deruxtecan (I-DXd) in Subjects With Pretreated Extensive-Stage Small Cell Lung Cancer (ES-SCLC) (IDeate-Lung01)
3.Merck, Daiichi Sankyo detail Phase 2 ADC results in small cell lung cancer, bispecific combo strategy

2024年9月5日,Vor Bio公布了其1/2 期 VBP101 试验的临床数据,VBP101主要评估干细胞疗法 tremtelectogene empogeditemcel(trem - cel)与 CD33 靶向抗体偶联药物(ADC)Mylotarg 联用用于治疗复发/难治性急性髓系白血病(AML)患者的效果[1]。
干细胞移植后白血病复发风险
虽然患者进行了造血干细胞移植(HCT),但高风险急性髓系白血病(AML)和骨髓增生异常综合征(MDS)仍经常复发。HCT后的靶向治疗可减少复发,但会对植入细胞产生毒性限制。
VOR33 是一种异基因 CRISPR/Cas9 基因组编辑的造血干细胞和祖细胞(HSPC)治疗产品,缺乏 CD33 蛋白,这个试验正是对 HCT 后复发风险高的 CD33 + AML 或 MDS 患者进行研究,以便在 HCT 后使用 Mylotar靶向残留的 CD33 + 急性 AML 细胞,从而避免对植入的 VOR33 细胞产生毒性。
参与者将接受HCT植入,植入后将接受 Mylotarg治疗,治疗周期≤4个周期。评估 VOR33 安全性的主要终点是 28 天成功植入的发生率。研究将首先评估递增 Mylotarg剂量水平的安全性,以确定最大耐受剂量(MTD)和推荐的 2 期剂量(RP2D)。后续将进一步扩大参与者数量,以评估 Mylotarg的 RP2D[2]。
100%植入,无复发生存期改善
公布的数据包括 18 名接受 trem - cel 治疗的患者,截至 2024 年 7 月 19 日的数据截止日期,其中 10 名患者接受了 Mylotarg 治疗。详细数据如下[1]:
可靠的植入效果:100% 的患者实现了初级中性粒细胞植入(中位时间为 9 天)和强劲的血小板恢复(中位时间为 16.5 天)。在第 28 天,CD33 编辑效率高(中位数为 89%,范围为 71 - 94%),并且实现了完全的髓系嵌合。
血液系统的屏障:不同 Mylotarg 剂量( 0.5、1和 2mg/平方米)下,中性粒细胞和血小板计数保持稳定。
Mylotarg 治疗指数的拓宽:药物暴露由 AUC 表示,与疗效相关,与标记的 Mylotarg 剂量一致;最大浓度由 Cmax 远低于已知的毒性范围。
早期证据表明患者受益:与已发表的高危 AML 对照者相比,在无复发生存期方面,患者受益。
VBP301 研究将继续招募患者,继续关注其试验目的。预计今年年底,Vor Bio计划与FDA讨论trem - cel与Mylotarg联合用药的关键试验设计。
Vor Bio 是一家扔处于临床阶段的细胞和基因组工程公司,其多条管线扔处于临床研究阶段(详见图片),旨在通过对造血干细胞进行工程改造,使移植后的靶向治疗成为可能,从而改变血癌患者的护理标准。
参考文献:
1.New Clinical Data Validates Vor Bio’s Approach of Using Shielded Transplants to Deliver Targeted Therapies
2.Allogeneic Engineered Hematopoietic Stem Cell Transplant (HCT) Lacking the CD33 Protein, and Post-HCT Treatment With Mylotarg, for Patients With CD33+ AML or MDS
展开更多