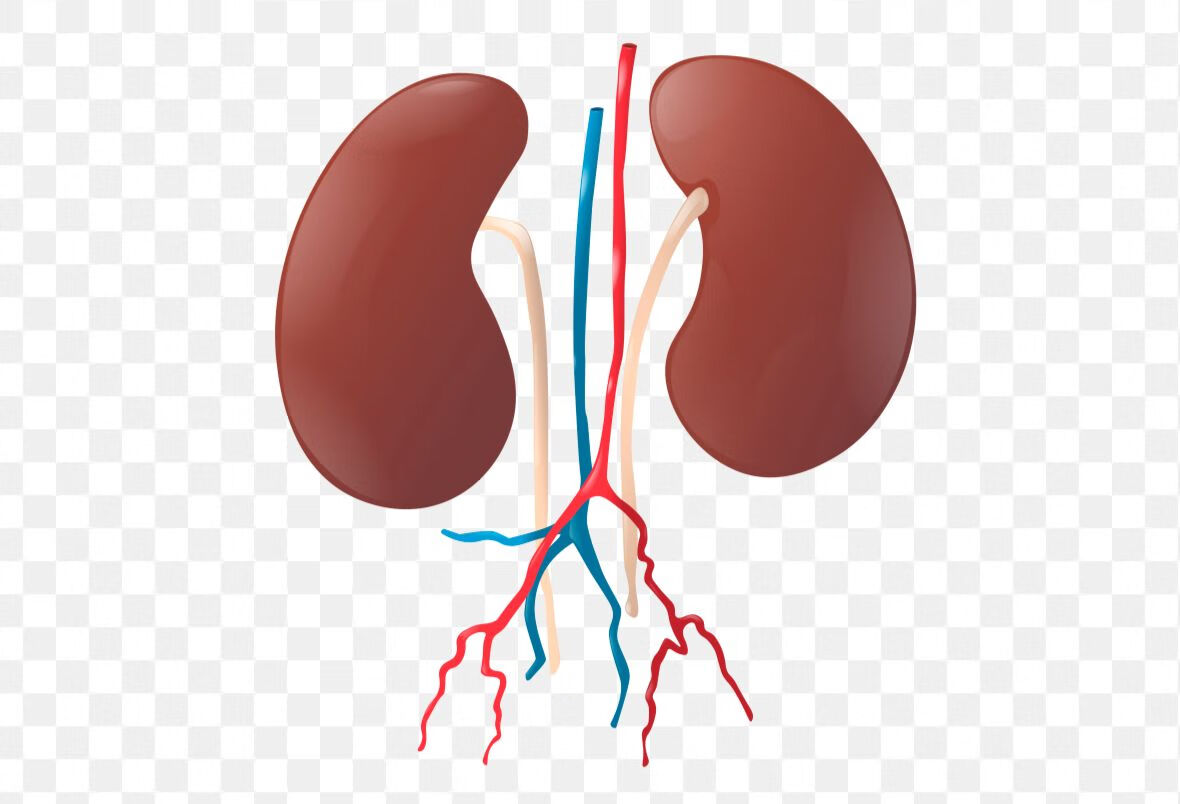
1. 肾上腺为什么会长肿瘤
- 1.1 作为内分泌器官,长肿瘤有两个因素:
- 第一是自己长,就是说肾上腺本身出现问题,长肿瘤,这种叫做原发性的肾上腺肿瘤。
- 第二有时肾上腺本身不想长肿瘤,但是有人刺激它,让他长,是谁么?那就是要搞清楚谁在控制这个肾上腺。
- 1.2 第三是其他肿瘤转移过来的,比如肺部,乳腺,结肠,肝,等。
2. 肾上腺长肿瘤需要怎么处理?
- 2.1 肾上腺肿瘤的检出率那么高,是不是每个人都有症状,都需要处理,都需要手术?
- 2.2 首先需要搞清楚肾上腺肿瘤是否有功能。
- 2.3 目前的检验指标显示是激素正常,那么是不是就没有功能么?
- 2.4 那么如果激素检测都是正常的,那么可以认为是没有功能的么?
- 2.5 对于有功能的肾上腺肿瘤,是否一定要手术治疗么?
- 2.6 对于无功能的肾上腺肿瘤,需要么处理么?
- 2.7 对于继发的肾上腺肿瘤,可以建议神经外科处理脑垂体,因此不急于处理肾上腺。
- 2.8 还有一种比较麻烦的就是两边都有肿瘤,都差不多,那么怎么办?
- 2.9 肾上腺其实很重要,如果人体没有肾上腺,又没有补充激素,会危及生命。
- 2.10 对于双侧肾上腺嗜铬细胞瘤,需要注意是不是一种叫 MEN 的综合症。
- 2.11 对于体检发现肾上腺肿物,血液学指标是正常,但又有高血压,但瘤子又很小,不像嗜铬细胞瘤,怎么办?
因此肾上腺肿瘤其实还是比较复杂的一个疾病,国外都是一个叫内分泌外科在处理,因为涉及内科和外科,因此比较复杂。
肾上腺肿瘤很高发,具体原因很多,有本身的,也有外在因素的。
治疗方面,一些可以观察,一些可以药物,一些可以外科治疗,但需要结合血液学指标,症状,患者的意愿,以及医生的经验,综合判断。

首先这两个激素升高要考虑很多因素,第一,单纯肥胖导致,库欣病,肾上腺的肿瘤,异位 ACTH 综合症。
异位 ACTH 是垂体外病变引起的双侧肾上腺皮质增生支气管肺癌尤其是燕麦细胞癌、甲状腺癌、胸腺癌、鼻咽癌及起源于神经嵴组织的肿瘤有时可分泌一种类似 ACTH 的物质,具有类似 ACTH 的生物效应,从而引起双侧肾上腺皮质增生,这一类患者常有明显的肌萎缩和低血钾症肿瘤多为恶性,预后往往不好,手术治疗后生存期也不久。
出现库欣综合征往往是皮质醇增多,出现向心性肥胖、皮肤菲薄、脸上各种小毳毛发生。单纯肥胖是皮质醇升高和或 ACTH 升高,但是皮质醇的节律不存在异常,以上所说的其他疾病都会影响皮质醇节律性,正常的节律性是早 8 点皮质醇是下午 16 点的 2 倍。
临床上,肾上腺疾病多见于内分泌科,最为常见的是肾上腺肿瘤,肾上腺癌或者是肾上腺皮质增生等等。肾上腺疾病对人体的危害很大,尤其是肾上腺肿瘤或者是肾上腺癌在治疗方面,多选择手术治疗!那么,对于手术切除肾上腺后会对人体有什么影响?是大家所关注的问题。今天我们就来讲一下,肾上腺切除后,对身体有什么影响?
肾上腺肿瘤可分为无功能腺瘤和有功能腺瘤。无功能腺瘤常常没有任何临床症状,多在体检中无意发现。有功能的肾上腺肿瘤根据分泌的激素不同可以分为皮质醇腺瘤、醛固酮腺瘤。
皮质醇腺瘤
皮质醇腺瘤分泌皮质激素增多引起的,常见的表现是向心性肥胖,满月脸、水牛背,胸腹颈背脂肪增多,皮肤菲薄,多血质,皮肤紫纹;痤疮、多毛、女性月经失调,男性阳痿;性欲减退,免疫力低下;骨质疏松,容易引起脊柱压缩性骨折;血压上升,心肌肥厚,心衰;情绪烦躁,甚至精神异常。
醛固酮腺瘤
醛固酮腺瘤主要表现为高血压,多为缓慢进展的良性高血压,一般降压药物效果不明显;低血钾,醛固酮有促进尿钾排泄的作用,常引起肌肉无力、周期性麻痹、手足搐弱,甚至吞咽和呼吸困难,心电图常有明显异常。血浆肾素活性减低,由于醛固酮分泌增多,体内肾素分泌受到抑制,引起血浆肾素活性减低。

肾上腺肿瘤的分类可按其性质分为良性肿瘤和恶性肿瘤;按有无内分泌功能分为非功能性肿瘤和功能性肿瘤;按发生部位分为皮质肿瘤、髓质肿瘤、间质瘤或转移瘤等。肾上腺的常见的肿瘤主要有无功能腺瘤、嗜铬细胞瘤、醛固酮瘤、肾上腺皮质腺瘤和皮质癌、转移瘤等;一般在发现肾上腺占位后,为了明确诊断需要完善常规检查:监测血压、心率、电解质、肾上腺皮质,髓质,垂体,下丘脑各项激素水平、增强CT或MRI等;对于双侧的肾上腺占位病变,若不能明确其内分泌功能,辅助性采用DSA下双侧肾上腺静脉采血分析有一定帮助。
肾上腺是体内重要的内分泌器官, 肾上腺髓质内不但可以得到肾上腺素,还可得到去甲肾上腺素、多巴胺,其副作用较肾上腺素为小,其升血压、救命的效果往往更好。
肾上腺皮质产生和分泌皮质激素可达40余种。皮质激素可分为三类:
1 调节糖和蛋白质代谢的激素—糠皮质激素 以皮质醇为代表,由束状带分泌,临床常用的为可的松。此类素可促进糖原异生作用,维持血糖的浓度。缺乏时易发生低血糖。过多时,糖原异生作用增强,可破坏蛋白质或阻止其合成,使人体皮下脂肪过度增加,血糖升高,皮肤变薄出现紫纹,肌无力,骨质疏松。此外,糖皮质激素对各种物质代谢都有影响,它与胰岛素、生长素、肾上腺髓质激素等一起来调节机体的物质代谢和能量供应,使体内的生理活动彼此协调和平衡。
2 调节盐和水代谢的激素—盐皮质激素 以醛固酮为代表,由球状带分泌,临床应用者为醋酸脱氧皮质酮。这种激素使肾曲管吸收钠和氯而排出钾和磷,缺乏这种激素,则血浆中钠的浓度降低,因而水分丢失,血液浓缩,同时血钾增高。这种激素过多,则情况相反,即血钠增高而钾降低。盐皮质激素对糖、蛋白质的代谢也可有一定作用,只是作用较轻。盐皮质激素的产生和分泌在生理状态下主要受肾素—血管紧张素系统的调节,其次是血钾、促肾上腺皮质激素等的影响。
3 性激素 肾上腺皮质还分泌较弱的雄性激素如胶氢表雄酮、雄烯二酮和微量的睾酮,由网状带分泌,对男女少年可促成其最早的第二性征如腋毛、阴毛的出现,以及下丘脑—垂体—性腺轴的成熟,从而使其青春期健康发育。肾上腺皮质还分泌微量的雌激素,一般无实际意义,但在肾上腺肿瘤病人,因其含量增加,可使男性患者出现阳萎、不育,女性患者出现月经失调。
2016年06月手术患者,女,76岁,苏州市人,主诉高血压二十年,体检发现双侧肾上腺占位两周,自述近期头晕乏力,血压波动较大,CT检查提示:双侧肾上腺可见长园性低密度影,右侧大小约3.8*3.5cm,左侧约2.5*2.0cm,其内可见脂质密度,增强可见明显强化,考虑肾上腺腺瘤;肾上腺功能检测提示皮质醇明显升高达33.26,遂考虑分期行腹腔镜下肾上腺肿瘤切除术。手术前充分准备达两周,监测各项激素水平、调整血压、心率、电解质平衡、血凝、血容量等各项指标。
第一次手术,术前CT双侧肾上腺占位

术前激素水平检测提示皮质醇偏高


病理报告提示右肾上腺腺瘤

3个月后,患者行第二次手术术前CT,右侧肾上腺术后改变,左侧肾上腺肿瘤较前次CT有所增大,达2.7*2.5cm,考虑腺瘤

术前监测激素水平,发现经过第一次手术切除右侧肾上腺腺瘤后效果明显,持续的高激素水平状态已经明显下降

充分游离左肾中上极,显露左肾上腺及腺瘤,必要时可显露肾脏动静脉,清晰显示中央静脉有助于减少对肾动静脉脉分支的损伤

离断中央静脉可减少肾上腺瘤体的渗血

完整切除左肾上腺腺瘤

双侧肾上腺肿瘤做手术时保留部分正常的肾上腺组织维持其少许内分泌功能,以生成生理量水平的激素。
利用医疗手套自制标本袋可降低医疗费用,完整切除左肾上腺腺瘤,腺体呈现金黄色,蛋黄状

围手术期部分肾上腺肿瘤患者电解质水平波动较大,如血钾,血钙等,应加强监测,积极补充

病理报告提示左侧肾上腺腺瘤


原发性醛固酮增多症 (PA)分型中特发性醛固酮增多症与醛固酮瘤最为常见(分别约70%、30%),而二者的治疗原则却截然不同。醛固酮瘤优先选择单侧手术切除,特发性醛固酮增多症则建议终生口服醛固酮受体阻断剂(安体舒通、依普利酮),鉴别二者的标准就是AVS。所以,AVS主要目的并非诊断,而在于鉴别单侧肾上腺醛固酮瘤与双侧肾上腺皮质增生。

2016年9月门诊患者,男性,43岁,湖州市人,自诉高血压三年,肢体无力持续低钾半年余,两周前不慎晕厥倒地,家属送其到外院体检发现右侧肾上腺外侧支占位1.2cm,遂来我院要求手术治疗,近期血钾最低时2.6mmol/l,头晕乏力,血压波动于160/95左右,长期服用波依定效果不佳,CT检查提示:右肾上腺可见一类园性软组织影,直径约1.2cm,增强后可见强化,考虑右肾上腺腺瘤;肾上腺功能检测提示醛固酮/肾素、醛固酮水平明显偏高,术前诊断为原发性醛固酮增多症,遂考虑行腹腔镜下右肾上腺肿瘤切除术。术前充分准备达一周,予以氯化钾、枸橼酸钾、安体舒通(螺内酯)术前调整血钾至4.07mmol/l。
术前CT提示右侧肾上腺占位,考虑腺瘤


患者术前低钾明显,血浆醛固酮/肾素活性比值ARR57.7-94.78≥40,提示醛固酮过多分泌为肾上腺自主性


充分游离右肾中上极,见右肾上腺及腺瘤紧贴下腔静脉及膈顶

该患者肾上腺腺瘤周围有一异位动脉分支,离断可见明显搏动性出血,顺利钳夹止血

阻断周围血供后,完整切除右肾上腺肿瘤

围手术期患者血钾波动较大,积极监测补充

术后病理报告符合术前肾上腺腺瘤诊断

原发性醛固酮增多症,是指肾上腺皮质分泌过量的醛固酮激素引起高血压,低血钾,低血浆肾素活性,和碱中毒为主要表现的临床综合征,又称Conn综合症,血浆醛固酮/肾素活性比值≥40,提示醛固酮过多分泌为肾上腺自主性,结合血浆醛固酮浓度大于20ng/dl,该比值是高血压患者中筛选原发性醛固酮增多症最可靠的方法。
2016年11月门诊患者,女,46岁,苏州市人,主诉高血压十年,肢体无力持续低钾两年余,两周前体检发现左侧肾上腺占位后来院要求手术治疗,自述近期血钾最低时2.2mmol/l,头晕乏力,血压波动于162/106左右,长期服用高血压药三联,效果不佳,CT检查提示:左肾上腺可见一园性低密度影,约2.2*2.0cm,考虑肾上腺腺瘤;肾上腺功能检测提示肾素、血管紧张素、醛固酮波动较大,术前初步诊断为原发性醛固酮增多症,遂考虑行腹腔镜下左肾上腺肿瘤切除术。术前充分准备达一周,血钾术前调整至4.8mmol/l。
术前CT提示左侧肾上腺占位,考虑腺瘤

术前激素水平检测提示低钾明显




充分游离左肾中上极,显露左肾上腺及腺瘤

游离左肾上腺及腺瘤,显露其内侧枝,寻找中央静脉是需清晰辨认,防止对肾动静脉脉分支的损伤,尤其避免误扎



对于正常的肾上腺组织需要保留部分,虽然增加了其复发风险,但需要维持肾上腺内分泌功能,以生成生理量水平的激素。

手术后患者血钾、血压、尿量波动均较大,经术前术后积极调整监测,逐步恢复正常。

病理报告提示左侧肾上腺腺瘤

2017年9月门诊女性患者,52岁,高血压一年,近期乏力,低钾表现,血钾3.34mmol/l,肾上腺功能检测提示醛固酮/肾素、醛固酮水平明显偏高,术前诊断为原发性醛固酮增多症,左肾上腺腺瘤,术前充分准备一周,调整血压、心率、电解质平衡等指标后行腹腔镜下右肾上腺肿瘤切除术。
CT提示右侧肾上腺肿瘤直径达2.5cm,考虑腺瘤


充分游离右肾中上极,显露左肾上腺腺瘤,呈蛋黄样改变

游离中央静脉后,完整切除肿瘤

2018年02月门诊患者,男,75岁,张家港市人,高血压三年,胸闷乏力两月余,一周前体检发现左侧肾上腺占位后来我院要求进一步治疗,血压波动于160/95左右,长期服用高血压药两联,CT检查提示:左肾上腺可见一园性低密度影,约2.0*2.0cm,考虑左肾上腺腺瘤;肾上腺功能检测提示肾素、血管紧张素、醛固酮正常,皮质醇明显升高,术前初步诊断为皮质醇增多症,遂考虑行腹腔镜下左肾上腺肿瘤切除术。术前充分准备达一周,术前术后予以补充激素。
术前CT提示左侧肾上腺占位,增强以后明显强化,考虑腺瘤,同时合并副脾。




术前检查提示皮质醇明显升高

术中发现左肾上腺腺瘤位置比较低,直视下被左肾脏上极阻隔,无法完全显示腺瘤。

完全游离左肾上极,增加可视空间

增加通道,下压肾脏,显露肿瘤

可见左肾上腺腺瘤位于肾上腺中下极

膈下滋养血管汇入肾上腺腺瘤

清晰显露左肾上腺中央静脉,并离断,完整切除左肾上腺腺瘤和部分肾上腺组织

完整取出手术标本,术后标本提示左肾上腺皮质腺瘤,符合术前诊断。


2018年04月门诊患者,男,52岁,吴江市人,低钾乏力十年,一直未予以重视,一周前体检发现双侧肾上腺占位后来我院要求进一步治疗,血压波动于150/90mmHg,血糖偏高,CT检查提示:左肾上腺区可见一强化占位,约3.6*3.0cm,考虑左肾上腺腺瘤,右肾上腺结节,不排除神经节细胞瘤可能;肾上腺功能检测提示肾素、血管紧张素、醛固酮正常,皮质醇明显偏高,血钾2.67mmol/l,术前初步诊断为左肾上腺腺瘤,皮质醇增多症,低钾血症,遂考虑行腹腔镜下左肾上腺肿瘤切除术。术前充分准备达一周,术前术后予以补钾和调整激素。术前CT提示左侧肾上腺占位,增强以后明显强化,考虑腺瘤,







肾上腺皮质癌(Adrenocortical carcinoma,ACC)是一种孤立的恶性肿瘤,ACC 是一种比较少见且具有高度侵袭性的恶性病变,发病率为0.7-2.0人/年·百万人。可发生于任何年龄,高峰年龄为40-50 岁,女性发病率稍高(55%-60%)。儿童的发病率高达0.27%,主要由于特异性 TP53 基因种系突变(R337H)。肾上腺皮质癌多为功能性,常表现女性男性化及肾上腺功能亢进,且易发生局部浸润和转移,如果有淋巴道和血道播散。
术前需要进行的实验室检查。包括基础血清皮质醇、促肾上腺皮质激素(ACTH)、17- 羟孕酮、雄烯二酮、睾酮、雌二醇、地塞米松抑制试验及尿游离皮质醇的测定。ACC 患者中约 80% 伴有激素自主分泌的特点。近些年常规采用的尿类固醇代谢产物分析有可能提高这一特点的检出率,且可作为监测早期复发的指标。
CT 基本可以在术前使大多数 ACC 患者得到正确的诊断。肿瘤体积一般较大,常在100g以上,偶可达1000g以上,呈侵袭性生长,境界不清,切面呈棕黄色或多色性,质较软,常有出血、坏死及囊性变; 肾上腺皮质癌直径多在5cm以上,部分大于11cm,而大多数腺瘤患者肿瘤体积小于 5cm。术前需要进行胸部 CT扫描,明确是否发生了肺转移。
肾上腺肿块活检的价值不大。一般用于患者发生肿瘤转移,失去了外科手术治疗的机会,或怀疑肾上腺肿物没有内分泌活性,且患者有肾上腺外恶性肿瘤的病史,细针穿刺活检,明确诊断。
手术是治疗非转移性ACC最有效的方法。开放性肾上腺切除术被认为是标准的 ACC 治疗方案,手术需完整切除肿瘤瘤体,包括清除周围脂肪组织和可疑受肿瘤侵犯的区域。皮质癌可向周围组织浸润,如肝、肾、脾脏、大血管、淋巴结等,甚至在腔静脉和右心房内生长形成瘤栓。开放手术肋缘下切口经腹途径是较理想的手术径路,因其暴露良好便于完整切除,可减少肿瘤组织溢出,并且有助于控制腔静脉、主动脉或肾蒂血管。腹腔镜手术不主张应用在治疗肾上腺皮质癌。因为其可能形成局部播散或造成肿瘤组织残留,仅在临床试验中报道过,最多是观察性研究的一部分。肾上腺皮质癌术后易复发,一般认为对于局灶性复发病灶也可再次行手术切除。皮质癌转移灶最多见于肺、肝脏和骨,手术治疗存活时间延长,并可缓解皮质醇过度分泌产生的症状。
ACC辅助治疗是非常有益的。目前的治疗方案包括米托坦、肿瘤局部放疗、细胞毒药物的应用,或者这些方案的联合应用。米托坦是唯一被批准用于终末期 ACC 患者中的药物。双氯苯二氯乙烷(O,P‐ODD)(米托坦)能改变肾上腺外皮质激素和雄激素代谢,抑制皮质激素分泌,破坏肾上腺皮质,使肿瘤缩小。适用于无法手术、术后肿瘤残留、有转移病灶的患者,属姑息性治疗。因此目前临床使用化疗药物多和双氯苯二氯乙烷联合应用。常用药物包括阿霉素、环磷酰胺、5‐氟尿嘧啶、顺铂、依托泊苷等。
射频消融治疗适用于无法手术的肾上腺皮质癌或其多发转移病灶,具有安全、微创等优点。缓解肿瘤局部症状并延长晚期皮质癌患者生存期。近年来采用介入治疗栓塞肿瘤供血动脉,术后肿瘤体积明显缩小,分泌功能降低,缓解了原发病灶引起的局部症状,提高了晚期肿瘤患者的生存质量。
肾上腺皮质癌预后总体不良,原因可能与不易早期诊断,一旦发现已近晚期,转移较早有关但总体来说,其5年生存率不超过35%~50%,多数2年左右。术后肾上腺癌复发比较常见,即使进行了肾上腺癌全切术,及时明确复发时间可以影响后续治疗方案。推荐每 3 个月进行一次影像学检查(胸部 CT 和腹部的 CT 或者 MRI), 同时联合检测血清皮质醇水平。

2017年01月门诊患者,男,45岁,盐城市人,体检发现右肾上腺区巨大占位两周余,来院要求手术治疗,自述无肢体乏力、头晕等明显不适,B超检查提示:右肾上腺可见一不规则椭圆型低密度影,约10.0*7.0*5.0cm,考虑右肾上腺肿瘤;肾上腺功能检测提示皮质醇明显偏高,肾素、血管紧张素、醛固酮正常,CT检查考虑肾上腺腺癌可能,结合皮质醇增高,术前诊断为肾上腺皮质癌,不排除肝癌,淋巴瘤,转移癌可能,决定行开放右肾上腺肿瘤切除术,术前考虑病情危重,积极联系ICU重症监护。术前CT提示右侧肾上腺巨大占位,考虑皮质癌,与肝脏黏连明显





术中发现右肾上腺肿瘤位置很高,肋缘下切口也无法显露肿瘤,仅能在肝下扪及肿瘤,充分抬起肝脏,游离下腔静脉,从肝脏脏面仔细剥离,分段切除肿瘤,肝脏面渗血明显,予以加压缝合,纱条填塞止血。

患者由于恶性肿瘤侵犯范围很大,累及肝脏,肾脏上极,下腔静脉血管壁,且凝血功能不佳,术后创面渗血明显,予以再次止血,DSA选择性栓塞治疗方控制出血,血色素一度下降至4.1g,血小板仅剩20,患者病情危重,在ICU重症监护室输注血制品12000ml,在泌尿外科、ICU、普外科、介入科等通力合作之下方才逐步控制病情。









2018年9月右肾上腺恶性肿瘤行手术治疗后,于2019年10月再次复发,而且进展迅速,预后不容乐观。





2017年04月门诊患者,女,55岁,苏州市人,主诉高血压十年,两周前体检发现左侧肾上腺占位后来院要求手术治疗,自述近年来出现头晕乏力,血压波动于185/110左右,长期服用高血压药三联,效果不佳,CT检查提示:左肾上腺可见一园性低密度影,约5.0*4.0*4.0cm,考虑左肾上腺腺瘤;肾上腺功能检测提示VMA明显增高,术前初步诊断为左肾上腺嗜铬细胞瘤,遂考虑行腹腔镜下左肾上腺肿瘤切除术。术前充分准备达两周,影像学提示左肾上腺肿瘤包绕左肾动静脉,术中必要时不得不切除右肾。








有些巨大的肾上腺肿瘤血供丰富,肿瘤乃至可能包绕腹腔干、肠系膜上动脉等重要血管,手术风险极大。




2019年9月门诊患者,患者,安徽宿州,女,65岁,体检发现左肾上腺肿物三月,体检CT提示:左肾上腺区结节灶,考虑嗜铬细胞瘤可能。游离甲氧基肾上腺素:192pg/ml,游离甲氧基去甲肾上腺素:357pg/ml。患者既往有脑梗史,长期服用阿司匹林肠溶胶囊、瑞舒伐他汀钙片。高血压病史十年,口服苯磺酸左氨氯地平片;糖尿病病史服用盐酸二甲双胍、格列齐特缓释片等;门诊拟“左肾上腺肿物,嗜铬细胞瘤可能”收住入院。




 肿瘤血供丰富,并累及整个左肾上腺,术中未见正常的肾上腺组织
肿瘤血供丰富,并累及整个左肾上腺,术中未见正常的肾上腺组织

 术中血压从游离肿瘤时的260/120降至切除肿瘤后的64/45mmHg,血压波动幅度巨大,符合嗜铬细胞瘤的临床表现。
术中血压从游离肿瘤时的260/120降至切除肿瘤后的64/45mmHg,血压波动幅度巨大,符合嗜铬细胞瘤的临床表现。








 2017年08月门诊患者,女,72岁,苏州市人,主诉高血压、冠心病十年,糖尿病五年,长期服用阿司匹林类抗凝药物,两周前体检发现右侧肾上腺占位后来院要求手术治疗,自述近年来时有心慌胸闷,长期服用高血压药三联,血压波动于165/95左右,CT检查提示:右肾上腺可见一园性低密度影,约4.3*5.6*4.5cm,考虑右肾上腺腺瘤;肾上腺功能检测提示正常,术前初步诊断为右肾上腺髓样脂肪瘤,肾上腺髓样脂肪瘤是一种发生于肾上腺的无功能良性肿瘤,在组织学上是由成熟的脂肪组织和正常的造血组织所构成。绝大多数发生于肾上腺髓质,该患者为老年高危患者,予以停用阿司匹林一周后,行腹腔镜下右肾上腺肿瘤切除术,术后恢复良好,病理结果提示为髓性脂肪瘤。
2017年08月门诊患者,女,72岁,苏州市人,主诉高血压、冠心病十年,糖尿病五年,长期服用阿司匹林类抗凝药物,两周前体检发现右侧肾上腺占位后来院要求手术治疗,自述近年来时有心慌胸闷,长期服用高血压药三联,血压波动于165/95左右,CT检查提示:右肾上腺可见一园性低密度影,约4.3*5.6*4.5cm,考虑右肾上腺腺瘤;肾上腺功能检测提示正常,术前初步诊断为右肾上腺髓样脂肪瘤,肾上腺髓样脂肪瘤是一种发生于肾上腺的无功能良性肿瘤,在组织学上是由成熟的脂肪组织和正常的造血组织所构成。绝大多数发生于肾上腺髓质,该患者为老年高危患者,予以停用阿司匹林一周后,行腹腔镜下右肾上腺肿瘤切除术,术后恢复良好,病理结果提示为髓性脂肪瘤。

CT提示右肾上腺肿瘤与膈顶毗邻关系明显。

术中发现右肾上腺肿瘤体积较大且与膈顶,下腔静脉关系密切。


2017年10月门诊患者,女,52岁,南京江宁人,主诉右侧腰酸两年,一月前体检发现右侧肾上腺巨大占位来我院要求手术治疗,自述近年来右侧腰酸明显,无明显头晕乏力,无肢体发麻等现象,无高血压史,CT检查提示:右肾上腺区可见一圆性囊性低密度影,约10*11*10cm,考虑右肾上腺皮质癌,并累及右肾上极背侧;肾上腺功能检测皮质醇未见明显异常,但VMA检测高达60.55,术前初步诊断为右肾上腺皮质癌、或右肾上腺嗜铬细胞瘤伴右肾转移,遂考虑取肋缘下切口经腹开放右肾上腺肿瘤切除术,术前考虑患者病情危重,皮质癌已可能浸润肝、肾,术前充分准备达两周,积极备血,联系快速病理,术中一并切除右肾肿瘤及右肾,术中失血达3000ml,术后转ICU重症监护。





术后病理提示恶性嗜铬细胞瘤,而该患者肾上腺肿瘤巨大却没有高血压病史,这说明一部分嗜铬细胞瘤患者的症状是隐匿性的,值得进一步研究。






有些肾上腺肿瘤游离过程中可能会发现异位的肾脏上极动脉

 此外,肾上腺肿瘤还需与一些腹腔内脏器或间位器官相鉴别,如副脾,胃憩室,囊肿,胰尾相鉴别。
此外,肾上腺肿瘤还需与一些腹腔内脏器或间位器官相鉴别,如副脾,胃憩室,囊肿,胰尾相鉴别。










其次,肾上腺肿瘤还需与转移癌相鉴别,初一看下图右肾上腺5cm左右占位病变,考虑恶性肿瘤,伴下腔静脉侵犯


检查胸片提示右上肺占位考虑肺癌,这时就要考虑肺癌才是原发肿瘤,肾上腺只不过是转移病灶。




肾上腺肿瘤也需与一些后腹腔内占位病变相鉴别,如增生、淋巴瘤、神经节瘤或纤维类良性肿瘤等,要与影像科阅片医生多沟通。









有些肾上腺血肿也需要和腺瘤相鉴别







此外并不是所有的嗜铬细胞瘤都是实性的,即使是肾上腺囊性病变也需要完善足够的术前准备,以避免术中术后心脑血管的剧烈波动。



 有些肾上腺肿瘤手术以后需要长期服用激素,影响伤口愈合容易感染,值得医患双方足够重视,尤其对于一些老年女性高危患者,糖尿病患者,一旦感染由于是机体深部感染,往往容易迁延不愈,治疗效果差。
有些肾上腺肿瘤手术以后需要长期服用激素,影响伤口愈合容易感染,值得医患双方足够重视,尤其对于一些老年女性高危患者,糖尿病患者,一旦感染由于是机体深部感染,往往容易迁延不愈,治疗效果差。

右肾上腺肿瘤术后感染脓肿形成包裹性积液,并引起右侧胸腔积液








肾上腺肿瘤的治疗方式和手术风险取决于其内分泌功能,肾上腺肿瘤手术前需要考虑肿瘤的性质,并针对性采取不同的术前准备方式,如激素、扩容、电解质平衡等等,降低围手术期的风险,且必要时需联系重症监护,肾上腺肿瘤手术的风险不完全取决于肿瘤的大小,而取决于肿瘤的内分泌功能强大与否,这是泌尿外科中风险很高的手术,往往危及生命,需严加重视;因而术前的充分准备和围手术期的监护非常重要,切不可仓促上阵,临阵磨枪,否则后果尤为严重。双侧肾上腺肿瘤做手术时尽可能保留少许正常的肾上腺组织以维持其基本的内分泌功能,但如果术后出现激素水平低下,不能达到生理水平的激素量时,患者需要终身服用激素。

肾上腺肿瘤可分为无功能腺瘤和有功能腺瘤。无功能腺瘤常常没有任何临床症状,多在体检中无意发现。有功能的肾上腺肿瘤根据分泌的激素不同可以分为皮质醇腺瘤、醛固酮腺瘤等。
皮质醇腺瘤
皮质醇腺瘤分泌皮质激素增多引起的,常见的表现是向心性肥胖,满月脸、水牛背,胸腹颈背脂肪增多,皮肤菲薄,多血质,皮肤紫纹;痤疮、多毛、女性月经失调,男性阳痿;性欲减退,免疫力低下;骨质疏松,容易引起脊柱压缩性骨折;血压上升,心肌肥厚,心衰;情绪烦躁,甚至精神异常。
醛固酮腺瘤
醛固酮腺瘤主要表现为高血压,多为缓慢进展的良性高血压,一般降压药物效果不明显;低血钾,醛固酮有促进尿钾排泄的作用,常引起肌肉无力、周期性麻痹、手足搐弱,甚至吞咽和呼吸困难,心电图常有明显异常。血浆肾素活性减低,由于醛固酮分泌增多,体内肾素分泌受到抑制,引起血浆肾素活性减低。
嗜铬细胞瘤
另外嗜铬细胞瘤也是肾上腺常见的肿瘤,由于肿瘤组织分泌大量儿茶酚胺类激素,如肾上腺素、去甲肾上腺素、多巴胺等,引起阵发性高血压,血压波动明显。儿茶酚胺类激素是体内调控血压的主要激素,其与血管内皮相关受体结合引起血管收缩,使血压上升,如果分泌过多常引起难以控制的高血压,一般降压药物治疗无效。

① 除夕纳入法定节假日 ② 5月2日纳入法定节假日 全年放假总数由11天增加至13天

小弟是指阴茎,阴茎肿了像游泳圈如果出现了异常表现,一般是多种原因所造成的,要及时详细的了解。

儿童椎管内神经鞘瘤相对成人较为少见,但也有其特点,以下为你详细阐述:
一、发病特点 发病率:相较于成人,儿童椎管内神经鞘瘤在儿童椎管内肿瘤中所占比例相对不高,但仍是需要关注的一类疾病。 年龄分布:可发生于各年龄段的儿童,不过不同年龄段的发病情况可能存在差异,总体来说没有明显的集中发病年龄段特点像某些特定儿童肿瘤那样。
二、临床表现 疼痛:同样是较为常见的症状,比如会诉说背部、颈部、腰部或肢体等部位的疼痛,由于儿童表达能力有限,可能描述不太准确,常表现为哭闹不安、不愿活动身体相应部位等,而且疼痛在夜间或活动后可能加重。 运动发育异常:与成人更多表现为既有运动功能受影响不同,儿童可能出现运动发育迟缓的情况。比如原本该到会爬、会走的阶段,却明显落后于同龄人,或者已经掌握的运动技能如行走,出现步态不稳、容易摔倒等情况,这是因为肿瘤压迫神经影响了正常的运动神经支配和发育。 脊柱畸形:部分儿童椎管内神经鞘瘤可能导致脊柱畸形,如脊柱侧弯等。这是由于肿瘤在椎管内生长,破坏了脊柱正常的力线平衡以及影响了周围肌肉的正常功能等因素共同作用的结果。 大小便功能障碍:若肿瘤位置影响到马尾神经等相关神经支配区域,儿童也可能出现大小便控制不佳的情况,比如尿床次数增多且难以通过常规训练改善、大便失禁等,不过在儿童中有时容易被误认为是正常的如厕训练未完成等情况而被忽视。
三、诊断难点与方法 诊断难点: 症状不典型:儿童往往不能准确清晰地表述自身症状,这使得依靠症状来判断疾病存在困难,容易与其他一些儿童常见疾病如生长痛、缺钙等混淆。 配合度低:在进行一些检查如影像学检查时,儿童可能因害怕、不理解而不能很好地配合,影响检查的顺利进行和结果的准确性。 诊断方法: 详细询问病史:医生需要向家长详细询问儿童的生长发育情况、症状出现的时间及变化过程、有无外伤史等,尽可能全面了解病情线索。 体格检查:仔细检查儿童的脊柱形态、肢体的感觉和运动功能、反射情况等,虽然儿童可能不太配合,但也要尽量准确判断是否存在神经系统异常。 影像学检查: X 线检查:可初步观察脊柱的形态,看是否存在脊柱侧弯等畸形情况,但对于肿瘤本身的显示并不理想。 CT 检查:能较好地显示椎管的骨性结构以及肿瘤对骨性结构的影响,但对于软组织的分辨能力相对较弱。 MRI 检查:是诊断儿童椎管内神经鞘瘤最重要的检查手段,它可以清晰地显示肿瘤的位置、大小、形态以及与周围神经、脊髓等组织的关系,为后续的治疗方案制定提供关键依据。 实验室检查:一般会进行血常规、血生化等常规检查,主要是为了排除其他可能引起类似症状的全身性疾病,如感染、代谢性疾病等。
四、治疗及预后 治疗: 手术治疗:手术切除是儿童椎管内神经鞘瘤的主要治疗方法。一旦确诊,在条件允许的情况下,尽可能早地进行手术。手术的目的是尽可能完整地切除肿瘤,解除肿瘤对神经组织的压迫,恢复神经功能。不过由于儿童身体仍在发育阶段,手术的难度和风险相对成人可能会更高一些,比如需要更加精细地操作以避免损伤脊髓和周围神经,同时要考虑到手术后脊柱的稳定性等问题。 辅助治疗:根据肿瘤的具体情况,如是否为恶性、切除是否完整等,可能会考虑辅助放疗或化疗等。但在儿童中,放疗和化疗的应用相对更加谨慎,因为它们可能会对儿童正在发育的身体尤其是神经系统造成潜在的伤害。 预后:总体来说,如果能早期发现并成功进行手术切除,且没有出现严重的神经损伤并发症,儿童的预后相对较好,可以恢复正常的生长发育和神经功能。但如果肿瘤发现较晚,已经造成了严重的神经损伤,或者手术过程中出现了意外的神经损伤等情况,可能会影响儿童日后的运动、感觉、大小便控制等功能,甚至可能导致残疾。 儿童椎管内神经鞘瘤需要引起家长和医生的高度重视,以便能早期发现、准确诊断和及时治疗,保障儿童的健康成长。

血小板过高要做骨髓穿刺检查吗?
展开更多














