
卵巢功能障碍是指卵巢在正常生理状态下无法正常运作,导致月经不规律、排卵问题、激素水平异常等问题。其病因主要包括年龄因素、卵巢囊肿、多囊卵巢综合征等。
1.年龄因素:随着年龄增长,女性的卵巢功能会逐渐衰退。到了更年期,卵巢功能减退会导致月经停止和激素水平变化。
2.卵巢囊肿:卵巢囊肿指的是卵巢内形成的液体或固体的囊肿。这些囊肿可导致卵巢排卵异常,影响卵巢功能,进而导致卵巢功能障碍的出现。
3.多囊卵巢综合征:是一种常见的女性生殖系统疾病,其特征之一是卵巢多囊,并伴有激素水平不平衡。也可导致排卵问题和卵巢功能障碍。
一旦出现卵巢功能障碍的现象,需尽快到医院就诊,在医生的指导下进行合理治疗。

都说现代女性要“上得厅堂,下得厨房;斗得过无赖,打得过流氓”,同时还要时刻注意身材不走样,气色不变差才是成功女性。否则就要冷不丁被冠上“黄脸婆”的称呼,被满脸胶原蛋白的00后叫一声老阿姨!其实,“黄脸婆”很大程度上都是你自己不注重保养,“熬”出来的!
我们都知道,植物的根系缺水、缺养分,花朵一定会衰朽、掉落,除了因为日常皮肤护理不当,同时随着年龄的增长,或是各种原因导致身体机能退化,我们的皮肤也会越来越差。人如果卵巢功能衰退,就会出现皮肤发黄、皱纹增多、月经改变、关节骨骼容易出现疼痛等情况,也就是我们常说的身体老化的表现。可想而知,卵巢在我们女性的一生中,扮演中重要的角色,是女性衰老的“进度表”。

一、卵巢的功能有哪些?
要想搞清上面的问题之前,我们先来了解一下卵巢功能。卵巢是女人最重要的生殖器官,它能分泌女性激素:雌激素与孕激素。孕激素有保护子宫内膜及促进生育的功能;雌激素不仅可以维持女性外观,使其散发女性魅力,更重要的是还可以保护心血管、保护骨骼、保护神经系统……雌激素几乎作用于女人的全身。人们常说女人是水做成的,那维系水样肌体晶莹玉润的法宝就是卵巢分泌的最重要的女性激素——雌激素。
二、决定卵巢功能的决定因素有哪些?

卵巢功能到底和什么有关呢?卵巢中含有许许多多的卵泡,其与卵泡的数量和质量密切相关。
(1)卵泡数量
卵泡数量在出生时已经被决定,约为200万~300万个,此后时时刻刻都在减少、死亡,到月经初潮时已降为30万~40万个左右。可见卵巢中的卵泡只会越来越少,不会越来越多,当卵泡耗竭,即进入绝经。女性一生中大约只有400个~500个卵泡发育成熟,用以维持正常月经及生育,而99.9%的卵泡均自生自灭了。
(2)卵泡质量
随着年龄的增长,因长时间受到外界影响:如恶劣环境、不健康饮食及不良的生活习惯等,卵泡的质量逐年下降。一般来说,每月有将近1000-2000个优秀卵泡一起生长,最后只有一个最优秀的卵泡发育成熟,其余卵泡全部陨落。
试管婴儿或不孕症用促性腺激素促排卵,最凶险的敌人就是卵巢过度刺激综合征(OHSS)了。人们和它斗争了几十年,还没有取得彻底的胜利。我们的目标很坚定,就是要OHSS-free(无OHSS)的促排卵治疗。把OHSS预防于萌芽之中,呵护好母亲和孩子的安全。
促排卵的凶险敌人——OHSS
不要以为做试管婴儿就像去一趟健身房那样简单,卵巢过度刺激综合征(OHSS)就是医生最担心的事件了。
它是发生于促排卵过程中的一种并发症,特征是多卵泡生长、卵巢体积显著增大,血管通透性增加,水份从血管内转移到外面,出现腹水、胸水、少尿、血液浓缩、血栓形成、以及肝肾功能受损,严重者可危及生命。

OHSS的级别
综合临床症状、超声及实验室检查可将OHSS分为轻、中、重三度:
- 轻度OHSS的发病率约20%~33%,表现为恶心、食欲差、腹胀等症状。
- 中度OHSS的发病率约3%~6%,在轻度的基础上出现腹水,检查发现白细胞轻度升高、血液轻度浓缩、肝酶升高。
- 重度OHSS的发病率约0.1%~2%,表现为大量的腹水、胸水、呼吸困难,低血容量休克、少尿、肾功能衰竭、甚至出现血栓危及生命。其中约1.9%的患者需要住院治疗。
OHSS的早晚发生之差
根据OHSS的发生时间可分为早发、晚发两种类型。
早发型OHSS与生长卵泡多,血清雌激素水平高有关,最重要的是注射HCG所诱发的,多发生在取卵后9天内。它来势汹汹,血球压积较高,腹水胸水增多时,常出现尿少,肾功能不全的危急指标。但如果没有怀孕,第10余天以后就转危为安,高枕无忧了。
晚发型OHSS一般发生在取卵后10天及以后,与怀孕胚胎分泌的HCG,以及注射的HCG黄体支持有关。它多与怀孕有关,起病缓,病情迁延,腹水胸水持续不减,血球压积多不高。住院的时间会比较长。
警惕OHSS的高风险女孩
哪些人群易发生卵巢过度刺激呢?
年轻(<30岁),身材瘦小(BMI<17)、多囊卵巢综合征、或卵巢内小卵泡很多的女性,过去发生过OHSS者更易再发,这类人群卵巢对促排卵药物的反应敏感,是高危人群。
抗苗勒氏管激素(AMH)及基础窦卵泡数(AFC)则是预测OHSS更客观直接指标。与年龄及BMI相比,AMH预测效果更好,当AMH>3.36ng/mL时OHSS发生的风险很高。

由于血清AMH值可在月经的任意一天抽血检测评估卵巢的储备,预测对促排卵药物的反应性。基础窦卵泡检测一般在月经来潮的第2~5天做阴道B超计数最为准确,以>14个小卵泡者易发生OHSS。反正高危女性的血清AMH水平是高的,基础窦卵泡是多的。

在促排过程中绝对避免OHSS的发生几乎是不可能的,但是近年来,负责任的医生们提出:“患者有权要求消灭OHSS的促排卵周期”。这对医生的要求更高了,OHSS成了辅助生殖计数中亟待攻克的首要难关。第一步,就是对高危人群可以进行早期预防,以降低OHSS的发生。

最好不让OHSS发生
1. 评估患者的卵巢反应性,制定个性化促排卵方案
对高风险女性,
①我们要精确计算和设计促性腺激素的启动剂量,以低剂量为原则;
②温和刺激方案、拮抗剂方案、联合GnRH激动剂扳机;
③当卵泡近成熟,血清雌激素水平过高时,可短暂停用促性腺激素,也称“coasting”;
④出现严重OHSS倾向时,可取消本周期;
⑤减少HCG的扳机剂量,取卵后禁用HCG进行黄体支持等。这些方法都能一定程度降低OHSS的发生。
2. 全胚胎冷冻
怀孕可增加OHSS的发生、加重病情,故高风险女性取卵形成胚胎后,可取消本周期新鲜胚胎移植,全部胚胎冷冻保存,择期做冻胚移植。这个策略可以显著降低迟发型OHSS的发生率,防治怀孕后病情迁延加重。并减少宫外孕、早产、低体重儿的风险。
3. 卵母细胞体外成熟(IVM)
卵母细胞体外成熟是在卵巢不刺激或微刺激的情况下,在小卵泡取卵,用特殊的体外培养液将不成熟的卵母细胞培养成熟后再做ICSI授精。IVM可以完全预防OHSS发生。中山大学附属第六医院生殖中心有成熟的IVM培养体系,不仅稳定,而且卵母细胞成熟率和妊娠率都令人欣喜。
4. 其它
在促排过程中B超发现OHSS倾向和盆腔积液征象时,可给高蛋白质饮食(鸡蛋、牛奶或蛋白粉等),避免剧烈运动以防止卵巢扭转。严重者可加用溴隐亭、阿司匹林、糖皮质激素、二甲双胍等药物预防和控制OHSS发生。
对OHSS的拯救行动
1. 补水补水
OHSS治疗以支持治疗为主。OHSS的发病机制是血管的渗透性增加,就如同一条漏水的水管,水不断外渗,导致水管里的水越来越少,杂质沉淀。所以最重要的是治疗措施是静脉补液,补的可不是普通的“水”,是昂贵的“琼浆玉液”,如人体白蛋白,血浆,代血浆等胶体液。

2. 抗凝抗凝
当OHSS发生时,人体内血管里的血液变得粘稠,容易形成血栓,这可是OHSS中最致命的风险呢。如果血栓堵上了肾、脑、肺等,就会器官衰竭了。历史上报告的死亡病例多是这个原因。所以给一些抗凝药物、皮质激素、多巴胺等,就是为了预防血栓。
3. 放水放水
OHSS形成的大量腹、胸水令人肚子胀,喘不过气,夜里不能平躺着睡觉,当这些症状难以忍受时可以考虑穿刺引流胸腹水,以缓解不适。
4. 保肝保肝
抽血检查时发现肝酶升高,表明肝功能受到一定程度的损害,这时就要护肝治疗啦。
综合而言, OHSS的预防远比治疗重要,如果发生了OHSS,遵循医生的指导就能顺利度过这道难关啦。这篇文章也是劝导年轻小夫妇,可不要自己不努力造人,就指望做试管婴儿,要知道促排卵也不是吃素的哦。
图片来源于网络,如有侵权请联系删除。

女性的卵巢功能如果保持的比较好的话女性就会显得比较年轻,女性的皮肤也会变得非常好,女性要想永保青春的话,保养卵巢一定要成为女性生活的一部分。
卵巢是女性最重要的生殖器官,然而很多女性都面临卵巢早衰的苦恼。因此,保养好卵巢很重要。那么女性怎么保养卵巢呢?
女性如何保养卵巢?
1、养成良好的生活习惯
生活有规律、起居有常、保持睡眠充足、做到劳逸结合等健康有规律的生活习惯,都能帮助保养卵巢的健康。
2、把握好生育时间
在现在的社会中,生育年龄普遍越来越大龄化,长期服用避孕药,首孕年龄越大,不进行母乳喂养等均易导致卵巢早衰。
3、适当运动
有专家发现缺乏锻炼的女性,卵巢早衰现象要比经常锻炼的女性提前很多。这说明女性坚持锻炼可使卵巢衰退的较晚。
4、调整好情绪
女性要善于调节好自己的情绪,正确对待发生的心理冲突,学会适当的发泄出心中的不良情绪,对保养卵巢会具有一定的帮助。
5、培养自己的兴趣爱好
专家指出,很多现代女性卵巢早衰都是营养心理压力过大所致。培养自己广泛的兴趣爱好,多听听音乐,种些花草都能帮助很好的调节情绪。
6、尽量少穿塑身内衣裤
塑身内衣的压迫,易导致卵巢发育受限,功能受损,使卵巢发生早衰现象。着装应该以宽松舒服为主要,若真想维持好的体态,不如多运动。
7、保持良好饮食和生活习惯
【采用高钙的饮食】每天摄取高钙的食物,可以低制卵巢疾病的产生率。
【少吃煎蛋】油煎的鸡蛋会增加患卵巢疾病的危机。因为煎鸡蛋的进程当中,会导致很多的生物活性分化产品的形成,如胆固醇氧化物等等。
【补充钙】每天摄取高钙食物可降低卵巢癌的发生率。含钙高的食物有豆制品、海带、紫菜、芝麻、山楂、海鱼、黑芝麻等。
【补充维生素和蛋白质】卵巢老化逐渐以分解代谢为主,蛋白质可以帮助人体组织的建造修补,是呵护卵巢的最有价值的营养成分。
【吃富含有叶酸的食物】增加富含有叶酸的食物,可以低制女性患卵巢疾病的产生。叶酸是一种水溶性的维生素b,是富含于绿色的蔬菜和柑橘类的生果以及全谷类的食物当中。
【多做腹式呼吸】腹式呼吸能够感觉到腹部的起伏,每天花30分钟的时间做腹式呼吸,腹壁肌肉的舒缩对子宫、卵巢有按摩的效果。
【改掉久坐的习惯】久坐很容易导致气血循环障碍,卵巢囊肿的症状影响盆腔健康。如果你的工作几乎离不开坐,最好每40分钟后站起来休息10分钟,让下肢血液能够畅通。

保养卵巢的一些小动作
一.吸气,双手向上伸展,保持5秒;吐气,双手合十,放于胸前。平衡呼吸。
此动作有利于增强心脏和肺部的氧气,给头部充氧,让大脑得到休息,对于月经不调引起的腰腹胀痛有缓解作用,同时也使卵巢处于上佳的休息状态。
二.向前弯腰,双手抱住小腿,前松后紧。
此动作有利于加强整个椎体的气血循环,预防因肾气虚弱所致的各种妇科疾病,可以消除紧张情绪。也可以使卵巢的激素分泌在正常的节奏中进行。
三.吐气,扭转腰部,保持5秒。左右各一次。
此动作可以纠正因平时姿态不正而引起的腹部胀痛,也能促使卵巢中偶尔出现的滤泡囊肿组织消失。
四.吐气,身体均匀向下。脚跟和臀部接触。
此动作可以加强整个全身气血循环,消除由于经期引起的水肿情况,按摩大小肠和子宫,消除便秘,也可对卵巢排卵后的创伤性劳损给予合理修复。
2024年9月4日,罗氏公司(Roche)官宣了fenebrutinib在复发型多发性硬化症患者的效果,最新数据将于第 40届欧洲多发性硬化治疗与研究委员会(ECTRIMS)大会上公布[1]。
接下来我们结合此次官宣数据和clinicaltrial公布数据,和大家先睹为快。
FENopta研究
FENopta研究是一项随机双盲对照研究,评估fenebrutinib 在复发型多发性硬化症中的疗效,也包含安全性和药代动力学信息。
主要结果
研究的主要结果是用药后第 4、8 、12 周的MRI扫描,观察新发 T1 钆增强(T1-Gd+)病灶率。次要终点包括在第4、8、12周通过脑部MRI扫描的新的或扩大的 T2 加权病变的数量、无任何新 T1 病变和新的或扩大的 T2 加权病变的患者比例(T1)。
12周研究的数据显示,fenebrutinib可穿过血脑屏障。与安慰剂相比,fenebrutinib组显著减少了新的T1病变和新的/扩大的T2病变(TI为活动性炎症的标志,T2体积变化代表慢性疾病负担)。T1病灶率方面,fenebrutinib组为0.077(0.043-0.135),对照组为0.245(0.144-0.418)[2]。
fenebrutinib的安全性特征与先前和正在进行的 fenebrutinib临床试验一致,并且没有发现新的安全问题。发生率大于 5% 的最常见不良事件(AEs)为尿路感染(8%)、新冠肺炎(7%)和咽炎(5%)。一名患者(1%)发生了严重不良事件。在开放标签扩展期,一名患者(1%)新出现无症状丙氨酸氨基转移酶升高,并在停药后恢复。
罗氏还公布了更长期的数据[1]:
接受fenebrutinib治疗的患者在一年时无复发的比例达96%,年复发率(ARR)为 0.04,并且通过扩展残疾状态量表(EDSS)测量,48 周内残疾无变化。
MRI显示fenebrutinib 治疗抑制了大脑中的疾病活动。在 48 周时,99%的患者无 T1 钆增强病变。在持续使用 fenebrutinib 治疗的 48 周内,T2 病变体积减少量是双盲期结束时(12周)的3倍。
临床试验方法
在双盲阶段,参与者分为两组,一组接受 200mg fenebrutinib口服,每日2次,持续12周。另外一组接受与 fenebrutinib匹配的安慰剂口服,每日2次,持续12周。
关于fenebrutinib
Fenebrutinib 是一种口服、可逆且非共价的布鲁顿氏酪氨酸激酶(BTK)抑制剂。 fenebrutinib 具有强效和高选择性的特点,对BTK的选择性是其他激酶的130倍,这种高选择特性有助于提高长期安全性[1]。
此外,它是目前唯一处于多发性硬化症Ⅲ期试验中的可逆抑制剂。fenebrutinib 是 B 细胞和小胶质细胞激活的双重抑制剂,这种双重抑制可能减少多发性硬化症的疾病活动和残疾进展,从而有可能满足多发性硬化症患者的目前未满足的医疗需求。
关于多发性硬化
多发性硬化(MS)是一种免疫介导的中枢神经系统炎性脱髓鞘疾病,病变具有时间多发与空间多发的特征。MS分为临床孤立综合征、复发缓解型MS、继发进展型MS和原发进展型MS(PPMS)。
复发缓解型MS的病程表现为明显的复发和缓解过程,每次发作后不留或仅留下轻微症状。80%~85%的MS患者疾病初期表现为本类型[3]。
原发进展型MS中,10%~15%的MS患者残疾功能障碍与临床复发无关,呈缓慢进行性加重,病程大于1年。PPMS分型包括原有MS疾病分型中的进展复发型MS(PRMS)。头颅MRI和(或)脊髓MRI具备典型MS病灶特征,脑脊液特异性寡克隆区带(oligoclonal bands,OCB)常为阳性[3]。
MS一经明确诊断,应尽早开始DMT并长期维持治疗,推荐患者共同参与制定治疗决策,设立明确的治疗目标及随访计划,定期评估,在确保安全的前提下尽快达到治疗目标。
关于罗氏制药[4]
罗氏制药始终致力于将科学成果转化为创新药品。 凝聚了来自罗氏、基因泰克、中外制药和全球250多个合作伙伴的全产业链成果,覆盖临床开发、制造和商业运营等。
罗氏制药拥有丰富的产品组合和产品管线罗氏聚焦于科学研究的成果转化可以追溯到一个多世纪前。罗氏专注于抗肿瘤、免疫、眼科、抗感染、神经科学和罕见病等疾病领域,坚信科学成果能为减轻人类痛苦、延长人类生命,从而拥有更加美好健康的未来,发挥巨大作用。50多年来,罗氏一直走在癌症研究和治疗的最前沿。如今,罗氏研发的药物,已经惠及了很多乳腺癌患者、皮肤癌患者、卵巢癌患者以及肺癌患者等,为他们赢得了宝贵的时间。
在世界卫生组织基本药物目录中,有超过30个罗氏开发的药品。通过聚焦创新、不断研发,以解决大量尚未被满足的患者需求,罗氏以实际行动兑现对社会,对患者的长期承诺。
参考文献:
1.Roche’s fenebrutinib demonstrated near-complete suppression of disease activity and disability progression for up to 48 weeks in patients with relapsing multiple sclerosis.
2.A Study to Investigate the Efficacy of Fenebrutinib in Relapsing Multiple Sclerosis (RMS) (FENopta)
3.中华医学会神经病学分会神经免疫学组 . 多发性硬化诊断与治疗中国指南(2023版)[J]. 中华神经科杂志, 2024, 57(1): 10-23. DOI: 10.3760/cma.j.cn113694-20230918-00173.
4.https://www.roche.com.cn/about/business/pharmaceuticals
2024年9月4日,信达生物制药集团宣布其PD-1/IL-2α-bias双特异性抗体融合蛋白IBI363获得美国食品和药物监督管理局(FDA)授予快速通道资格(fast track designation, FTD),拟定适应症为既往接受过至少一线含PD-1/L1检查点抑制剂系统性治疗后进展的局部晚期或转移性黑色素瘤(脉络膜黑色素瘤除外)。
主要结果
37例既往接受过免疫治疗的黑色素瘤患者接受了1mg/kg IBI363治疗并至少接受了一次基线后肿瘤评估,11例患者获得了客观缓解,包括1例CR和10例PR,ORR和DCR分别为29.7%和73.0%。
8例既往未经过免疫治疗的黏膜型黑色素瘤受试者中,6例受试者达到客观缓解,其中1例受试者最佳疗效为CR,5例受试者最佳疗效为PR,总体ORR达到75.0%,DCR为100%。
关于IBI363(PD-1/IL-2α-bias双特异性融合蛋白)
IBI363是由信达生物自主研发的全球首创PD-1/IL-2双特异性融合蛋白,同时具有阻断PD-1/PD-L1通路和激活IL-2通路两项功能。
IBI363的IL-2臂经过了设计改造,保留了其对IL-2 Rα的亲和力,但削弱了对IL-2Rβ和IL-2Rγ的结合能力,以此降低毒性;而PD-1结合臂可以同时实现对PD-1的阻断和IL-2的选择性递送。
由于新激活的肿瘤特异性T细胞同时表达PD-1和IL-2α,这一差异性策略可以更精确和有效地实现对该T细胞亚群的靶向和激活。IBI363不仅在多种荷瘤药理学模型中展现出了良好抗肿瘤活性,在PD-1耐药和转移模型中也表现出了突出的抑瘤效力。
从临床迫切需求出发,信达生物正在中国、美国、澳大利亚开展临床研究探索IBI363在针对各种晚期恶性肿瘤的有效性和安全性。
关于黑色素瘤
黑色素瘤是一种从黑色素细胞发展而来的恶性肿瘤,是美国第五大最常见的癌症病因3。虽然黑色素瘤只占所有类型皮肤癌的3%,但它的死亡率是所有类型中最高的,而且最容易发生转移。
在中国,黑色素瘤的发生率和死亡率也在逐年增加。按发病部位分类,黑色素瘤主要分为皮肤黑色素瘤、肢端黑色素瘤和粘膜黑色素瘤等。中国黑色素瘤与欧美白种人差异较大,两者在发病机制、生物学行为、组织学形态、治疗方法以及预后等方面差异较大。
对于晚期皮肤和肢端黑色素瘤,如携带 BRAF V600 突变,则首选分子靶向药物BRAF抑制剂联合MEK抑制剂,无BRAF V600突变的患者一线治疗可考虑化疗与抗血管生成药物联合治疗,免疫治疗尚未在国内获批晚期黑色素瘤一线治疗的适应症。二线主要考虑与已接受一线治疗不同的药物治疗,对于一线未使用过PD-1单抗的受试者,二线治疗可选择PD-1单抗。
对于晚期粘膜黑色素瘤,一线治疗可考虑化疗或PD-1单抗联合抗血管生成药物,如携带BRAF V600突变,可选择BRAF抑制剂±MEK 抑制剂,后线治疗选择十分有限]。
关于信达
信达生物成立于2011年,致力于研发、生产和销售肿瘤、自身免疫、代谢、眼科等重大疾病领域的创新药物,让我们的工作惠及更多的生命。公司已有10个产品获得批准上市,它们分别是信迪利单抗注射液,贝伐珠单抗注射液,阿达木单抗注射液,利妥昔单抗注射液,佩米替尼片,奥雷巴替尼片, 雷莫西尤单抗注射液,塞普替尼胶囊,伊基奥仑赛注射液和托莱西单抗注射液。
目前,同时还有4个品种在NMPA审评中,4个新药分子进入III期或关键性临床研究,另外还有18个新药品种已进入临床研究。
公司已与礼来、罗氏、赛诺菲、Adimab、Incyte和MD Anderson 癌症中心等国际合作方达成30多项战略合作。信达生物在不断自研创新药物、谋求自身发展的同时,秉承经济建设以人民为中心的发展思想。
9月1日,欧洲心脏病学会年会(ESC)上,拜耳公布了FINEARTS-HF III期研究结果,这个研究也同时发布在《新英格兰医学杂志》(NEJM)上。这个研究是关于非奈利酮在射血分数轻度降低或保留的心力衰竭中的实际应用,来看其心衰潜力的结果。
FINEARTS-HF研究
FINEARTS-HF研究是一项多中心随机双盲平行对照试验,甾体类盐皮质激素受体拮抗剂(如非奈利酮)可降低射血分数降低的心衰患者的发病率和死亡率,但它们在射血分数轻度降低或保留的心力衰竭患者中的疗效尚未确定。
因此该研究的目的是评估非奈利酮对患有心力衰竭(NYHA II-IV级)和左心室射血分数≥40%(LVEF ≥ 40%)疗效和安全性。
主要结果
研究的主要结果是在最长42个月的时间内,评估入组参与人的心血管死亡和心力衰竭事件的数量的综合终点,其中心力衰竭事件包括首次和复发事件。
- 在中位随访32个月期间,非奈利酮组3003名患者中的624名发生了1083次主要结局事件,对照组2998名患者中的719名发生了1283次主要结局事件(比率比,0.84;95% CI,0.74 至 0.95;P = 0.007)。
- 非奈利酮组总恶化心力衰竭事件数为842次,安慰剂组为1024次(比率比,0.82;95% CI,0.71 至 0.94;P = 0.006)。
- 心血管原因死亡的患者百分比分别为8.1%和8.7%(风险比,0.93;95% CI,0.78 至 1.11)[1]。
在射血分数轻度降低或保留的心力衰竭患者中,非奈利酮导致总恶化心力衰竭事件和心血管原因死亡的复合结局发生率显著低于安慰剂。
临床试验方法
实验组:非奈利酮,口服,根据肾小球滤过率(eGFR)调整剂量。对于eGFR≤60 mL/min/1.73m² 的成年患者,起始剂量是10mg/天 qd,最大剂量是20mg/天。对于 eGFR>60 mL/min/1.73m² 的成年患者,起起始剂量是20mg/天,最大剂量是40mg/天[2]。
对照组:服用安慰剂,类非奈利酮。
关于非奈利酮[3]
非奈利酮创新结构非甾体高选择性MRA,抑制炎症纤维化,独立于血糖/血压管理,直接带来肾脏和心血管双重获益。
- 适应证:
适用于降低患有 2 型糖尿病(T2D)相关慢性肾脏病(CKD)的成年患者持续估算肾小球滤过率(eGFR)下降、终末期肾病、心血管死亡、非致命性心肌梗死以及因心力衰竭住院的风险。
- 注意事项:
可能会导致高钾血症,治疗期间定期测量血清钾,并相应地调整剂量。对于有高钾血症风险的患者,可能需要更频繁地监测。
关于心衰
心衰是一种复杂的临床综合征,是由于多种原因导致的心脏结构和/或功能异常,使心脏在静息或运动时难以有效地收缩和/或充盈,导致心输出量下降或心腔内压力增高,引起相关症状和/或体征[4]。心衰是各种心脏疾病的严重表现或晚期阶段,死亡率和再住院率居高不[5]。
指南推荐的治疗药物包括利尿剂、RAAS 抑制剂、β受体阻滞剂、盐皮质激素受体拮抗剂、SGLT‑2i等[4]。
关于拜耳[6]
拜耳是一家拥有150多年历史的生命科学企业,在医药保健和农业领域具有核心竞争力。凭借创新产品,拜耳始终致力于寻找解决方案以应对当今世界的一些重大挑战。
随着全球人口不断增长和老龄化程度不断加深,充足的食物供应和完善的医疗保健显得尤为重要。凭借创新产品,拜耳始终致力于寻找解决方案以应对当今世界的一些重大挑战。拜耳通过在研发活动中重点关注疾病预防、缓解和治疗,不断改善数量日益增长、预期寿命不断延长的人们的生活质量。我们还为供应可靠的高品质食物、饲料和植物原料做出重要贡献。
参考文献:
1.Solomon SD, McMurray JJV, et al.FINEARTS-HF Committees and Investigators. Finerenone in Heart Failure with Mildly Reduced or Preserved Ejection Fraction. N Engl J Med. 2024 Sep 1. doi: 10.1056/NEJMoa2407107. Epub ahead of print. PMID: 39225278.
2.Study to Evaluate the Efficacy (Effect on Disease) and Safety of Finerenone on Morbidity (Events Indicating Disease Worsening) & Mortality (Death Rate) in Participants With Heart Failure and Left Ventricular Ejection Fraction (Proportion of Blood Expelled Per Heart Stroke) Greater or Equal to 40% (FINEARTS-HF).
3.Product information:KERENDIA- finerenone tablet, film coated.Bayer Healthcare Pharmaceuticals Inc.September 1, 2022.
4.中华医学会, 中华医学会杂志社, 中华医学会全科医学分会, 等. 中国心力衰竭基层诊疗与管理指南( 实践版.2024)[J].中华全科医师杂志, 2024,23(7): 683-693.
5.中华医学会心血管病学分会, 中国医师协会心血管内科医师分会, 中国医师协会心力衰竭专业委员会, 等 . 中国心力衰竭诊断和治疗指南 2024[J]. 中华心血管病杂志, 2024, 52(3): 235-275.
肺癌是国内第一大癌,这条管线的新药也是百家争鸣,24年8月29日,拜耳又有新布局,其III期SOHO-02研究迎来首位患者。
SOHO-02研究布局于HER2激活突变的晚期非小细胞肺癌(NSCLC)的跑道,旨在评估其新药的疗效和安全性,拜耳对照对比的竞品是帕博利珠单抗和铂类药物。由于研究结果还没有发布,我们先看看这个研究的设计部分。
SOHO-02研究[1]
SOHO-02研究是一项多中心随机对照Ⅲ试验,之所以选择这个赛道,是为了寻找HER2突变型晚期非小细胞肺癌(NSCLC)的更优治疗方法。晚期 NSCLC大家知道,已扩散到附近组织或身体的其他部位,不太能通过目前可用的治疗方法治愈或控制。而HER2 是一种帮助细胞生长和分裂的蛋白质。癌细胞中异常 HER2 的产生,从而导致异常的细胞生长和分裂。
拜耳所研究的治疗药物BAY 2927088 可能可阻断突变的 HER2 蛋白,从而可能阻止 NSCLC 的扩散。那么这个对照试验考察什么结果?
主要结果
研究还是选择了经典的RECIST 1.1 标准下的无进展生存期(PFS),预计时间为两年。次要结果包括OS、ORR等。
临床试验方法
将入组患者分为两组,一组接受BAY2927088 20 mg,每日两次,口服,直至根据 RECIST v1.1 标准出现疾病进展、不可接受的毒性或其他停药标准。
另外一组采用标准治疗法,静脉注射 帕博利珠单抗+顺铂+培美曲塞,每 21 天一个周期,直至根据 RECIST v1.1 标准出现疾病进展、不可接受的毒性或其他停药标准。
关于BAY 2927088
BAY 2927088目前还处于Ⅱ期试验中,因此没有对应药品名,没有适应证等信息。但这个药来头可不小, 源自拜耳与美国麻省理工学院、哈佛大学博德研究所的长期战略研究联盟。且在24年被FDA认定为“突破性疗法”。FDA 的突破性疗法认定旨在加速有望成为治疗严重或危及生命的疾病药物的开发和审查。
突破性疗法认定也是基于 BAY 2927088的 I 期临床,估了该药在 HER2/EGFR 型晚期非小细胞肺癌成年患者中的安全性、药代动力学和疗效。早期临床证据表明,该药有望HER2型突变非小细胞肺癌患者受益[2]。
关于非小细胞肺癌
肺癌是全球癌症相关死亡的主要原因。非小细胞肺癌是最常见的肺癌类型,占病例的85%以上。在 2%-4%的晚期非小细胞肺癌中发现激活型 HER2 突变[2]。
人表皮生长因子受体 2/ERB-B2 受体酪氨酸激酶2(HER2/ERBB2)是 EGFR(表皮生长因子受体)家族中的一种酪氨酸激酶受体,是一个比较火的治疗靶点 。HER2没有已知的可溶性配体,其下游信号传导是通过与其他配体结合的 HER 家族成员二聚化而触发的,这导致下游 PI3K/AKT 和 MEK/ERK 通路的磷酸化和激活。HER2 通路的改变通过增加二聚化和自磷酸化来驱动肿瘤发生,导致细胞生长失控[3]。
关于拜耳
拜耳是一家全球性企业,在医疗保健和农业生命科学领域拥有核心竞争力。其设计产品和服务,旨在帮助应对世界上一些最大的挑战,并满足人类健康和营养的最基本需求。拜耳致力于推动可持续发展,并通过业务产生积极影响。借助科学的力量,拜耳开创了推动生命进步的新可能性。这意味着通过增强日常健康、改进患者护理方法以及寻找更好的方式来滋养世界各地的社区,重新构想如何关爱自己和彼此[4]。
参考文献:
1.A Study to Learn More About How Well BAY 2927088 Works and How Safe it is Compared With Standard Treatment, in Participants Who Have Advanced Non-small Cell Lung Cancer (NSCLC) With Mutations in the Genes of Human Epidermal Growth Factor Receptor 2 (HER2) (SOHO-02)
2.Bayer receives U.S. FDA Breakthrough Therapy designation for BAY 2927088 for non-small cell lung cancer harboring HER2 activating mutations
3.Uy NF, Merkhofer CM, Baik CS. HER2 in Non-Small Cell Lung Cancer: A Review of Emerging Therapies. Cancers (Basel). 2022 Aug 27;14(17):4155. doi: 10.3390/cancers14174155. PMID: 36077691; PMCID: PMC9454740.
24年8月30日,皮尔法伯制药近期官宣:欧盟委员会批准“恩考芬尼与比美替尼联合疗法”扩展适应症,可用于治疗携带 BRAF V600E 突变的晚期非小细胞肺癌(NSCLC)成年患者。
欧盟批准基于II期 PHAROS 试验的结果,今天让我们一起聊聊这个新药组合。
PHAROS研究
PHAROS研究是一项多中心非随机的II期研究,由辉瑞赞助,主要想确定恩考芬尼+比美替尼联合疗法治疗 BRAFV600E 突变的转移性非小细胞肺癌的安全性、有效性和耐受性。
主要结果
为了确定药物的有效性,选择“客观缓解(OR)的参与者百分比”这个指标作为主要结果,怎么理解ORR百分比?它指的是患者用药后实现完全缓解 [CR] 或部分缓解 [PR]占总参与人数的百分比。
这个完全缓解和部分缓解也不是凭空捏造的,完全缓解是所有非淋巴结靶病灶消失(所有靶病灶记录长度为 0 毫米,任何病理淋巴结 [记录为靶病灶] 的短轴必须缩小至 < 10 mm),并且所有非靶病灶完全消失(所有非靶病灶标记为 “消失”,所有淋巴结的大小必须为非病理性 [<10 毫米短轴])。部分缓解是靶病灶直径总和(SOD)减少 30% 或更多,以基线 SOD 为参考[1]。
试验结果不超过36个月,将试验分为两组(详见临床试验方法部分)——初始治疗组和已接受其他治疗组,结果显示,该联合疗法具有显著的临床益处,初治治疗组的ORR为 75%[15% 的完全缓解(CRs)和 59% 的部分缓解(PRs)],已接受其他治疗组为 46%(10% 的 CRs 和 36% 的 PRs)[2]。
安全性方面,最常见的治疗相关不良事件(TRAEs ≥20%)为恶心(50%)、腹泻(43%)、疲劳(32%)和呕吐(29%)。14% 的患者发生了治疗相关的严重不良事件,最常见的是结肠炎(3%)[2]。
临床试验方法
将招募初治患者,或接受过以下治疗的患者:
- 一线标准铂类化疗;
- 一线抗程序性细胞死亡蛋白 1(PD - 1)/ 程序性细胞死亡蛋白配体 1(PD - L1)抑制剂单独治疗或与铂类化疗联合治疗。
接受组合药物治疗的剂量如下:
- 恩考芬尼 450 mg,每日一次(qd)
- 比美替尼 45 mg,每日两次(bid)
28 天(±3 天)为一个治疗周期,持续到患者符合结果部分里介绍的治疗退出标准。
关于恩考芬尼与比美替尼
恩考芬尼是一种强效且高度选择性的 BRAF 抑制剂,比美替尼是一种强效且选择性的 MEK 抑制剂,它们抑制 MAPK 通路中的激酶 在 BRAFV600E 突变的 NSCLC 中该通路被持续激活,从而产生临床相关的抗肿瘤活性。2018 年,欧盟委员会(EC)批准恩考芬尼 + 比美替尼用于治疗携带 BRAFV600 突变的不可切除或转移性黑色素瘤成年患者。2020 年,欧盟委员会批准恩考芬尼与西妥昔单抗联合用于治疗既往接受过系统治疗的携带 BRAFV600E 突变的转移性 CRC 成年患者。
恩考芬尼的用药信息[4]
适应证:
BRAF V600E 或 V600K 突变阳性的不可切除或转移性黑色素瘤、BRAF V600E 突变阳性的转移性结直肠癌(CRC)、BRAF V600E 突变阳性的转移性非小细胞肺癌(NSCLC)。
注意事项
- 新发原发性恶性肿瘤:在使用BRAF抑制剂治疗的患者中观察到新发的皮肤和非皮肤原发性恶性肿瘤,BRAFTOVI也可能导致此类情况发生。
- 心肌病:与比美替尼联合用药,在治疗的患者中出现心肌病,表现为与症状性或无症状性射血分数降低相关的左心室功能障碍。在开始治疗前、开始治疗后一个月以及治疗期间每2-3个月通过超声心动图或MUGA扫描评估射血分数。根据不良反应的严重程度,暂停、减少剂量或永久停药。
- 肝毒性 与比美替尼联合用药,可能会发生肝毒性。用药前、治疗期间每月以及根据临床指征监测肝功能实验室检查。根据不良反应的严重程度,暂停、减少剂量或永久停药。
- 出血:根据不良反应的严重程度,暂停、减少剂量或永久停药。
- 葡萄膜炎 治疗患者有出现葡萄膜炎,包括虹膜炎和虹膜睫状体炎。每次就诊时评估视觉症状。定期进行眼科评估,对于新出现或恶化的视觉障碍,以及跟踪新出现或持续的眼科发现。根据不良反应的严重程度,暂停、减少剂量或永久停药。
比美替尼的用药信息[5]
适应证
- BRAF V600E 或 V600K 突变阳性的不可切除或转移性黑色素瘤、BRAF V600E 突变阳性的转移性非小细胞肺癌(NSCLC)。
注意事项:
- 新发原发性恶性肿瘤:与恩考芬尼联合使用时,可能会发生皮肤和非皮肤的新发原发性恶性肿瘤。在开始治疗前、治疗期间和停药后监测患者是否出现新的恶性肿瘤。
- 心肌病:在开始治疗前、开始治疗后一个月以及治疗期间每2-3个月通过超声心动图或MUGA扫描评估射血分数。治疗期间应密切监测有心血管危险因素的患者。根据不良反应的严重程度,暂停、减少剂量或永久停药。
- 间质性肺病:对于新出现或进展性的无法解释的肺部症状或发现,评估是否可能为间质性肺病(ILD)。根据不良反应的严重程度,暂停、减少剂量或永久停药。
- 肝毒性:可能会发生肝毒性。用药前、治疗期间每月以及根据临床指征监测肝功能实验室检查。根据不良反应的严重程度,暂停、减少剂量或永久停药
- 横纹肌溶解:用药前、治疗期间定期以及根据临床指征监测CPK和肌酐水平。根据不良反应的严重程度,暂停、减少剂量或永久停药。
关于非小细胞肺癌
在非小细胞肺癌(NSCLC)患者中,激活型 BRAF 驱动突变发生在大约3%- 4%的患者。虽然他们在所有 NSCLC患者中只占一小部分,但由于 NSCLC 患病人群较多,如全球每年新增病例超过 200 万例,死亡人数超过 170 万例 ,故BRAF 突变型 NSCLC 患者的数量相对较多[2]。
关于皮尔法伯 [5]
皮尔法伯集团(Pierre Fabre)拥有世界第二大护肤品及化妆品实验室,也是全法第二大私营制药集团。集团业务涵盖处方药、医学护肤品及公共健康三个领域,产品销往130多个国家和地区,于全球45个国家设有子公司。
集团旗下皮尔法伯制药公司致力于植物研究,是植物药研发领域的行业翘楚。大自然就是我们的灵感源泉,为我们提供朝健康和美丽迈进的方向,也是我们业务模式一直以来的核心。我们致力于研究天然物质,为达成皮尔法伯的绿色使命打下坚实的基础。
参考文献:
- An Open-label Study of Encorafenib + Binimetinib in Patients With BRAFV600-mutant Non-small Cell Lung Cancer
- Riely GJ, Ahn MJ, Felip E, Ramalingam SS, Smit EF, Tsao AS, Alcasid A, Usari T, Wissel PS, Wilner KD, Johnson BE. Encorafenib plus binimetinib in patients withBRAFV600-mutant non-small cell lung cancer: phase II PHAROS study design. Future Oncol. 2022 Mar;18(7):781-791. doi: 10.2217/fon-2021-1250. Epub 2021 Dec 17. PMID: 34918546.
- Product information:BRAFTOVI- encorafenib capsule
- Product information:MEKTOVI- binimetinib tablet, film coated
- https://www.pierre-fabre.com/zh-cn/jituanpinpai
- https://mma.prnewswire.com/media/2493339/Pierre_Fabre_Approval.pdf
24年7月31日,号称“世界首款脑部再生治疗药”的人体体细胞干细胞加工产品获批日本,他便是我们今天的主角——vandefitemcel(SB623)。这款药物是一款可进行颅内植入的混悬液,用于治疗因创伤性脑损伤导致的慢性运动性瘫痪。值得注意的一点是,这款药物在日本的获批为有条件有时限的获批。

新药批准是基于在日本和美国进行的全球Ⅱ期临床试验,目前公开发表在期刊上的有两篇,分别是16年和21年发布。我们来看看这两项研究的主要效果。
干细胞输注的研究
两篇研究都使用了骨髓来源的间质干细胞(MSC),MSCs 有下列特性[1]:
1.免疫原性低;
2.可从不同的成人组织中分离出来,并在培养皿中以极大的扩增能力进行培养。
至于MSCs与神经系统的渊源,还得从神经系统疾病机制说起,间质干细胞与神经系统旁分泌信号有关,涉及免疫调节、神经保护、诱导内源性神经发生、血管生成和细胞外基质重塑等[1]。正是因为这些背后的机制,干细胞和神经修复似乎“天然契合”,故而干细胞正在被为神经领域疯狂探索中。
研究1主要对18 名病情稳定的慢性中风患者进行了 12个月的随访,就有效性而言,多项评分有所改善:
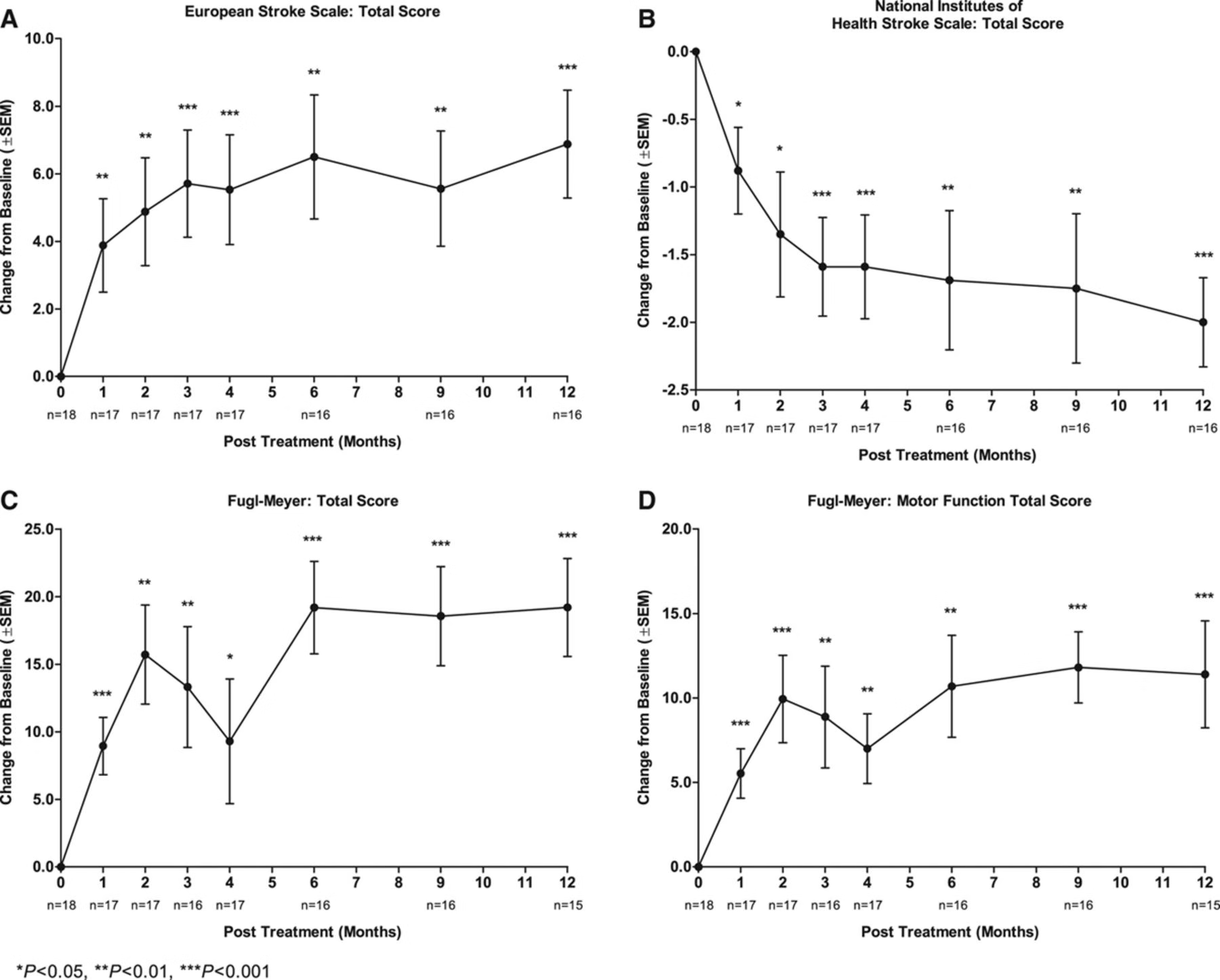
欧洲卒中量表:平均增加 6.88(95%置信区间,3.5 - 10.3;P < 0.001)
国立卫生研究院卒中量表:平均减少 2.00(95%置信区间,-2.7 至 -1.3;P < 0.001)
Fugl - Meyer 总分:平均增加 19.20(95%置信区间,11.4 - 27.0;P < 0.001)
Fugl - Meyer 运动功能总分:平均增加 11.40(95%置信区间,4.6 - 18.2;P < 0.001)。但改良 Rankin 量表未观察到变化。
在安全性方面,所有患者都经历了至少 1 次治疗期间出现的不良事件,6 名患者经历了 6 次严重的治疗期间出现的不良事件,其中 2 次可能或肯定与手术过程有关,但没与细胞治疗有关。所有严重的治疗期间出现的不良事件都已解决,且没有后遗症。没有剂量限制性毒性反应或死亡[3]。
研究2主要确定了后续研究干细胞所采用的量表差异,为期 1 年,是一项双盲随机手术假对照的Ⅱ期试验,也称 STEMTRA 试验。创伤性脑损伤(TBI)继发慢性运动功能缺损的患者(N = 61)接受了脑内立体定向植入修饰的骨髓来源间充质基质(SB623)细胞。通过多项量表对比测量[4]。
测量结果如下:
残疾评定量表为 - 1.5 分
Fugl - Meyer 上肢子量表为 6.2 分
Fugl - Meyer 下肢子量表为 3.2 分
Fugl - Meyer 运动量表为 8.4 分
总的来说,研究2后其后续继续临床试验奠定了技术基础,确定了后续试验的评分量表和评估方式。
此外,根据SanBio官网最新信息,目前正在进行上市后研究[5]。

具体如何输注?输多少怎么定?
这个药物是由健康成人骨髓液来源的间质细胞加工,当移植到脑内受损的神经组织时,会释放 FGF-2(一种蛋白质),促进受损神经细胞原本具有的再生能力,有望促进神经细胞的增殖和分化[6]。
适应证:与创伤性脑损伤相关的慢性运动性瘫痪的改善[7]。
用法用量 [7]:对于成人,使用专用的输送装置套件,通过脑立体定向手术,将5×10^6个人(同种异体)骨髓来源的间充质干细胞(300μL细胞悬液)植入到病灶周围的脑组织中。
通过在颅骨上制作的钻孔,沿着三条轨迹将细胞植入到病灶周围区域。对于每条轨迹,注射100μL细胞悬液,在总共5个位点上分别沉积20μL溶液,这些位点从最深位点开始间隔5 - 6mm。植入的速度应约为10μL/min。按照以下步骤进行植入:
1. 在开始操作之前,将专用输送装置套件中的导向&停止器和配备管芯的插入器连接到用于侵入性神经外科手术的头部固定装置上。
2. 解冻用于颅内植入的细胞悬液,用专用制备溶液洗涤,并使用专用制备溶液将细胞悬液的浓度调整为1.67×106个细胞/100μL。在将制备好的细胞悬液填充到专用输送装置套件中的固定有插管的微注射器之前,用专用制备溶液清洗该微注射器。
关于疾病[7]
创伤性脑损伤(TBI)是由头部受到强烈的外力作用引起的,例如交通事故或跌倒,这会损伤颅骨内的脑组织。TBI 的症状表现和出现时间在患者之间差异很大,并且根据大脑受影响的区域,患者可能会经历运动功能障碍或高级大脑功能障碍等后遗症。
研究表明,被破坏或受损的脑组织不会自然再生,进入 TBI 慢性期并出现运动性瘫痪的患者,其日常生活和社交生活将受到终身影响,这表明存在着重大的未满足的医疗需求。
关于SanBio
SanBio 致力于再生细胞药的研究、开发、制造和销售的再生细胞业务。主要针对现有医疗・药品无法应对、未满足医疗需求较高的中枢神经系统领域的疾病[6]。
参考文献:
1.Azevedo-Pereira RL, Aizman I, Nejadnik B. Mesenchymal Stem Cells Promote an Increase in Neuronal Oscillation via Glutamate Tonic Release. Neuroscience. 2024 Aug 6;552:76-88. doi: 10.1016/j.neuroscience.2024.06.015. Epub 2024 Jun 21. PMID: 38909673.
2.Study of Modified Stem Cells (SB623) in Patients With Chronic Motor Deficit From Ischemic Stroke (ACTIsSIMA)
3.Steinberg GK, Kondziolka D, Wechsler LR, Lunsford LD, Coburn ML, Billigen JB, Kim AS, Johnson JN, Bates D, King B, Case C, McGrogan M, Yankee EW, Schwartz NE. Clinical Outcomes of Transplanted Modified Bone Marrow-Derived Mesenchymal Stem Cells in Stroke: A Phase 1/2a Study. Stroke. 2016 Jul;47(7):1817-24. doi: 10.1161/STROKEAHA.116.012995. Epub 2016 Jun 2. PMID: 27256670; PMCID: PMC5828512.
4.Kawabori M, Weintraub AH, Imai H, Zinkevych I, McAllister P, Steinberg GK, Frishberg BM, Yasuhara T, Chen JW, Cramer SC, Achrol AS, Schwartz NE, Suenaga J, Lu DC, Semeniv I, Nakamura H, Kondziolka D, Chida D, Kaneko T, Karasawa Y, Paadre S, Nejadnik B, Bates D, Stonehouse AH, Richardson RM, Okonkwo DO. Cell Therapy for Chronic TBI: Interim Analysis of the Randomized Controlled STEMTRA Trial. Neurology. 2021 Feb 22;96(8):e1202-e1214. doi: 10.1212/WNL.0000000000011450. PMID: 33397772; PMCID: PMC8055341.
5.https://www.sanbio.com/
6.基礎研究結果のお知らせ:主要開発品SB623が神経活動とネットワーク形成を促進することを示した論文がNeuroscienceに掲載
7.SanBio Obtains Marketing Approval for “AKUUGO®Suspension for Intracranial Implantation” (INN: Vandefitemcel) as a Therapeutic Agent for Improving Chronic Motor Paralysis From Traumatic Brain Injury (TBI)
展开更多














