
3岁的小孩膝盖外翻如何治疗,因为小孩的骨骼发育,现在3岁还是刚开始,如果是觉得膝盖有些外翻,因为有些膝盖外翻合并上下关节也有问题,首先要看看有没有扁平足,有些小孩会合并有些扁平足,有些小孩可能有髋关节的问题,髋关节脱位或者发育差一些也会出膝盖外翻,如果排除掉扁平足跟髋关节的问题,有些膝盖外翻,可以叫小孩平时常生活中家长给按摩一下,如果外翻可以跟做内翻跟它对抗的动作,或者是教小孩翘二郎还是盘腿,这些动作有些帮助。










参考文献:
[1]2岁前罗圈腿属正常[J].启蒙(0-3岁). 2012(08)
[2]丁焕文,张迪辉,涂强,等.计算机辅助膝内翻及外翻畸形分析和精确矫形[J/CD]. 中华关节外科杂志: 电子版,2012,6( 3) : 376-385.
[3]<期刊>·医药卫生科技·外科学;·医药卫生科技·儿科学;·《现代医药卫生》,2013年.10期
[4]维生素D缺乏性佝偻病防治建议专家讨论会纪要,中华医学会儿科学分会儿童保健学组,全国佝偻病防治科研协作组,中华儿科杂志,2008,46(3):192-194.
[5]宋立.膝关节内外翻预防与治疗[J].运动医学杂志. 2015(15):441-443
[6]https://zhuanlan.zhihu.com/p/30322927
[7]胡祖杰.儿童X型腿、O型腿的评估与治疗进展[J].现代医药卫生,2013,29(10):1512-1513.DOI:10.3969/j.issn.1009-5519.2013.10.034.

说到腿型发育比较有典型特征的有X型腿和O型腿,宝宝在刚刚学走路时,走路的姿势或多或少都有点像O型腿,另外宝宝过早的学习走路会对腿部的肌肉造成严重的压迫,双腿承受压力,会容易变形。所以家长要通过科学的判断,来说明宝宝腿型发育是否正常。
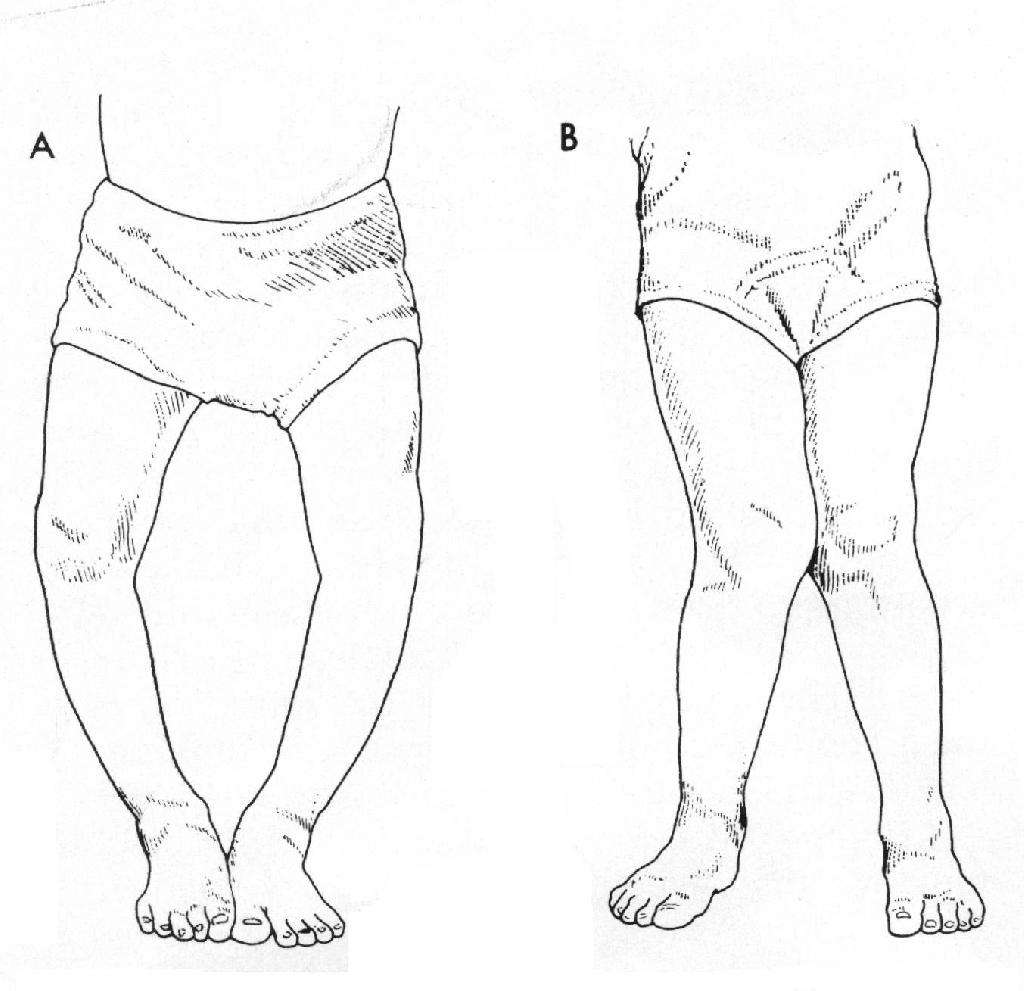
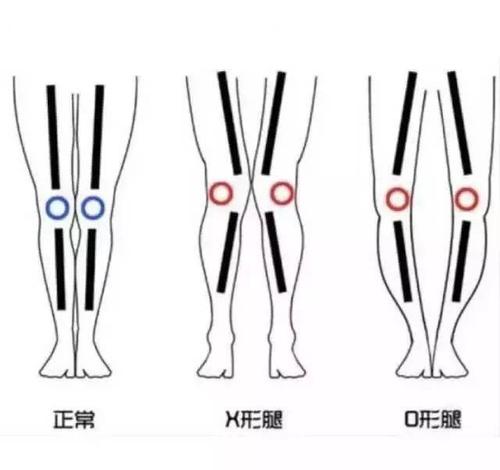
O型腿:而O型腿医学上称为”膝内翻”,是指膝关节内翻畸形,是以两下肢自然伸直或站立时,两足内踝能相碰而两膝不能靠拢为主要的表现。
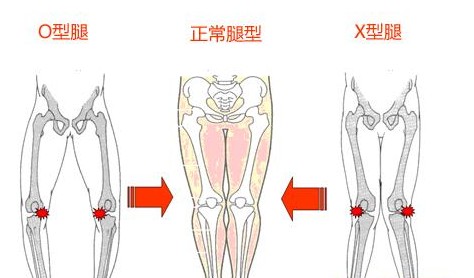
X型腿:“X型腿”的学名是膝外翻,是膝关节外翻畸形,指两足并立时,两侧膝关节碰在一起,而两足内踝无法靠拢。让宝宝平躺着在床上,脱掉裤子和纸尿裤,使宝宝双膝自然并拢,看两个脚踝之间的距离,如果这个距离小于3厘米则是正常情况,如果在3~6厘米可以继续在观察一段时间,而大于6厘米则可能会是X型腿的征兆。

但宝宝的腿型都会经历一个发育的过程,在一到两岁宝宝的腿型可能会是O型腿,便于宝宝学习走路,在两到三岁时O型腿会消失,由于骨骼的发育,可能会膝外翻,变成X型腿,到7岁左右腿型会恢复成正常,所以也要根据宝宝的年龄来判断腿型是否正常。

1、不要过早的学习走路,有的家长看到别的孩子跟自己的孩子年龄一样大或者小,都已经学会了走路,心中难免有点焦急,但每个宝宝腿部力量的发育都不一样,家长切不可拔苗助长。

2、不正确的坐姿,儿童的坐姿经常喜欢一个跪坐的姿势W型腿,这种情况下往往会加重他这种膝外翻畸形。家长发现宝宝有这种姿势的话要即时纠正。
3、不要对学步车产生依赖,家长可能会觉得学步车比较方便,但这会影响宝宝的走路姿势站在这样的车中,孩子的双腿会时不时的分开,时间长了容易形成X型腿或O型腿。此外,时间长了孩子会对学步车产生依赖,不利于腿部肌肉的正常发育。宝宝形成O型腿X型腿还有很多其他的因素,比如宝宝患有佝偻病,所以在早期要合理足量的补钙。
如果宝宝真的形成O型腿X型腿,家长千万不要自己矫正,例如绑住宝宝的双腿,一定要带宝宝去看医生,在医生的指导下科学的矫正宝宝的腿型。

稍微大一点的孩子我们可以通过运动来辅助改善“O”型腿,矫正方法具体如下:
【1】直立,两脚并拢,两手扶膝做两膝向正前方的下蹲,起立运动,做 20~3O次.
【2】弯腰,两手扶膝做向左的和向右的绕环运动,做20~30次.
【3】两脚开立稍大,弯腰,两手扶膝做两膝向内相靠练习,每次坚持10秒钟,做5~10次.
【4】两脚平行站立.先以脚跟为轴,做脚尖外展和内旋运动;再以脚尖为轴,做脚跟外展和内旋运动,各做20~30次.
【5】坐在椅子上,尽力用小腿夹住书,坚持一定时间.如果用橡皮带将两膝捆住做,效果更加显著.
【6】跪坐在腿上,塌腰,两脚慢慢向外向前移动,腰部随之也逐渐直起来.做 15~20次.

关注营养 关爱健康 健康一生相随。
感谢平台让我们相遇,感谢有您的关注、转发、点赞和评论,更多营养和教育问题可以与我交流。让育儿更轻松,让教育更有效 ,我将继续带来更多精彩内容。
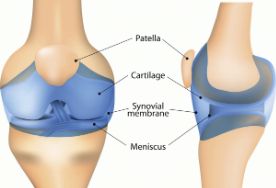
X 型腿或 O 型腿,使用专用定做支具通过佩戴后,根据患者的畸形角度大小,及大腿,小腿的周长调整支具的长度,宽度,角度,逐步使膝关节适应支具的改变!
1. 初次佩戴前需检查 X 片,确定支具合适,同时第一天开始,第一天天佩戴一小时,或半小时!然后每天增加半小时!一个月食时,骨科门诊复查,检查支具的合适情况,是否需要及时调整!
2. 每三个月调整一次,以适应膝关节的矫正状态,内衬需要垫棉布防止压伤。尽可能选择定制类型的支具。定制类型的支具可以根据患者的下肢长度,肢体的周长进行匹配,随着后期的可调性能达到最满意的治疗效果。
3. 加强下肢力量练习,如单腿站立,垫脚尖!同时给孩子补充足量的钙及维生素 D!
4. 出现任何问题,包括皮肤受压,感觉麻木,孩子不配合,请及时联系医生复诊检查!

O 型腿与 X 型腿是儿童较常见的下肢畸形,也是患儿家长们最担心的问题之一。
O 型腿在医学上又称膝内翻,主要表现有双下肢向外弯曲,双膝之间距离增宽,走路摇摆;平卧位时,下肢伸直,髌骨向正上方,双侧内踝并拢时,双膝之间存在距离,距离越大,内翻越重。
“X”形腿又称膝外翻,主要表现有走路时双膝相互碰撞,容易跌倒,足趾向内偏;平卧位,下肢伸直,髌骨向正上方,双膝并拢时,双侧内踝之间存在距离,距离越大,外翻越重。
膝内外翻的成因分为生理性与病理性两类。
- 儿童期大多数的膝内外翻为生理性的。
- 小儿正常发育过程,如果不出现任何的干扰因素,随站立和运动的发育,下肢向内弯曲能够自动地矫正。
- 生理性的膝内外翻一般不必进行特殊的治疗,随负重和骨骼的发育将会自动纠正。
- 还有一种为病理性膝内外翻,病因主要有佝偻病、外伤、炎症、脑瘫等,均可造成膝内、外翻畸形。
严重的膝内外翻如不及时矫正,将会影响双下肢外观、行走步态,并影响下肢力线异常,早期出现骨性关节炎,致关节长期疼痛及活动障碍。
病理性膝内外翻通常不能自行纠正,且程度较严重,一般在治疗原发病的基础上再行手术干预。
经临床实践证明,像按摩及支具等保守治疗一般无效,通常需手术干预。
以往多行截骨矫形手术治疗,此治疗方法虽然技术成熟,且效果满意,但是创伤大、出血多、骨折愈合时间长,患儿需经历长期的痛苦。
目前的新技术是 8 字钢板单侧骺板阻滞术,它是通过阻滞一侧骺板的生长,通过另一侧骺板的自然生长,逐渐纠正畸形,它克服了截骨矫形术的缺点,不但手术切口小、创伤小、出血少,而且术后即可下地活动,恢复正常生活,患儿及家长容易接受,矫正角度可以在动态观察中得到控制,几乎适合于所有生长发育期儿童。
但如果患儿过了青春期,比如男孩出现遗精,女孩已来月经,那么就错过了此方法的最佳治疗时间,则可能需行截骨矫形才能达到治疗目的。
所以,家长需关注小孩的生长发育情况,如发现其肢体发育跟其他同龄小孩不一样,则及时来骨科就诊,以免延误最佳的治疗时机。
当地时间9月12日,FDA批准首个皮下注射抗PD1免疫疗法,用于特定类型肺癌、肝癌、黑色素瘤、软组织癌。这个皮下疗法组合包括两部分组成:一部分是阿替利珠单抗;另一个是 Halozyme公司自己研制的重组人透明质酸酶rHuPH20[1]。
皮下疗法应用Halozyme的ENHANZE药物递送技术,可将原本30mim的静注时间缩短为7min。让我们一起来看支撑这项研究背后的临床试验结果。
相似的血药浓度、有效性和安全性
该获批基于一项随机多中心 Ib/III 期的试验,研究的主要目的要看看阿替利珠单抗这个药,打在皮下和打在静脉里在一些特定患者身上效果有什么不一样。这些特定患者为局部晚期或者已经转移的非小细胞肺癌患者,他们之前没做过癌症免疫治疗,而且之前用含铂类的药治疗也没效果。
试验的主要结果显示,皮下注射atezolizumab和静脉注射 atezolizumab 的几何平均比值 (GMR) 为1.05 (90% CI,0.88-1.24),AUC 0-21 天为 0.87 (90% CI,0.83-0.92),这表明皮下注射可以达静脉注射相当的血药浓度。有效性方面,皮下和静脉的总缓解率 (ORR) 、无进展生存期 (PFS) 和总生存期 (OS) 数据相似[2]。
安全性方面,最常见的任何级别不良反应是疲劳、肌肉骨骼疼痛、咳嗽、呼吸困难和食欲下降。
关于阿替利珠单抗
根据FDA获批信息,该药适应证如下,本次的获批主要是制剂类型的不同。
适应证[3]
1. 非小细胞肺癌(NSCLC):
- 单药用于经手术及含铂化疗后的Ⅱ至ⅢA期NSCLC成人患者辅助治疗(肿瘤细胞PD-L1表达≥1%)。
- 单药一线治疗高表达PD-L1、无EGFR或ALK畸变的转移性NSCLC成人患者。
- 与贝伐珠单抗等联合用于无EGFR或ALK畸变的转移性非鳞状NSCLC成人患者一线治疗。
- 单药治疗含铂化疗期间或后进展的转移性NSCLC成人患者(有EGFR或ALK畸变患者应在对应FDA批准疗法进展后使用)。
2. 小细胞肺癌(SCLC):与卡铂和依托泊苷联合用于广泛期SCLC成人患者一线治疗。
3. 肝细胞癌(HCC):与贝伐珠单抗联合用于未接受全身治疗的不可切除或转移性HCC成人患者。
4. 黑色素瘤:与考比替尼和维莫非尼联合用于BRAF V600突变阳性的不可切除或转移性黑色素瘤成人患者。
5. 肺泡软组织肉瘤(ASPS):单药用于2岁及以上不可切除或转移性ASPS成人及儿童患者。
关于Halozyme[4]
Halozyme 是一家生物制药公司,致力于提供颠覆性解决方案,以改善新兴和成熟疗法的患者体验和结果。作为采用专有酶 rHuPH20 的 ENHANZE药物输送技术的创新者,Halozyme 经过商业验证的解决方案用于促进注射药物和液体的皮下输送,目的是通过快速皮下输送和减轻治疗负担来改善患者体验。
Halozyme 已在全球 100 多个市场的 8 种商业化产品中触及超过 800,000名患者的上市后使用,其 ENHANZE技术已授权给领先的制药和生物技术公司,包括罗氏、武田、辉瑞、杨森、艾伯维、礼来等。
参考文献:
1.Halozyme Announces FDA Approval of Roche's Tecentriq Hybreza™ With ENHANZE® for Multiple Types of Cancer
2.FDA Approves Subcutaneous Atezolizumab and Hyaluronidase-tqjs for Use in All Indications of IV Atezolizumab
3.Product information:.TECENTRIQ- atezolizumab injection, solution
4.https://ir.halozyme.com/news/news-details/2024/Halozyme-Announces-FDA-Approval-of-Roches-Tecentriq-Hybreza-With-ENHANZE-for-Multiple-Types-of-Cancer/default.aspx

2024年9月10日,诺和诺德一项减肥研究登顶《新英格兰医学杂志(NEJM)》,公布了胰高血糖素样肽-1(GLP-1)受体激动剂利拉鲁肽在儿童中的减重数据:利拉鲁肽组近一半参与者BMI降低 5%以上。让我们一起来看看这项儿童减肥药的研究。
火锅烤肉、奶茶饮料等诱惑层出不穷,让不做选择的成年人慢慢走上了肥胖之路。而我们祖国的花朵,面对这些,也茁壮成长成了“小胖子”。据统计,我国6~17岁、6岁以下儿童和青少年超重/肥胖率分别达到19.0%和10.4%[1]。
孩子肥胖与很多疾病息息相关,如2型糖尿病、脂肪性肝炎、多种癌症。除了引导健康饮食和规律的生活方式[2],一些药物选择对于超重儿童提供了选择。
虽然经常提到司美格鲁肽、利拉鲁肽,但是其在儿童中的安全性一直引人担忧,于是就有了NEJM这个研究。这个研究是一项双盲随机对照试验。试验分为利拉鲁肽组和对照组,参与者每日一次注射药物,在4-5周内每周剂量递增,直至达到最终剂量[3]。试验有效性结果主要看参与者BMI变化百分比。
共有 82 名参与者接受了随机分组;56 人被分配至利拉鲁肽组,26 人被分配至安慰剂组。
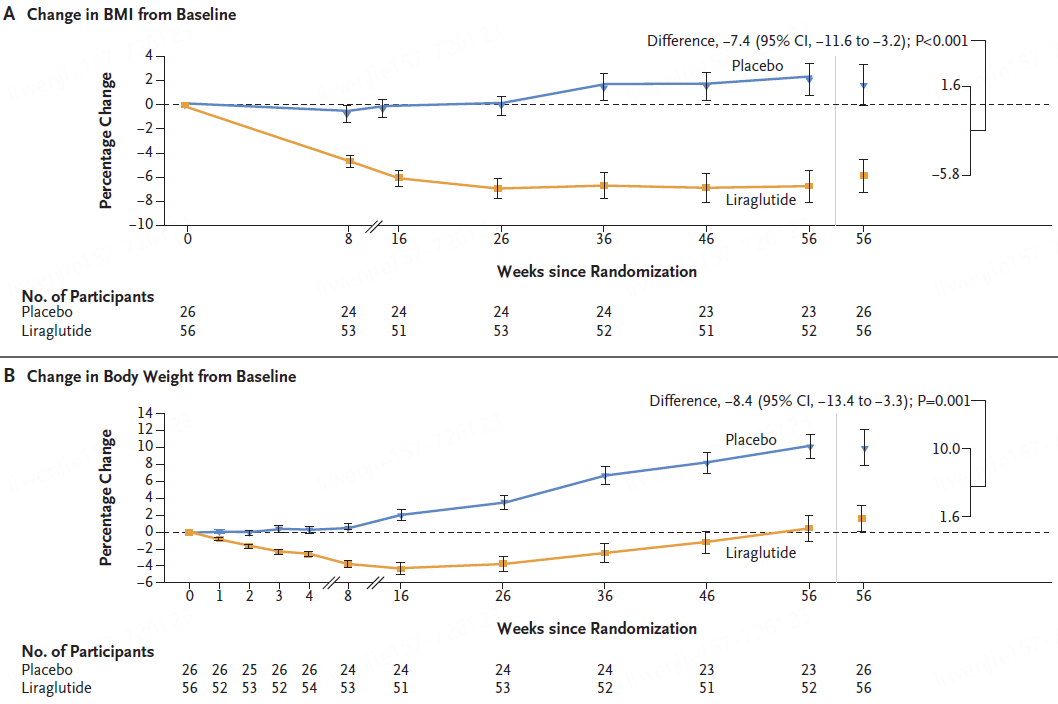
试验结果表明,在第 56 周时,利拉鲁肽组BMI较基线的平均变化百分比为 - 5.8%,安慰剂组为 1.6%。
利拉鲁肽组体重的平均变化百分比为 1.6%,安慰剂组为 10.0%。
利拉鲁肽组46%的参与者BMI降低至少5%,而安慰剂组为 9%(调整后的优势比为 6.3 [95% CI,1.4 至 28.8];P = 0.02)。
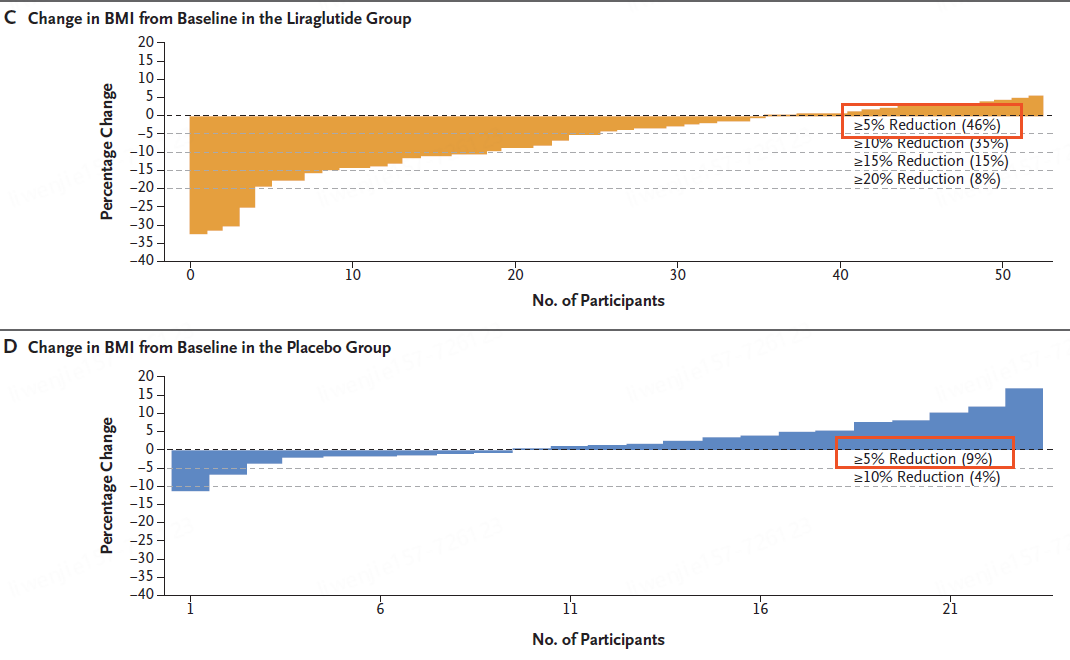
利拉鲁肽组和安慰剂组分别有 89% 和 88% 的参与者发生不良事件。胃肠道不良事件在利拉鲁肽组更为常见(80% vs 54%);利拉鲁肽组和安慰剂组分别有 12% 和 8% 的参与者报告了严重不良事件。
关于利拉鲁肽
利拉鲁肽(VICTOZA)的已获批适应症包括:
作为饮食和运动的辅助手段,用于改善 10 岁及以上成人和儿童 2 型糖尿病患者的血糖控制。
降低已确诊心血管疾病的成人 2 型糖尿病患者发生主要不良心血管事件(心血管死亡、非致命性心肌梗死或非致命性中风)的风险。
说明书也也发布了黑框警告信息:
本品禁用于有甲状腺髓样癌个人或家族史的患者以及患有 2 型多发性内分泌腺瘤综合征(MEN 2)的患者。应告知患者使用本品可能存在的甲状腺髓样癌风险,甲状腺肿瘤的症状包括颈部肿块、吞咽困难、呼吸困难、持续性声音嘶哑。
关于诺和诺德[5]
诺和诺德是一家全球领先的医疗保健公司,成立于1923年,总部位于丹麦。其的宗旨是在糖尿病领域的传统基础上,推动变革以战胜严重的慢性疾病。诺和诺德通过开创科学突破、扩大药品的可及性以及致力于预防并最终治愈疾病来实现这一目标。诺和诺德在80个国家拥有约 69,000名员工,产品在大约170个国家销售。
参考文献:
1.中国超重/肥胖医学营养治疗指南(2021)
2.Fox CK, Barrientos-Pérez M, Bomberg EM, Dcruz J, Gies I, Harder-Lauridsen NM, Jalaludin MY, Sahu K, Weimers P, Zueger T, Arslanian S; SCALE Kids Trial Group. Liraglutide for Children 6 to <12 Years of Age with Obesity - A Randomized Trial. N Engl J Med. 2024 Sep 10. doi: 10.1056/NEJMoa2407379. Epub ahead of print. PMID: 39258838.
3.SCALE KIDS: Research Study to Look at How Well a New Medicine is at Lowering Weight in Children With Obesity
4.Product information:VICTOZA- liraglutide injection
5.https://www.novonordisk.com/

在 2024 年世界肺癌大会上,一项关于局部晚期或转移性 ROS1 阳性非小细胞肺癌(NSCLC)的试验公布了数据,这是一项多中心Ⅱ期试验,试验药物是新一代酪氨酸激酶抑制剂(ROS1 TKI)taletrectinib,在试验中的代码是AB - 106[1]。
总体缓解率达85.2%,亚洲患者达87.9%
试验的主要结果是客观缓解率(ORR),最长时间为 4 年,入组患者根据既往接收ROS1 TKI治疗的情况分为两组,一组既往胃接受,另外一组接受过[2]。从试验的结果来看,未接收过这类药物治疗ORR比例更好,达85.2%。详细数据如下所示:
- 先前未接受过 ROS1 TKI 治疗的患者(n = 54),经过中位随访 15.8 个月(范围 3.6 - 29.8),taletrectinib 展现出了较好疗效,确认总体缓解率(cORR)高达 85.2%(95%CI,72.88% - 93.38%)。值得一提的是,亚洲患者(n = 33)与非亚洲地区患者的 cORR 相近,分别为 87.9%(95%,71.80% - 96.60%)和 81.0%(95%CI,58.09% - 94.55%)。
- 先前接受过 ROS1 TKI 治疗的患者中(n = 47),中位随访 15.7 个月(范围 3.9 - 29.8),taletrectinib 的 cORR 也达到了 61.7%(95%CI,46.38% - 75.49%)。亚洲患者(n = 21)与其他地区患者(n = 26)的 cORR 分别为 57.1%(95%CI,34.02% - 78.18%)和 65.4%(95%,44.33% - 62.79%)。
- 在基线时有可测量脑转移的患者中,评估颅内反应显示,初治组(n = 9)的颅内客观缓解率(IC - ORR)为 66.7%(95%CI,29.93% - 92.51%),其中完全缓解(CR)率为 22.2%,部分缓解(PR)率为 44.4%[1]。
最常见不良反应为肝药酶升高
导致剂量减少的治疗出现的不良事件(TEAEs)发生在 37.1%的患者中,其中 16.4%是由于肝酶升高。导致治疗中断的 TEAEs 报告在 7.5%的患者中;其中 1.3%被认为与治疗相关。没有报告导致死亡的 TEAEs。
其他不良反应发生率如下:
- 至少 15%的患者(n = 159)中最常见的 TEAEs 是丙氨酸氨基转移酶升高(任何级别,67.9%;≥3 级,15.1%),天冬氨酸氨基转移酶升高(67.3%;6.9%),腹泻(56.6%;0.6%),恶心(51.6%;1.9%),呕吐(33.3%;1.3%),便秘(25.2%;0.0%),贫血(20.1%;4.4%),味觉障碍(19.5%;0.0%),血肌酸磷酸激酶升高(18.2%;3.8%),头晕(17.0%;0.0%)和 QT 延长(15.1%;3.1%)[2]。
Taletrectinib是何许药物?
最后再回到taletrectinib,这个药作为新一代 ROS1 TKI 药物,在TRUST - II 试验中表现确实亮眼。
由于对 ROS1+肿瘤有着更高的效力,taltrectinib 能够提升患者无进展生存期(PFS),同时这个药物的中枢神经系统(CNS)渗透率也更高,药理机制上,可以有选择性地抑制 ROS1 野生型以及其对 TRKB 的耐药突变;与其他 ROS1+抑制剂相比,taltrectinib 的安全性更优,并且与中枢神经系统相关的不良事件(AE)极少[3]。
参考文献
1.Taletrectinib Shows Consistent Efficacy, Safety in ROS1+ NSCLC Independent of Prior TKI Exposure
2.Taletrectinib Phase 2 Global Study in ROS1 Positive NSCLC (TRUST-II)
3.Nagasaka M, Brazel D, Ou SI. Taletrectinib for the treatment ofROS-1positive non-small cell lung cancer: a drug evaluation of phase I and II data. Expert Opin Investig Drugs. 2024 Feb;33(2):79-84. doi: 10.1080/13543784.2024.2305131. Epub 2024 Jan 29. PMID: 38224083.

近期Merck宣布其正在进行的IDeate-Lung01 Ⅱ 期试验结果积极,试验主角ifinatamab deruxtecan(I-DXd)用于治疗广泛期小细胞肺癌(ES-SCLC),在入组患者中,12mg/kg I-DXd 1的客观缓解率(ORR)为 54.8%[1]。

IDeate-Lung01是一个多中心随机开放研究,主要结果:在广泛期小细胞肺癌(ES-SCLC)患者中,使用I-DXd治疗后的客观缓解率(ORR)百分比,试验最长约 36 个月[2]。
这里的客观缓解率就是在参与试验的人中,达到最佳总体缓解的人所占的百分比,“总体缓解”指的是经确认的完全缓解或者部分缓解。对于所有的靶病灶、非靶病灶和新出现的病灶来说,完全缓解就是所有的病灶都消失了;部分缓解就是所有病灶直径的总和至少减少了 30%。
疾病控制率高达90.5%,客观缓释率达54.8%
经盲态独立中心审查(BICR)评估,在接受I-DXd治疗的广泛期小细胞肺癌患者中,12mg/kg 队列(n = 42)的确认客观缓解率(ORR)为 54.8%(95%置信区间:38.7 - 70.2),8mg/kg 队列(n = 46)为 26.1%(95%置信区间:14.3 - 41.1)[1]。

在 12mg/kg 队列中观察到 23 个部分缓解(PR)。在 8mg/kg 队列中观察到 1 个完全缓解(CR)和 11 个部分缓解。
在 12mg/kg 和 8mg/kg 队列中,分别观察到中位缓解持续时间(DoR)为 4.2 个月(95%置信区间:3.5 - 7.0)和 7.9 个月(95%置信区间:4.1 - 未确定),疾病控制率(DCR)为 90.5%(95%置信区间:77.4 - 97.3)和 80.4%(95%置信区间:66.1 - 90.6)。
12mg/kg 剂量的中位治疗持续时间为 4.7 个月(0.03 - 15.2),8mg/kg 剂量为 3.5 个月(0.03 - 13.9)。在 12mg/kg 和 8mg/kg 队列中,分别观察到中位无进展生存期(PFS)为 5.5 个月(95%置信区间:4.2 - 6.7)和 4.2 个月(95%置信区间:2.8 - 5.6),中位总生存期(OS)为 11.8 个月(95%置信区间:8.9 - 15.3)和 9.4 个月(95%置信区间:7.8 - 15.9)。
12mg/kg 剂量已被选定用于试验的剂量第二部分。截至 2024 年 4 月数据截止时,12mg/kg 队列的中位随访时间为 15.3 个月(95%置信区间:13.6 - 16.2),8mg/kg 队列为 14.6 个月(95%置信区间:13.4 - 16.5)。 在有脑靶病灶的患者中,经中枢神经系统(CNS)BICR 评估,在 12mg/kg 队列(n = 10)和 8mg/kg 队列(n = 6)中分别观察到颅内客观缓解率为 50.0%(95%置信区间:18.7 - 81.3)和 66.7%(95%置信区间:22.3 - 95.7)。在这些患者中,每个队列中均观察到两个颅内完全缓解。
安全性数据
12mg/kg 队列中 50.0% 患者发生 3 级或更高等级治疗中出现的不良事件,8mg/kg 队列中 对应比例达43.5% 。两种剂量下常见治疗相关不良事件有恶心、食欲下降、贫血、中性粒细胞减少、白细胞减少和乏力等。
12mg/kg 和 8mg/kg 剂量下分别有五例和四例间质性肺病、肺炎事件被确认为与治疗相关,多数为低级别。12mg/kg 和 8mg/kg 队列中因不良事件导致的治疗中断分别为 16.7% 和 6.5%。
关于I-Dxd
I-Dxd是一种首创 B7-H3 靶向抗体药物偶联物(ADC),与第一三共开发的其他抗体药物偶联物(一样,向癌细胞递送相同的毒性有效载荷。I-Dxd靶向一种B7-H3 的蛋白质,该蛋白质在包括前列腺癌和食管癌在内的多种癌症中过度表达[3]。
参考来源:
1.Ifinatamab Deruxtecan Continues to Demonstrate Promising Objective Response Rates in Patients with Extensive-Stage Small Cell Lung Cancer in IDeate-Lung01 Phase 2 Trial
2.Ifinatamab Deruxtecan (I-DXd) in Subjects With Pretreated Extensive-Stage Small Cell Lung Cancer (ES-SCLC) (IDeate-Lung01)
3.Merck, Daiichi Sankyo detail Phase 2 ADC results in small cell lung cancer, bispecific combo strategy

2024年9月5日,Vor Bio公布了其1/2 期 VBP101 试验的临床数据,VBP101主要评估干细胞疗法 tremtelectogene empogeditemcel(trem - cel)与 CD33 靶向抗体偶联药物(ADC)Mylotarg 联用用于治疗复发/难治性急性髓系白血病(AML)患者的效果[1]。
干细胞移植后白血病复发风险
虽然患者进行了造血干细胞移植(HCT),但高风险急性髓系白血病(AML)和骨髓增生异常综合征(MDS)仍经常复发。HCT后的靶向治疗可减少复发,但会对植入细胞产生毒性限制。
VOR33 是一种异基因 CRISPR/Cas9 基因组编辑的造血干细胞和祖细胞(HSPC)治疗产品,缺乏 CD33 蛋白,这个试验正是对 HCT 后复发风险高的 CD33 + AML 或 MDS 患者进行研究,以便在 HCT 后使用 Mylotar靶向残留的 CD33 + 急性 AML 细胞,从而避免对植入的 VOR33 细胞产生毒性。
参与者将接受HCT植入,植入后将接受 Mylotarg治疗,治疗周期≤4个周期。评估 VOR33 安全性的主要终点是 28 天成功植入的发生率。研究将首先评估递增 Mylotarg剂量水平的安全性,以确定最大耐受剂量(MTD)和推荐的 2 期剂量(RP2D)。后续将进一步扩大参与者数量,以评估 Mylotarg的 RP2D[2]。
100%植入,无复发生存期改善
公布的数据包括 18 名接受 trem - cel 治疗的患者,截至 2024 年 7 月 19 日的数据截止日期,其中 10 名患者接受了 Mylotarg 治疗。详细数据如下[1]:
可靠的植入效果:100% 的患者实现了初级中性粒细胞植入(中位时间为 9 天)和强劲的血小板恢复(中位时间为 16.5 天)。在第 28 天,CD33 编辑效率高(中位数为 89%,范围为 71 - 94%),并且实现了完全的髓系嵌合。
血液系统的屏障:不同 Mylotarg 剂量( 0.5、1和 2mg/平方米)下,中性粒细胞和血小板计数保持稳定。
Mylotarg 治疗指数的拓宽:药物暴露由 AUC 表示,与疗效相关,与标记的 Mylotarg 剂量一致;最大浓度由 Cmax 远低于已知的毒性范围。
早期证据表明患者受益:与已发表的高危 AML 对照者相比,在无复发生存期方面,患者受益。
VBP301 研究将继续招募患者,继续关注其试验目的。预计今年年底,Vor Bio计划与FDA讨论trem - cel与Mylotarg联合用药的关键试验设计。
Vor Bio 是一家扔处于临床阶段的细胞和基因组工程公司,其多条管线扔处于临床研究阶段(详见图片),旨在通过对造血干细胞进行工程改造,使移植后的靶向治疗成为可能,从而改变血癌患者的护理标准。
参考文献:
1.New Clinical Data Validates Vor Bio’s Approach of Using Shielded Transplants to Deliver Targeted Therapies
2.Allogeneic Engineered Hematopoietic Stem Cell Transplant (HCT) Lacking the CD33 Protein, and Post-HCT Treatment With Mylotarg, for Patients With CD33+ AML or MDS
展开更多














