
良性钙化原来是长这样的……
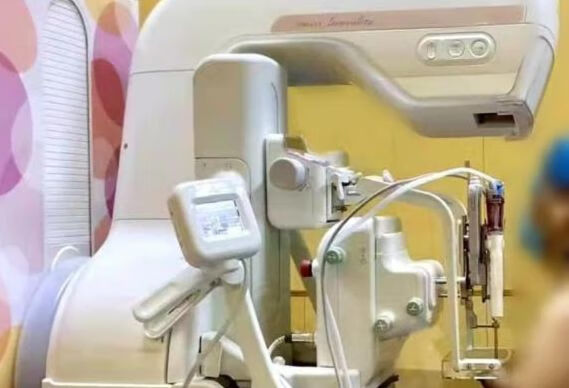
视频主要两部份组成,前半部分介绍设备及乳腺目标钙化的立体定位操纵,后半部分展示了立体定位后真空辅助乳腺钙化微创活检实际操作过程。该操作目前仅少数大型乳腺中心能完成,此视频也是目前全网能检索到的唯一操作实景视频。

乳腺钼靶检查是目前全世界公认的应用于大范围人群乳腺癌筛查的最主要的影像学检查项目,乳腺钼靶检查同时也是针对乳腺钙化最敏感的检查手段,甚至有时钙化是临床现有的乳腺癌检查手段所能发现的唯一征象。
钙化成份 按化学成分可以分为两种类型。 I 型钙化以二水草酸钙为主, 是分泌产生的, 多发现在囊性增生性病变中, 很少有恶变; II 型钙化以羟基磷灰石为主, 它是磷酸钙盐的一种, 多出现在增生性的病变中, 既可能是良性的, 也可能是恶性的。 II 型钙化比I型更为常见, 约是 I 型的2 ~ 3 倍。目前为止,乳腺钼靶检查无法区分 I 型和 II 型乳腺钙化。
并非所有的钙化都是恶性的,也并非所有的钙化需要有创活检,研究表明可疑恶性乳腺钙化最后活检证实为恶性的概率在 10 ~ 20% 。乳腺钙化的风险程度需要结合 钙化形态与钙化分布综合判断。
钙化形态
一 良性钙化
① 皮肤钙化
② 血管钙化
③ 爆米花样钙化
④ 点状钙化
⑤ 空心钙化
⑥ 杆状钙化
⑦ 钙乳沉积钙化
⑧ 缝线钙化
⑨ 蛋壳样
⑩ 营养不良性钙化
二 可疑钙化
① 无定形钙化
② 粗大的不均匀钙化
三 恶性钙化
① 细小多形性
② 细小线样或分枝状
钙化分布
⑴ 弥漫或散在分布
⑵ 区域状分布是指较大范围内分布的钙化( > 2cm3 );
⑶ 段样分布常提示病变来源于一支导管及其分支, 也可能发生在一叶或一个段叶上的多灶病变;
⑷ 成簇分布是指至少有 5 枚钙化占据一个较小的空间( <1cm3) ;
⑸ 线样分布的钙化排列呈线形,可见分支点。
微钙化 ,指直径通常小于5毫米的钙化灶, 一直被认为是乳腺癌早期检出及诊断的重要证据之一。
1984 年 Le Gal 等依据形态学特点把微钙化分为 5 型,得到行业内广泛认可:
1 型钙化(典型良性钙化):环形, 100% 良性
2 型钙化:形态规整的点状, 22% 恶性
3 型钙化:细沙样, 40% 恶性
4 型钙化:形态不规整的点状 66% 恶性
5 型钙化(典型恶性钙化):蠕虫样 100% 恶性

对于可疑恶性的钙化,需要活检明确诊断,现有乳腺钙化诊断手段:
- 钙化钼靶体表投影定位后开放活检
- 超声引导下钙化穿刺 / 真空辅助活检
- 乳腺钼靶钙化立体定位下真空辅助活检
- 乳腺钼靶钙化立体定位开放活检
其中乳腺钼靶钙化立体定位手术需专业的设备,多学科联合,目前仅少数区域医疗中心开展,优点为提高钙化切取的成功率,缩短手术时间,且对乳房外形影响较小,患者满意度高。

乳腺癌的发病率已经是全球癌症发病率首位,也是女性癌症死亡的首要原因。有些乳腺癌灶在最初形成时, 是以钙化灶为主要表现的,此时可能肿块尚未形成。详见我的文章《早期乳腺癌的四大表现及相应症状》。
钼靶是检查乳腺钙化最灵敏的手段,远超过 B 超和磁共振。对于 BI-RADS 分级 4a(风险为 2-10%)及以上级别的钙化,建议钙化灶活检。详见我的文章《彩超和钼靶有何不同?哪一个检查更好?》。
什么样特征的钙化灶的 BI-RADS 分级在 4a 及以上?我在文章《如何对待钼靶上的钙化灶》里较详细讲解了从钙化的分布和钙化的形态两方面来判断恶性风险的大小。总的来说,钙化灶分布上越密集,形态上越细小,BI-RADS 分级越高,越需要手术。
但临床上会遇到一种情况:钙化灶是比较细小,但分布弥漫整个乳房或大半个乳房。放射科医生给出的 BI-RADS 分级有时是 4a 级,少数情况下是 3 级。这种情况如何判断癌的风险大小?如何活检?
一、诊断的难点
前面说过,评判钙化灶恶性程度最基本的两个特征,钙化的分布和钙化的形态,两两组合有四种情况:细小密集钙化很容易评判为 BI-RADS 高分级,建议活检;粗大广泛钙化很容易评判为 BI-RADS 低分级,建议随访;粗大而密集,可以理解为爆米花样钙化,一般也是 BI-RADS 低分级,可以选择随访;最难的就是细小广泛钙化,很难判断其恶性风险等级。其中尤其是钙化灶密度较大的病例最为困难。
这种广泛密集细小钙化灶,单独观察某一个局部,可以认为是典型的细小密集钙化灶,容易得出 BI-RADS 高分级结论,建议活检。但乳腺里广泛如此,总不能把所有的细小密集钙化区域都切出去活检吧?这样的话,整个乳房,至少是大半个乳房都得切除。如果最终结果是乳腺癌倒也罢了,如果是良性的,患者肯定难以接受的。
二、“法不责众”
这时候的诊断思路,需要先明白个前提,再做个假设,用反证法得出结论。前提:细小密集的钙化,一般是 BI-RADS 4a 或 4b 的分级,即便是 4b,活检结果不是癌的可能性是 50-90%。也就是说,大多数情况下都是良性的。假设:如果乳腺内如此细小密集处都是乳腺癌,那么应该钙化所分布区域都是乳腺癌,也就是整个乳房或大半个乳房都是乳腺癌。反证法:如果是如此严重的乳腺癌,医生触诊时基本上就已觉察出乳腺明显异常,和对侧乳房的显著手感的差别。也很难逃过 B 超磁共振的眼睛。因此,假设不成立,可认为癌的可能性很小。
需要说明两点: 1,放射科医生吧这么密集细小的钙化只打 3 级或 4a 级,其实已经无意间运用来了上述的反证法思路。2,反证法推翻假设是,触诊和 B 超磁共振等检查不可能漏掉如此严重的乳腺癌,不管是否经验丰富的医生触诊,都建议加做 B 超或磁共振确认是否有乳腺癌。
三、注意“众”中的“佼佼者”
前面反证法推理中有句话:如果乳腺内如此细小密集处都是乳腺癌,那么应该钙化所分布区域都是乳腺癌。这里面有个隐含的前提,就是细小密集的钙化在整个乳房内是处处相似的。如果看起来如此均匀的钙化,在某个局部有与众不同之处,是“众”中的“佼佼者”,就需要区别对待了。有如下一些情况:
- 钙化灶的密集程度是有差别的,如果钙化灶总体上广泛而比较密集,而某个局部特别密集,显著和周边区域不一致。要引起重视。
- 除了细小密集这两个乳腺癌的常见钙化特征外,钙化灶多形性也很重要。如果广泛细小钙化灶中,某个局部钙化灶点状、三角状、小分支状等各种形态都有,这种多形性钙化要特别对待。
- 在随访复查中发现,某个区域的钙化较前明显程度加重,而其他区域钙化无明显变化,这也要引起重视的。对于这些情况,有经验的放射科医生可能给出 4b 及以上的级别,并指出其具体的位置。就算放射科没有特别指出,临床医生自己读钼靶图像也需要引起警惕。
四、决策总结
对于乳腺广泛细小密集钙化灶的钼靶影像,需要仔细看一下有没有特别密集区或多形性明显区,如果有,建议该区域活检。
如果整体上一致性很高,触诊无特殊,建议加做 B 超或磁共振,如无异常选择随访复查钼靶。复查中对钙化形态变化明显的区域需要及时活检,没有变化继续复查。
如 B 超磁共振显示有 BI-RADS 4 及病灶,要对所示病灶及其所处的钙化区域活检,可结合钼靶钙化灶图像,适当扩大活检范围以取到更多钙化灶。
每次体检或者在检查过程中医生提到有“钙化”点,都会让很多人感到担心,甚至害怕,而乳腺钙化就是其一。

那么乳腺钙化到底有多可怕呢?
首先,乳腺钙化往往来源于我们女性的乳腺X线检查报告中,也就做钼靶检查,是目前女性乳腺癌重要筛查手段之一,相比其他检查,钼靶检查对乳腺钙化灶的识别能力极高。因此,要想知道自己的乳腺有没有钙化灶,最好的检查方式就是做钼靶!
其次,注意:我们女性的乳腺的任何部位位置都可以发生钙化灶,钙化就像是我们的沙子,小石头一样沉积在我们女性乳腺的某个特别位置上。
女性发生乳腺钙化的原因有很多。有一部分女性发生钙化就像化石一样,乳腺内坏死细胞物质形成的;而有一些女性是因为哺乳过程中乳汁淤积等浓缩的细胞分泌物形成的结晶;当然,还有一些女性是因为乳腺内的炎症,瘢痕等引起的钙化。
最后,在临床上,乳房钙化以在终末导管和腺泡形成的居多,不过确实也有个别女性乳腺钙化是在乳房间质和乳房皮肤形成的。

不同部位的钙化,良恶性程度确实是有差别的,可怕程度也不一样!
- 导管内钙化多见于恶性肿瘤;
- 乳腺小叶钙化通常是弥漫或散在分布的,多见于乳腺良性病变;
- 乳腺间质、皮肤钙化也多为良性钙化灶。
如果纯属依据钙化形态来判断良恶性的话,大家只要记住细小多形性、线样或线样分支状钙化就要引起大家高度怀疑恶性的了,不然良性可能性大!
但是不管如何,纯属依据钙化形态、具体位置来判断良恶性,还是缺乏足够的证据的,具体良恶性还是必须要由专业的医生来判断的,必要时时必须要进行活检才能判断的,切勿自己过分担心!
而且最主要的一点是:不要因此害怕担心自己被查出钙化灶就不做乳腺钼靶等乳腺癌的筛查,乳腺癌早发现早诊早治可降低30%死亡风险,建议40岁以上女性定期接受钼靶诊断!
而且面对钼靶诊断报告:
第一,不要紧张不要百度,要去寻求专业医生的意见;
第二,相信医生的判断,不是所有的钙化都需要处理,如果医生提示您要重视切不可拖延;
第三,不要相信非专业人士的非专业处理,吃药,按摩疏通都解决不了问题,反应可能会导致病情的进展。

钼靶检查乳腺有钙化点的话,可以在医生的指导下进行乳腺部位的穿刺活检,确定钙化点的病理性质之后,再进行具体的治疗。乳腺钙化点大多数是由于乳腺功能异常,激素分泌异常等原因所导致的乳腺囊肿或者是乳腺结节。乳腺钙化点的患者一定要定期的去医院进行复查,可以做乳腺b超,或者是进行乳腺的病理活检,都可以确定乳腺的病理性质。同时要改变自己的不良生活饮食习惯,不要吸烟喝酒。保持一个良好的心态,尽量不要熬夜劳累。
冻卵,受到了越来越多的关注。但你对冻卵女性了解有多少?她们年龄多大?冻卵后她们又如何使用的?通过1篇荟萃分析我们来一起揭秘。
一、研究方法
研究人员按照系统综述和荟萃分析的首选报告项目(PRISMA)建议进行了系统综述。他们搜索了 PubMed、Scopus 和 Web of Science 从建库到 2021 年 1 月的文献,对发表日期没有限制。纳入的研究需为英文,且研究了计划性冻卵的使用者或潜在使用者的特征、最初信息来源以及卵子处置情况。提取的数据通过主题分析进行分析,纳入研究的方法学质量使用 QualSyst 标准进行评估。
二、研究结果
- 研究筛选情况
- 最初检索到 1074 条记录,其中 29 项研究符合纳入标准,包括 12 项定性研究和 17 项定量研究。调查的回复率在 38% - 85% 之间。
- 女性特征
- 计划性冻卵的使用者或潜在使用者大多为单身、受过高等教育、有工作,平均年龄为 37 岁。
- 信息来源
- 媒体和朋友是计划性冻卵最初知识的最常见来源,而健康专业人员则是较不常见的来源。
- 卵子使用情况
- 大多数计划性冻卵者没有尝试使用冷冻卵子怀孕,但她们并不后悔进行了该过程。
三、讨论与启示
- 人口特征与卵子使用
- 计划性冻卵的大多数使用者或潜在使用者具有特定的人口统计学特征,并且最终大多没有使用她们冷冻保存的卵子。这可能是由于多种原因,比如在冻卵后的生活中,她们的生育计划发生了改变,或者虽然有生育的想法但尚未尝试使用冷冻卵子。
- 卵子处置的选择
- 对于未使用的卵子,存在多种处置方式。可以选择丢弃,这可能是因为女性认为自己不再需要这些卵子,或者缺乏合适的使用途径。也可以选择捐赠给其他女性,为那些有生育困难的女性提供帮助。此外,还可以捐赠给研究机构,用于相关的科学研究,以推动生育医学的发展。
- 对健康专业人员的指导意义
- 了解计划性冻卵潜在使用者的主要特征,健康专业人员可以更加主动地宣传正确的冻卵知识,包括冻卵的风险、成功率以及后续可能面临的问题等。同时,在咨询过程中,也可以根据女性的年龄、婚姻状况和生育计划等因素,提供更加个性化的建议,帮助她们做出更有效的决策。
参考来源:Giannopapa M, Sakellaridi A, Pana A, Velonaki VS. Women Electing Oocyte Cryopreservation: Characteristics, Information Sources, and Oocyte Disposition: A Systematic Review. J Midwifery Womens Health. 2022 Mar;67(2):178-201. doi: 10.1111/jmwh.13332. Epub 2022 Feb 13. PMID: 35156301.
原始卵泡位于卵巢皮质中,处于静止状态。其数量在出生时就已确定(每个卵巢大约 60 万到 100 万个),并在儿童期和整个生育期持续逐渐减少,因为原始卵泡会被募集并离开静止状态。
大多数原始卵泡在初次募集后发生闭锁,无法达到窦状卵泡阶段,只有少数能继续生长直至排卵,在生育期大约排卵 450 次左右,只有极少数卵泡能发育成有受精能力的卵子。当原始卵泡几乎耗尽,只剩下大约 1000 个原始卵泡时,就会导致绝经。
随着女性生育观念的转变以及医学技术的飞速发展,冻卵技术作为一种生育力保存的手段,正逐渐走进大众的视野。这一技术为女性在面临生育挑战时提供了一种可能的解决方案,无论是因为职业发展、个人生活规划,还是由于疾病治疗等原因导致的生育延迟或生育风险增加。
一、冻卵技术的原理与方法
冻卵技术的核心原理是在极低的温度下保存卵子,使其代谢活动几乎停止,从而延长卵子的存活时间。目前主要有两种常见的冻卵方法:慢冻法和玻璃化冷冻法。
慢冻法是一种较为传统的方法,它通过逐步降低温度,让卵子在这个过程中逐渐适应低温环境。在这个过程中,会使用一些冷冻保护剂来减少冰晶的形成,因为冰晶可能会对卵子的结构造成损伤。具体来说,卵子首先在含有一定浓度冷冻保护剂的溶液中进行预处理,然后以相对缓慢的速度降温,经过多个阶段的温度调控,最终将卵子储存于液氮中,温度可达 -196°C。
玻璃化冷冻法则是一种更为先进的技术,它能够在更短的时间内实现卵子的冷冻。这种方法使用了更高浓度的冷冻保护剂,并且通过极快的冷却速度,使卵子在瞬间从液态转变为一种类似玻璃的固态,从而避免了冰晶的形成。玻璃化冷冻法在保护卵子的结构和功能方面具有一定的优势,因此近年来受到了越来越多的关注和应用。
二、冻卵技术的适用人群与临床应用
- 癌症患者的生育力保存 对于许多癌症患者,尤其是年轻女性,化疗、放疗等治疗手段可能会对卵巢功能造成不可逆的损害,导致生育能力丧失。冻卵技术为这些患者提供了在接受治疗前保存生育能力的机会。例如,在一些血液系统癌症或生殖系统癌症的治疗中,医生会建议患者在开始治疗前考虑冻卵。通过采集卵子并进行冷冻保存,患者在治愈癌症后,如果有生育的意愿,就有可能使用这些冷冻的卵子尝试受孕。
- 延迟生育的女性 随着社会的发展,越来越多的女性选择在事业有成之后再考虑生育问题。然而,女性的生育能力会随着年龄的增长而逐渐下降,尤其是在 35 岁之后,这种下降趋势更为明显。冻卵技术为这些希望延迟生育的女性提供了一种保障。她们可以在年轻、生育能力较强的时候将卵子冷冻保存,等到合适的时机再尝试受孕。
三、冻卵技术的临床效果与影响因素
- 卵子的存活率和受精率 冻卵技术的临床效果受到多种因素的影响。从卵子的存活率和受精率来看,不同的研究报道结果有所差异。一般来说,玻璃化冷冻法在卵子存活率和受精率方面可能表现出一定的优势。一些研究显示,玻璃化冷冻法的卵子存活率可达 90% 以上,受精率也在 70% - 90% 左右;而慢冻法的卵子存活率在 50% - 70% 左右,受精率在 60% - 70% 左右。然而,这些数据并不是绝对的,实际的存活率和受精率还会受到卵子本身的质量、冷冻保护剂的使用、冷冻和解冻的操作过程等多种因素的影响。
- 怀孕率和活产率 冻卵后的怀孕率和活产率也是衡量技术效果的重要指标。随着技术的不断发展,冻卵后的怀孕率和活产率也在逐步提高。例如,慢冻法的活产率从早期的较低水平逐渐上升,从 1996 - 2004 年的每移植 21.6% 提高到 20,02 - 2004 年的 32.4%;玻璃化冷冻法的活产率和持续怀孕率从 2004 年之前的 29.4% 提高到 2004 年之后的 39%。但需要注意的是,怀孕率和活产率还与女性的年龄、身体状况、受孕环境等多种因素密切相关。
冻卵技术作为一种新兴的生育力保存手段,为女性的生育选择提供了更多的可能性。然而,我们也应该清醒地认识到,这项技术仍然处于不断发展和完善的过程中,面临着诸多技术挑战和伦理法律问题。只有通过不断的研究和探索,才能使冻卵技术更好地服务于女性的生育健康,为更多女性实现生育梦想提供有力的支持。
参考文献:Cacciottola L, Donnez J, Dolmans MM. Ovarian tissue and oocyte cryopreservation prior to iatrogenic premature ovarian insufficiency. Best Pract Res Clin Obstet Gynaecol. 2022 May;81:119-133. doi: 10.1016/j.bpobgyn.2021.09.010. Epub 2021 Nov 15. PMID: 34887172.
在当今社会,女性面临着多种可能影响生育能力的因素,如癌症治疗、延迟生育等。因此,生育力保存成为了一个重要的研究领域,而冻卵技术作为其中的一种方法,正逐渐受到关注。其目的在于为面临生育风险的女性提供一种保存生育能力的选择,以便在未来需要时能够实现生育梦想。
冻卵技术的原理
为了长期保存细胞的活性,需要将细胞置于极低的温度下,使其进入一种类似于 “暂停生命活动” 的状态。对于哺乳动物细胞来说,通常使用的储存温度是 -196°C(液氮的温度)。在这个温度下,水呈固态,生物反应停止,对冻存细胞的主要威胁被认为是背景辐射对 DNA 造成的损伤。
然而,冻卵过程中最关键的是要避免在温度变化过程中对卵子造成损伤。当水冷却到冰点以下时会形成冰晶,冰晶的体积比液态水大,会对细胞内的细胞器造成压力和剪切力,导致细胞受损。因此,避免冰晶形成是成功冻卵的首要目标。此外,随着水的冻结,溶质被排除在固体之外,会使剩余未冻结溶液的溶质浓度升高,对细胞内蛋白质产生毒性,避免这种溶液效应是第二个目标。在解冻过程中,如果升温缓慢,会有自由水解冻和再结晶的危险,而快速升温则可能导致细胞外渗透压突然下降,引起自由水快速流入细胞,造成细胞肿胀和损伤,即渗透压冲击,避免这种情况是第三个目标。
为了实现这些目标,所有成功的冻卵方法都使用了一种叫做冷冻保护剂的化学物质。冷冻保护剂分为渗透性和非渗透性两类。渗透性冷冻保护剂是小分子物质,能够穿透细胞膜,与水分子形成氢键,防止冰晶形成,并在一定浓度下可使水形成玻璃化状态(一种固态但不膨胀的状态)。常用的渗透性冷冻保护剂有丙二醇(PROH)等。非渗透性冷冻保护剂则留在细胞外,通过从细胞内吸取自由水来使细胞内空间脱水,从而增加渗透性冷冻保护剂在细胞内的浓度,进一步协助防止冰晶形成。在解冻过程中,非渗透性冷冻保护剂还可以防止因细胞内冷冻保护剂不能快速扩散出去而导致的渗透压冲击,常用的非渗透性冷冻保护剂有蔗糖等。
冻卵的方法
- 慢冻法(Slow - Freeze)
- 慢冻法在卵子仍处于代谢状态时使用较低的初始冷冻保护剂浓度,以降低毒性。冷冻保护剂通常在室温下添加,然后温度逐渐降低(约 2°C/min)到 -6°C 的播种温度。在这个温度下,通过用冰冷的器械触碰冻存容器的外部,引入一个小冰晶作为种子,诱导溶液中的冰晶形成。然后溶液在这个温度下保持一段时间(如 10 - 30 分钟)以达到平衡,之后温度再逐渐降低到 -32°C。在这个过程中,冰晶在细胞外介质中逐渐生长,冷冻保护剂浓度逐渐增加,特别是在细胞内空间,通过非渗透性冷冻保护剂进一步脱水。最后将冷冻容器投入液氮中。
- 在解冻时,为了防止冰晶再结晶,需要快速升温,但要注意避免渗透性冷冻保护剂在细胞内高浓度引起的渗透压冲击,因此需要使用额外的非渗透性冷冻保护剂。随着渗透性冷冻保护剂逐渐从卵子中扩散出来,非渗透性冷冻保护剂的浓度逐渐降低,直到卵子被放回标准培养基中。
- 快速冷冻法(Vitrification)
- 快速冷冻法(玻璃化冷冻)在室温下向细胞中添加高浓度的渗透性冷冻保护剂,由于这种高浓度的冷冻保护剂毒性较大,卵子不能在这个温度下长时间停留。经过短暂的平衡后,卵子直接投入液氮中。为了进一步防止冰晶形成,使用极快的冷却速度。在解冻时,也需要极快的升温速度以防止冰晶再结晶。
冻卵技术的临床应用
- 癌症患者的生育力保存
- 对于新诊断出癌症且面临绝育治疗的女性来说,冻卵是一种保存生育能力的方法。化疗和放疗等癌症治疗方法可能会导致卵巢功能衰竭,而冻卵可以在治疗前进行。例如,卵巢皮质含有大量原始卵泡,可以通过腹腔镜采集卵巢皮质,然后进行冻存。或者也可以采集处于生发泡阶段的卵子进行冻存,尽管生发泡卵子的体外成熟技术还不太可靠。
- 在癌症患者中使用冻卵技术也存在一些问题,如刺激卵泡和采集卵子所需的时间可能会延迟癌症治疗,而且对于患有全身性或播散性恶性肿瘤的患者,移植冻存的卵巢组织需要谨慎,因为可能存在残留的恶性细胞。
- 延迟生育
- 随着社会的发展,越来越多的女性选择延迟生育。由于年龄的增长会导致生育能力下降,冻卵为这些女性提供了一种在年轻时保存卵子的方法,以便在未来想要生育时使用。然而,目前对于冻卵技术在延迟生育方面的应用,还缺乏长期的数据,例如需要冻存多少卵子才能实现满意的怀孕率还不确定。
- 伦理问题及其他应用
- 冻卵技术为那些反对胚胎冷冻保存的夫妇提供了一种选择,也可以用于一些胚胎冷冻保存不合法的国家。此外,冻卵还可以用于卵子捐赠,通过冻存捐赠者的卵子,可以解决传统卵子捐赠中存在的一些问题,如捐赠者的可用性、成本、同步捐赠者和接受者的日程安排等。
冻卵技术的临床结果
- 存活率和受精率
- 不同的研究报道了不同的卵子存活率和受精率。例如,一些研究使用慢冻法报道的卵子存活率在 50% - 70% 左右,受精率 60% - 70% 左右;而使用玻璃化冷冻法报道的卵子存活率和受精率可能更高,如一些研究中卵子存活率可达 90% 以上,受精率也在 70% - 90% 左右。
- 怀孕率和活产率
- 从临床结果来看,冻卵后的怀孕率和活产率也在不断提高。慢冻法的活产率从 1996 - 2004 年的每移植 21.6% 提高到 2002 - 2004 年的 32.4%;玻璃化冷冻法的活产率和持续怀孕率从 2005 年之前的 29.4% 提高到 2005 年之后的 39%。同时,冻卵后的流产率也呈现出随着活产率提高而下降的趋势。
参考文献:Jain JK, Paulson RJ. Oocyte cryopreservation. Fertil Steril. 2006 Oct;86(4 Suppl):1037-46. doi: 10.1016/j.fertnstert.2006.07.1478. PMID: 17008147.
在人类辅助生殖领域,冷冻保存技术是一项非常重要的技术手段。它包括精子、胚胎和卵母细胞的冷冻保存。研究表明,精子和胚胎的冷冻保存已经成为常规操作,卵母细胞的冷冻保存也正逐渐在临床实践中得到更广泛的应用。
胚胎冷冻保存降低了新鲜胚胎移植的数量,提高了体外受精(IVF)周期的有效性。数据显示,同时进行新鲜胚胎和冷冻胚胎移植的女性,通过使用冷冻胚胎可获得额外 8% 的生育机会。卵母细胞冷冻保存相较于胚胎冷冻有更多优势,比如为因肿瘤治疗或慢性疾病面临生育力丧失风险的女性保存生育能力、用于卵子捐赠以及推迟生育等,还能避免胚胎冷冻所涉及的宗教和伦理道德问题。
冷冻保存技术的基本原理和方法
- 传统缓慢降温法
- 冷冻保护剂的作用
- 在胚胎和卵母细胞的冷冻保存过程中,防止冰晶形成和有毒溶质浓度过高是关键,这两者是导致细胞死亡的主要原因。为了实现这一点,细胞悬浮的冷冻溶液中需要添加冷冻保护剂(CPA)。CPA 分为细胞内 / 膜渗透性(如丙二醇、二甲基亚砜、甘油、乙二醇等)和细胞外 / 膜非渗透性化合物(如蔗糖、海藻糖、葡萄糖、蛋白质、脂蛋白等)。渗透性 CPA 通过渗透梯度置换水分,部分占据细胞内水的位置,而非渗透性 CPA 则增加细胞外渗透压,在冷冻前支持细胞脱水,解冻后防止水分快速进入细胞。
- 不同阶段的处理
- 对于人类胚胎和卵母细胞,在缓慢降温前,通常会让其暴露于渗透性和非渗透性 CPA 的混合物中 10 分钟进行脱水。对于早期卵裂阶段的胚胎和卵母细胞,常用低浓度的丙二醇(1.5M)和蔗糖(0.1 - 0.25 - 0.5M),而囊胚阶段的胚胎则常用甘油。以最初成功的小鼠和牛胚胎冷冻保存协议为例,是将胚胎以 - 0.3°C - 0.5°C/min 的缓慢降温速率冷却到 - 80°C - 120°C,但这个过程很长(几个小时)。后来有了改进的方法,如将绵羊和牛胚胎以 0.3°C/min 的速率缓慢冷却到 - 30 - 35°C 后,再浸入液氮中,大大缩短了冷冻过程(1.0 - 1.5 小时)。人类胚胎一般是以 0.3°C/min 的低冷却速率冷却到约 - 30°C - 40°C,然后以 - 50°C/min 的速率增加冷却到 - 80°C - 150°C 后再浸入液氮中。在缓慢降温过程中,手动在 5 到 - 8°C 之间诱导冰晶成核(播种),缓慢冷却到 - 30°C - 40°C 后再快速冷却到 - 196°C 的胚胎 / 卵母细胞,需要在 25°C - 37°C 的温水中快速解冻,然后逐步去除 CPA 进行细胞再水化。
- 冷冻保护剂的作用
- 玻璃化(超快速冷冻保存)法
- 技术原理
- 玻璃化是一种不同于缓慢降温的冷冻保存方法,它是在低温下通过极端提高粘度使溶液固化,避免冰晶在细胞内和细胞外空间形成。这是通过高浓度的 CPA(4 - 8mol/L)和极高(超快速)的冷却速率实现的。在玻璃化过程中,细胞主要在超快速冷却开始前通过暴露于高浓度的 CPA 进行脱水,以获得玻璃化的细胞内和细胞外状态。但玻璃化过程中 CPA 的高浓度可能对细胞有毒性,不过可以通过混合不同的 CPA 来降低每种 CPA 的相对浓度,并将胚胎 / 卵母细胞暴露于溶液的时间减到最少来控制毒性。
- 操作要点
- 用于玻璃化的冷冻溶液由渗透性(如 EG、G、DMSO、PG、乙酰胺等)和非渗透性(如蔗糖、海藻糖等)试剂组成,有些协议还会补充大分子物质如聚乙二醇等。为了提高冷却速率,胚胎 / 卵母细胞玻璃化的溶液体积已被大幅减小(0.1 - 2μL),并开发了特殊的载体系统,如开放式拉伸吸管、Flexipet - 剥脱移液器、Cryotop 等。玻璃化技术操作难度较大,因为胚胎 / 卵母细胞必须在极短时间(<1min)内处理非常浓缩、粘稠且体积小的玻璃化溶液,所以操作人员需要经过良好的培训。
- 技术原理
人类胚胎和卵母细胞冷冻保存的实践经验及安全性
- 胚胎冷冻保存的实践经验
- 不同阶段的效果
- 对于人类胚胎冷冻保存,早期卵裂阶段胚胎解冻后至少保留一半初始卵裂球被认为是存活的。在一项大型多中心研究中,14000 个早期卵裂阶段缓慢冷冻和解冻的胚胎中,73% 的胚胎至少有一半初始卵裂球仍然完整,移植后的临床妊娠率和着床率分别为 16% 和 8.4%。对于囊胚冷冻保存,常用甘油和蔗糖的组合作为冷冻溶液,报道的内细胞团和滋养层细胞至少 50% 存活的存活率在 69% - 98% 之间,着床率在 16% - 30% 左右。早期卵裂阶段人类胚胎已成功在多种基于 DMSO、EG 等的溶液中玻璃化,存活率约 60% - 80%,且有多个妊娠 / 分娩案例。囊胚玻璃化常用 EG 和 DMSO 的混合物作为溶液,报道的总体存活率在 70% - 99% 之间,着床率在 20% - 50% 左右。
- 不同方法的比较
- 在一些比较研究中,发现玻璃化和缓慢降温在胚胎存活和着床率方面各有优劣。例如,在某些情况下玻璃化的卵裂阶段和囊胚阶段胚胎解冻后存活率较高,但在有经验的群体中,玻璃化并不比缓慢降温有更高的怀孕概率。
- 不同阶段的效果
- 卵母细胞冷冻保存的实践经验
- 不同方法的影响
- 在缓慢冷冻卵母细胞方面,提高蔗糖浓度(从 0.1M 到 0.3M)可以提高脱水率以及 MII 卵母细胞的存活率和受精率。改变 CPA 的平衡温度、冰晶成核和将胚胎浸入液氮的操作,以及用胆碱替代钠或直接向卵母细胞细胞质中注射蔗糖等方法都能提高卵母细胞的存活率。但缓慢冷却的卵母细胞相对于新鲜对照组发育较慢。在玻璃化卵母细胞方面,常用的玻璃化溶液由渗透性(2.7M EG 和 2.1M DMSO)和非渗透性 CPA(0.5M 蔗糖)组成,改进的玻璃化技术提高了玻璃化人类卵母细胞解冻后的存活率和受精率,与新鲜对照卵母细胞相当。
- 不同方法的影响
参考文献:Konc J, Kanyó K, Kriston R, Somoskői B, Cseh S. Cryopreservation of embryos and oocytes in human assisted reproduction. Biomed Res Int. 2014;2014:307268. doi: 10.1155/2014/307268. Epub 2014 Mar 23. PMID: 24779007; PMCID: PMC3980916.
展开更多














