当前位置:首页>
乙肝可以治愈吗?
随着核苷酸类抗病毒药物不断研发使用,丙型肝炎已经归为多数可以治愈的疾病。那么慢性乙型肝炎可以治愈吗?最新研究结果提示,新型抗病毒药物使用,结合长效干扰素序贯治疗,可以临床治愈部分乙型肝炎,相信不久将来,乙肝不再是影响人类健康的顽疾。
本站内容仅供医学知识科普使用,任何关于疾病、用药建议都不能替代执业医师当面诊断,请谨慎参阅
-
大多数慢性乙型肝炎(CHB)患者需要长期甚至终生抗病毒治疗,随着抗病毒治疗方案的不断升级,CHB患者生存期明显延长,患者开始呈现老龄化趋势,合并高血压、糖尿病等基础疾病的比例增加[1],且抗病毒药物也存在一定的肾脏毒性等副作用,以上因素及HBV感染本身的影响,都可能增加CHB患者治疗过程中的骨肾安全性风险[2-3]。
近期我国学者对全国47家医院门诊、2703位经治CHB患者(使用核苷类似物治疗>6个月)开展了一项横断面研究,以评估经治CHB患者的肾脏功能损害相关因素及肾小管损伤高危因素。
研究数据显示,所有患者中57.1%有至少一个肾功能指标异常,14.6%患者合并慢性肾脏病(CKD),提示CHB经治患者的慢性肾损害比例高,尿视黄醇结合蛋白(RBP)、尿β2-微球蛋白、α1-微球蛋白三种肾小管损伤标志物的异常率分别为10.4%、27.1%和18.4%,且患者使用恩替卡韦(ETV)、富马酸替诺福韦酯(TDF)等药物抗病毒治疗时长,与肾小管损伤标志物异常有关[4]。
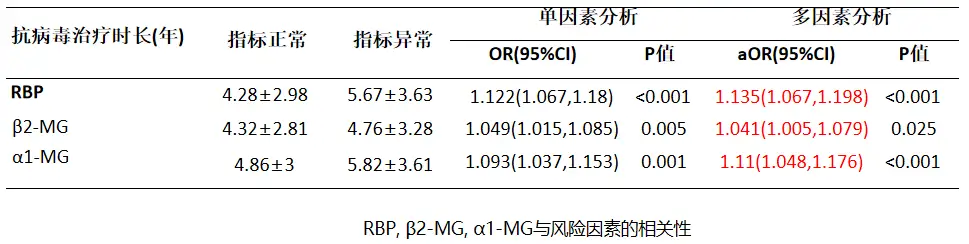
图1 肾小管损伤标志物与抗病毒治疗时长的相关性
一项韩国临床研究数据显示,在102例阿德福韦酯(ADV)耐药、90例ETV耐药患者(无ADV耐药)中,使用TDF进行治疗的,在TDF治疗的五年期间,患者的肾小球滤过率(eGFR)出现进行性下降,股骨密度较基线时也显著下降(-2.48%, p<0.001)[5],提示TDF治疗对患者肾脏功能和骨密度的影响不容忽视。
国内外多个权威CHB指南均将存在或伴有肾功能损伤/骨病高危风险的患者列为“特殊人群”,对抗病毒治疗专门提出推荐意见,例如欧洲肝脏研究协会(EASL)2017版指南就建议,存在骨肾安全性风险的NA初治CHB患者优选丙酚替诺福韦(TAF)或ETV,TDF经治患者应换用TAF或ETV,且先前暴露于NA的患者应优选TAF[4]。
EASL指南的推荐与此后2018版美国肝病研究学会(AASLD)指南推荐相似[5],我国2019年版《慢性乙型肝炎防治指南》对慢性肾脏病患者、肾功能不全或接受肾脏替代治疗的患者推荐ETV或TAF作为一线抗HBV治疗药物,且TAF治疗肾功能不全的患者时,并不需要调整剂量(肌酐清除率<15ml/min且未透析的患者,目前尚无推荐剂量)[6]。
虽然TAF与TDF的前体药物均为替诺福韦,但二者的结构不同,TAF的预磷酸化和磷酰胺酯前药结构,使其能够直达肝脏快速发挥抗病毒作用,同时TAF在血浆中更加稳定,降低了非靶器官的替诺福韦暴露,从而在保障疗效的同时改善了骨肾安全性。
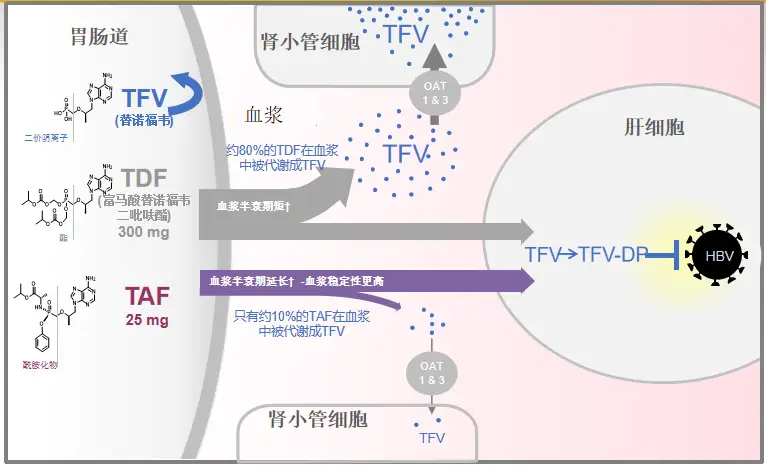
图2 TAF精准靶向肝脏,降低骨肾风险
2020年AASLD年会公布了TAF两项核心临床III期研究108 & 110研究的5年随访数据,TAF治疗5年后患者eGFR仅有轻微下降(见图3),且TDF经治患者换用TAF治疗后,eGFR及β2微球蛋白:尿肌酐值(β2M:Cr)等近端肾小管标志物水平均较换用TAF前有所上升;TAF治疗组的髋/脊柱骨密度相对保持稳定,而TDF经治患者换用TAF后,髋/脊柱骨密度平均百分比增加(见图4),都支持了TAF治疗良好的骨肾安全性[7]。
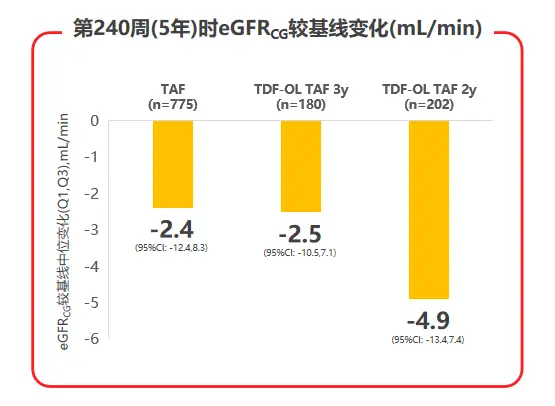
图3 108 & 110研究治疗240周时eGFR变化情况
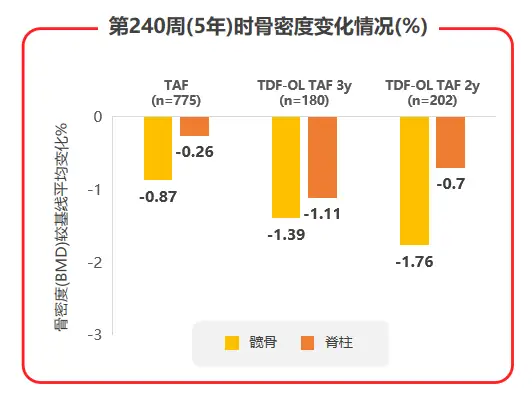
图4 108 & 110研究中治疗240周时骨密度变化情况
2020年EASL年会则公布了TAF临床II期4035研究数据,在治疗伴有肾功能损伤,且TDF或其它NAs经治已获得病毒学应答CHB患者的研究队列A中,患者换用TAF后仍能维持病毒学抑制和ALT正常的状态,且肌酐清除率、血肌酐、血磷水平,RBP:Cr、β2M:Cr等近端肾小管功能标志物水平均维持稳定,髋/脊柱骨密度小幅上升,提示TAF治疗的骨肾安全性良好[8]。
以上临床证据均显示,CHB患者的骨肾安全性风险应得到高度重视,而存在风险或已有肾功能损伤/骨病的患者,无论是初治还是经治,均应按照指南推荐将TAF作为治疗优选方案,从而实现疗效和安全性两方面的获益。
参考文献:
1. Wong G L, Wong V W, Yuen B W, et al. An Aging Population of Chronic Hepatitis B With Increasing Comorbidities: A Territory-Wide Study From 2000 to 2017.[J]. Hepatology, 2020, 71(2): 444-455.
2. Shin J, Kwon H J, Jang H R, et al. Risk factors for renal functional decline in chronic hepatitis B patients receiving oral antiviral agents[J]. Medicine, 2016, 95(1).
3. Biver E, Calmy A, Rizzoli R. Bone health in HIV and hepatitis B or C infections[J]. Therapeutic Advances in Musculoskeletal Disease, 2017, 9(1): 22-34.
4.刘静, 肖光明, 吕芳芳, 等. 一项中国慢性乙型肝炎门诊经治患者肾脏功能损害的横断面研究
5. Lim Y S, Gwak G Y, Choi J, et al. Monotherapy with tenofovir disoproxil fumarate for adefovir-resistant vs. entecavir-resistant chronic hepatitis B: a 5-year clinical trial[J]. Journal of Hepatology, 2019, 71(1): 35-44.
6. European Association For The Study Of The Liver. EASL 2017 Clinical Practice Guidelines on the management of hepatitis B virus infection[J]. Journal of Hepatology, 2017, 67(2): 370-398.
7. Terrault N A, Lok A S F, McMahon B J, et al. Update on prevention, diagnosis, and treatment of chronic hepatitis B: AASLD 2018 hepatitis B guidance[J]. Hepatology, 2018, 67(4): 1560-1599.
8. 中华医学会感染病学分会,中华医学会肝病学分会.慢性乙型肝炎防治指南(2019年版)[J].实用肝脏病杂志,2020,23(1):后插9-后插32.
9. Chan HL, et al. Poster 803 Maintenance of High Levels of Viral Suppression and Improved Safety Profile of Tenofovir Alafenamide (TAF) Relative to Tenofovir Disoproxil Fumarate (TDF) in Chronic Hepatitis B Patients Treated for 5 Years in 2 Ongoing Phase 3 Studies[J]. Hepatology, 2020, 72(S1): 131A-1159A.
10. Lim Y-S, Lin C-Y, Heo J, et al. SAT442 - Safety and efficacy of switching to tenofovir alafenamide (TAF) in virally suppressed chronic hepatitis B (CHB) patients with hepatic impairment: week 48 results from a phase 2 open label study[J]. Journal of Hepatology, 2020, 73(S1): S872. -
大多数慢性乙型肝炎(CHB)患者需要长期甚至终生抗病毒治疗,随着抗病毒治疗方案的不断升级,CHB患者生存期明显延长,患者开始呈现老龄化趋势,合并高血压、糖尿病等基础疾病的比例增加[1],且抗病毒药物也存在一定的肾脏毒性等副作用,以上因素及HBV感染本身的影响,都可能增加CHB患者治疗过程中的骨肾安全性风险[2-3]。
近期我国学者对全国47家医院门诊、2703位经治CHB患者(使用核苷类似物治疗>6个月)开展了一项横断面研究,以评估经治CHB患者的肾脏功能损害相关因素及肾小管损伤高危因素。
研究数据显示,所有患者中57.1%有至少一个肾功能指标异常,14.6%患者合并慢性肾脏病(CKD),提示CHB经治患者的慢性肾损害比例高,尿视黄醇结合蛋白(RBP)、尿β2-微球蛋白、α1-微球蛋白三种肾小管损伤标志物的异常率分别为10.4%、27.1%和18.4%,且患者使用恩替卡韦(ETV)、富马酸替诺福韦酯(TDF)等药物抗病毒治疗时长,与肾小管损伤标志物异常有关[4]。
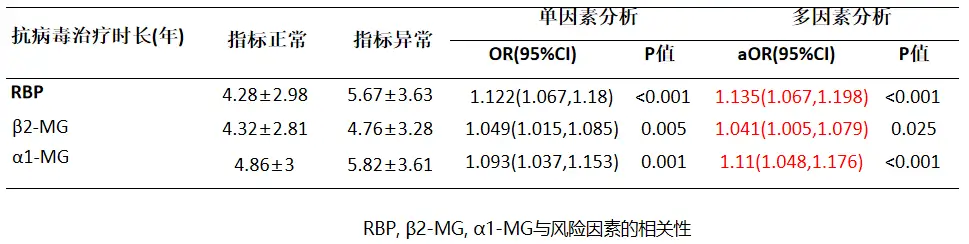
图1 肾小管损伤标志物与抗病毒治疗时长的相关性
一项韩国临床研究数据显示,在102例阿德福韦酯(ADV)耐药、90例ETV耐药患者(无ADV耐药)中,使用TDF进行治疗的,在TDF治疗的五年期间,患者的肾小球滤过率(eGFR)出现进行性下降,股骨密度较基线时也显著下降(-2.48%, p<0.001)[5],提示TDF治疗对患者肾脏功能和骨密度的影响不容忽视。
国内外多个权威CHB指南均将存在或伴有肾功能损伤/骨病高危风险的患者列为“特殊人群”,对抗病毒治疗专门提出推荐意见,例如欧洲肝脏研究协会(EASL)2017版指南就建议,存在骨肾安全性风险的NA初治CHB患者优选丙酚替诺福韦(TAF)或ETV,TDF经治患者应换用TAF或ETV,且先前暴露于NA的患者应优选TAF[4]。
EASL指南的推荐与此后2018版美国肝病研究学会(AASLD)指南推荐相似[5],我国2019年版《慢性乙型肝炎防治指南》对慢性肾脏病患者、肾功能不全或接受肾脏替代治疗的患者推荐ETV或TAF作为一线抗HBV治疗药物,且TAF治疗肾功能不全的患者时,并不需要调整剂量(肌酐清除率<15ml/min且未透析的患者,目前尚无推荐剂量)[6]。
虽然TAF与TDF的前体药物均为替诺福韦,但二者的结构不同,TAF的预磷酸化和磷酰胺酯前药结构,使其能够直达肝脏快速发挥抗病毒作用,同时TAF在血浆中更加稳定,降低了非靶器官的替诺福韦暴露,从而在保障疗效的同时改善了骨肾安全性。
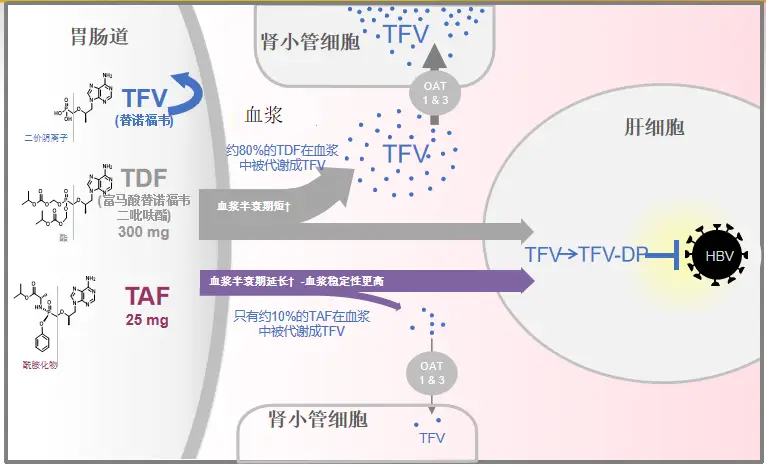
图2 TAF精准靶向肝脏,降低骨肾风险
2020年AASLD年会公布了TAF两项核心临床III期研究108 & 110研究的5年随访数据,TAF治疗5年后患者eGFR仅有轻微下降(见图3),且TDF经治患者换用TAF治疗后,eGFR及β2微球蛋白:尿肌酐值(β2M:Cr)等近端肾小管标志物水平均较换用TAF前有所上升;TAF治疗组的髋/脊柱骨密度相对保持稳定,而TDF经治患者换用TAF后,髋/脊柱骨密度平均百分比增加(见图4),都支持了TAF治疗良好的骨肾安全性[7]。
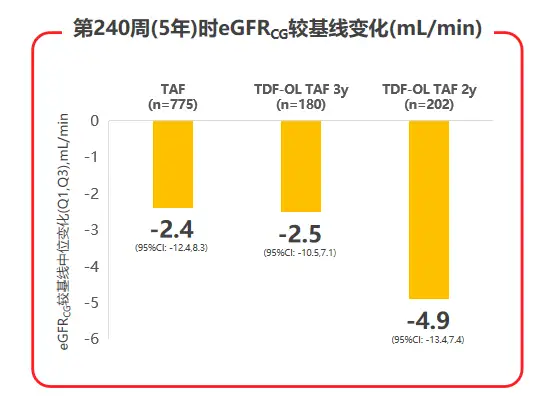
图3 108 & 110研究治疗240周时eGFR变化情况
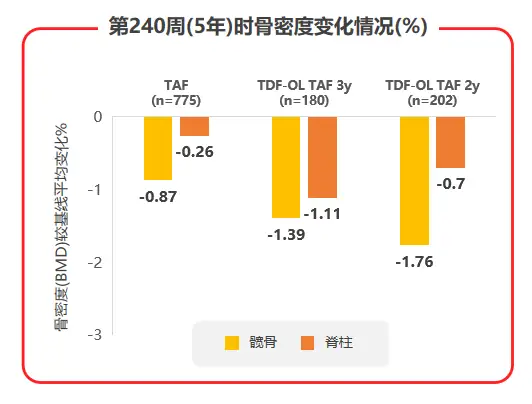
图4 108 & 110研究中治疗240周时骨密度变化情况
2020年EASL年会则公布了TAF临床II期4035研究数据,在治疗伴有肾功能损伤,且TDF或其它NAs经治已获得病毒学应答CHB患者的研究队列A中,患者换用TAF后仍能维持病毒学抑制和ALT正常的状态,且肌酐清除率、血肌酐、血磷水平,RBP:Cr、β2M:Cr等近端肾小管功能标志物水平均维持稳定,髋/脊柱骨密度小幅上升,提示TAF治疗的骨肾安全性良好[8]。
以上临床证据均显示,CHB患者的骨肾安全性风险应得到高度重视,而存在风险或已有肾功能损伤/骨病的患者,无论是初治还是经治,均应按照指南推荐将TAF作为治疗优选方案,从而实现疗效和安全性两方面的获益。
参考文献:
1. Wong G L, Wong V W, Yuen B W, et al. An Aging Population of Chronic Hepatitis B With Increasing Comorbidities: A Territory-Wide Study From 2000 to 2017.[J]. Hepatology, 2020, 71(2): 444-455.
2. Shin J, Kwon H J, Jang H R, et al. Risk factors for renal functional decline in chronic hepatitis B patients receiving oral antiviral agents[J]. Medicine, 2016, 95(1).
3. Biver E, Calmy A, Rizzoli R. Bone health in HIV and hepatitis B or C infections[J]. Therapeutic Advances in Musculoskeletal Disease, 2017, 9(1): 22-34.
4.刘静, 肖光明, 吕芳芳, 等. 一项中国慢性乙型肝炎门诊经治患者肾脏功能损害的横断面研究
5. Lim Y S, Gwak G Y, Choi J, et al. Monotherapy with tenofovir disoproxil fumarate for adefovir-resistant vs. entecavir-resistant chronic hepatitis B: a 5-year clinical trial[J]. Journal of Hepatology, 2019, 71(1): 35-44.
6. European Association For The Study Of The Liver. EASL 2017 Clinical Practice Guidelines on the management of hepatitis B virus infection[J]. Journal of Hepatology, 2017, 67(2): 370-398.
7. Terrault N A, Lok A S F, McMahon B J, et al. Update on prevention, diagnosis, and treatment of chronic hepatitis B: AASLD 2018 hepatitis B guidance[J]. Hepatology, 2018, 67(4): 1560-1599.
8. 中华医学会感染病学分会,中华医学会肝病学分会.慢性乙型肝炎防治指南(2019年版)[J].实用肝脏病杂志,2020,23(1):后插9-后插32.
9. Chan HL, et al. Poster 803 Maintenance of High Levels of Viral Suppression and Improved Safety Profile of Tenofovir Alafenamide (TAF) Relative to Tenofovir Disoproxil Fumarate (TDF) in Chronic Hepatitis B Patients Treated for 5 Years in 2 Ongoing Phase 3 Studies[J]. Hepatology, 2020, 72(S1): 131A-1159A.
10. Lim Y-S, Lin C-Y, Heo J, et al. SAT442 - Safety and efficacy of switching to tenofovir alafenamide (TAF) in virally suppressed chronic hepatitis B (CHB) patients with hepatic impairment: week 48 results from a phase 2 open label study[J]. Journal of Hepatology, 2020, 73(S1): S872.
-
为实现慢性乙型肝炎(CHB)治疗中,“HBV DNA降得越低越好”的治疗目标,近年来国内外权威指南纷纷调整一线治疗推荐,推荐丙酚替诺福韦(TAF)等多种强效低耐药药物[1-2]。凭借良好的抗病毒效果和骨肾安全性,TAF获得我国越来越多临床医师的青睐。
在2020年美国肝病研究学会(AASLD)年会上,TAF治疗CHB的两项核心临床III期研究——108 & 110研究5年随访数据公布[3],TAF维持了此前持续强效抗病毒、骨肾安全性良好的整体表现,为其在我国CHB治疗中的进一步广泛应用提供了力证。
108 & 110两项临床III期研究,均为国际多中心、双盲、随机对照临床试验,本次分析共纳入1248名CHB患者(纳入标准为:HBV DNA≥20000 IU/mL,男性ALT>60 U/L,女性ALT>38 U/L,eGFRCG≥50 mL/min,近期影像学检查无肝细胞癌(HCC)证据),入组患者按2:1比例分入TAF组(n=866)或TDF组(n=382),其中TDF组患者180例在第96周、202例在第144周后开放标签,换用TAF进行治疗(见图1)。
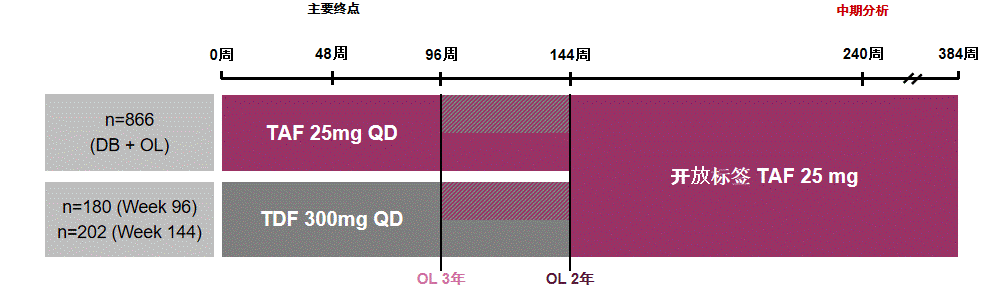
图1 108 & 110研究整体设计
不同治疗组患者整体基线特征如图2所示,可看出研究入组患者有着同时覆盖初治及经治患者(核苷(酸)类似物经治患者约占25%)、亚裔比例较高(TAF组中比例79%)、病毒载量均值高(平均值为7 log10IU/mL)和ALT水平高(96%患者ALT超过正常参考值上限/ULN一倍以上)的特点。
2019年我国《慢性乙型肝炎防治指南》扩大CHB患者启动治疗的适应证,将HBV DNA阳性、ALT持续异常(ALT>ULN)且排除其它原因导致ALT升高的慢性HBV携带者纳入抗病毒治疗范围,108 & 110研究人群整体特征与这一适应证对应患者群体相似。
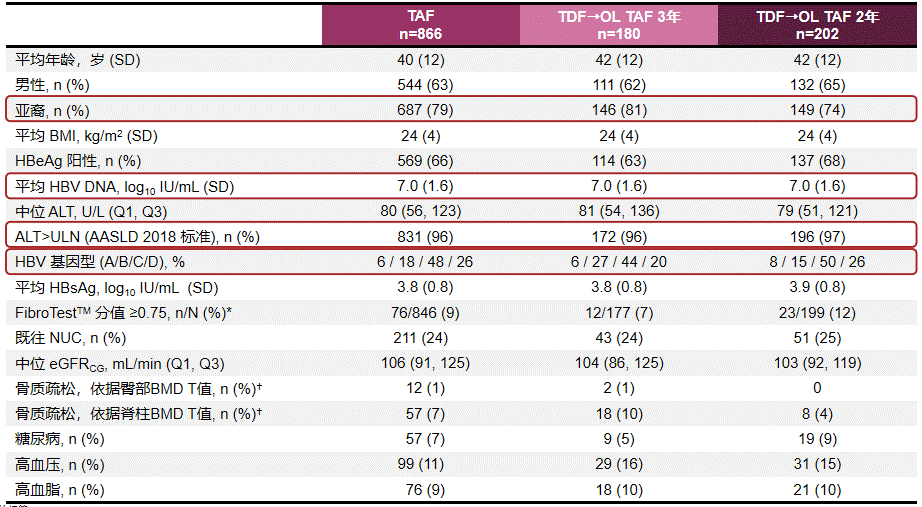
图2 108 & 110研究患者基线特征
两项研究5年分析时的有效性终点为治疗240周的病毒学抑制率(定义病毒抑制为HBV DNA<29 IU/mL),其它有效性终点则包括研究过程中持续评估的ALT复常率、血清学应答、肝纤维化变化、基因型耐药等指标。研究的安全性终点包括不良事件(AEs),LDL-C、淀粉酶升高等实验室检查结果异常,以及各项骨肾安全性标志物的变化。
在有效性终点方面,TAF治疗组的5年病毒学抑制率为93%,TDF换用TAF治疗2年或3年的患者病毒学抑制率分别为96%和92%,TAF治疗均实现并维持相似的高病毒学抑制率。
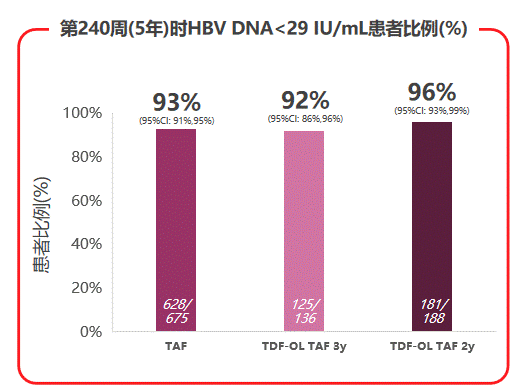
图3 108 & 110研究病毒学抑制状况
按照2018年AASLD最新ALT正常标准(男性患者≤35 U/L,女性患者≤25 U/L)评价,TAF治疗组、换用TAF两年/三年的三组患者,ALT复常率分别为76%、76%和74%,提示ALT治疗可维持CHB患者较高的ALT复常率。
AASLD年会同期公布了108 & 110研究一项亚组分析,该分析共纳入1632名CHB患者,评估患者基线HBV DNA载量对治疗过程中ALT复常的影响,分析结果显示TAF组患者的ALT复常率不受基线HBV DNA载量影响,且对基线低、中、高病毒载量患者,TAF治疗的ALT复常率均高于TDF(见图4)[4]。
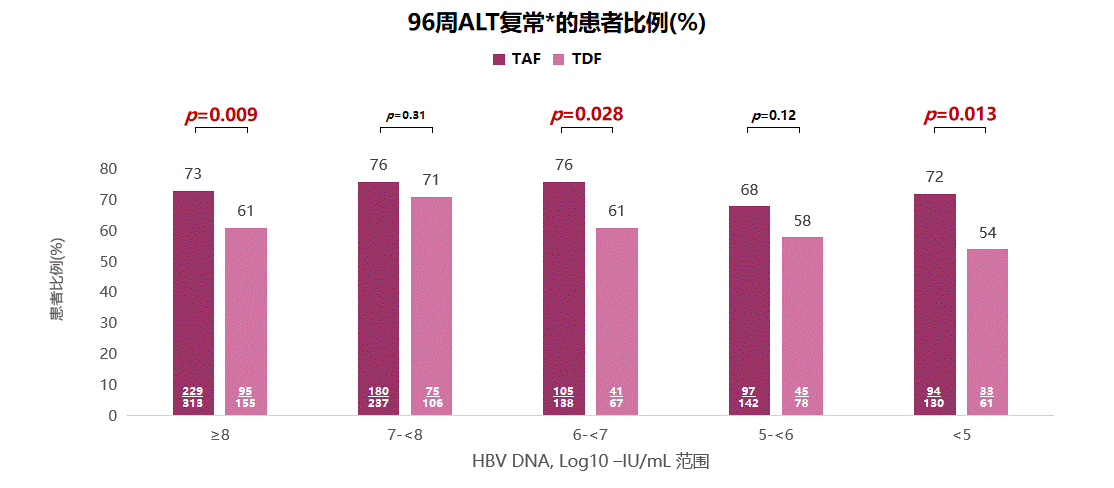
图4 108 & 110研究中基线病毒载量不同患者的ALT复常比例
血清学应答方面,TAF或TDF治疗患者5年内的HBsAg消失率均较低(共5例),但HBeAg消失/血清学转换率逐年增加(见图5),FibroTest检查结果显示,大多数患者的肝纤维化维持稳定或有所改善,肝纤维化加重比例约为10%。5年分析报告的随访240周期间,未观察到基因型耐药(表型耐药结果待定),TAF治疗相关耐药的发生率仍然为0.
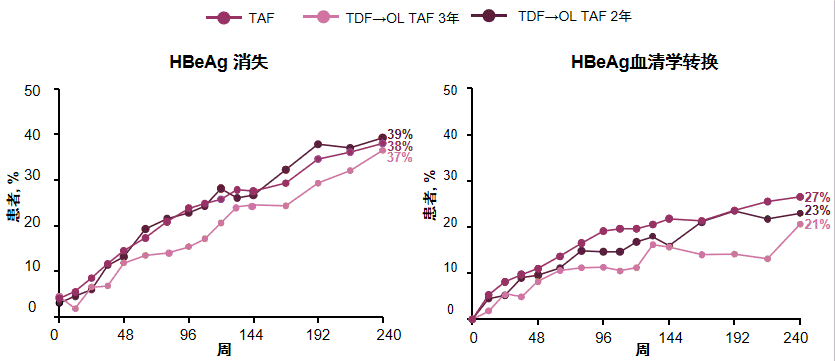
图5 108 & 110研究的HBeag消失/血清学转换情况
在治疗安全性方面,三个治疗组的不良事件和实验室检查结果异常发生率接近,3-4级不良事件或严重不良事件发生率低,因不良事件停药患者不足1%。肾脏安全性指标显示,TAF治疗5年后患者估算肾小球滤过率(eGFRCG)仅有轻微下降,且TDF经治患者换用TAF治疗后,eGFRCG(见图6)及β2微球蛋白:尿肌酐值(β2M:Cr)等近端肾小管标志物水平,均较换用TAF前有所上升,提示TAF治疗较好的肾脏安全性。
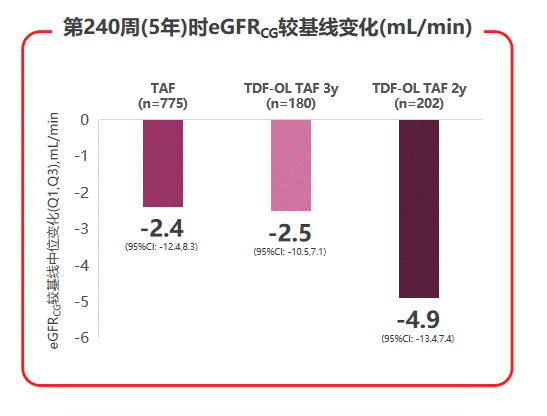
图6 108 & 110研究中患者eGFRCG变化状况
而在骨安全性方面,TAF治疗组的髋/脊柱骨密度相对保持稳定,TDF经治患者换用TAF后,髋/脊柱骨密度平均百分比增加(见图7),提示换用TAF可能改善TDF治疗导致的骨流失。综合不良事件、实验室检查结果异常发生率和骨肾安全性数据,TAF在强效抑制病毒、耐药仍然为0的基础上,安全性也令人满意。
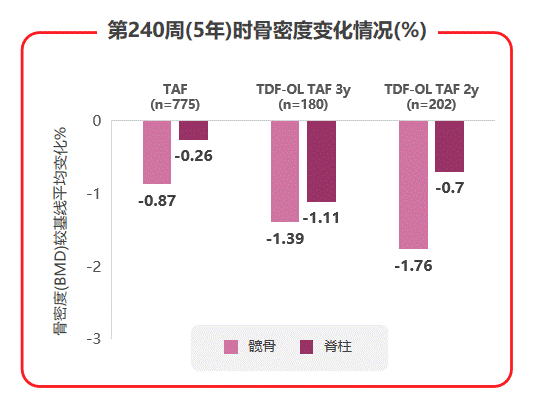
图7 108 & 110研究中患者髋/脊柱骨密度治疗5年间变化情况
总结
108 & 110研究的5年分析数据,实现了有效性和安全性的双优,为TAF长期使用提供了重要循证医学证据。而AASLD年会上公布的多项真实世界研究[5-6],也反映出TAF作为目前国内外指南力推荐治疗用药,已经开始全方位深入CHB治疗,用于情况不同的各种实战环境,相信未来还会有更多反映TAF优势的临床应用数据。
参考文献:
1. 中华医学会感染病学分会,中华医学会肝病学分会.慢性乙型肝炎防治指南(2019年版)[J].实用肝脏病杂志,2020,23(1):后插9-后插32.
2. Terrault N A, Lok A S F, McMahon B J, et al. Update on prevention, diagnosis, and treatment of chronic hepatitis B: AASLD 2018 hepatitis B guidance[J]. Hepatology, 2018, 67(4): 1560-1599.
3. Chan HL, et al. AASLD 2020. Abstract 803.
4. Lim Y-S, et al. AASLD 2020. Abstract 796.
5. Zhang YQ, et al. AASLD 2020. Abstract 779.
6. Zhang YQ, et al. AASLD 2020. Abstract 780. -



杨松,医学博士,副主任医师,北京大学副教授,北京肝病学会青委会副主任委员,主持我国16部肝病指南共识文件撰写。
点击跟医生交流→ https://m.healthjd.com/s/EvaluationManage/DoctorDetail?doctorId=194110237171
图片来源于网络,如有侵权请联系删除。
-
老刘今年46岁,是一家服装店的老板,半年前的一次体检中,他被检查出了乙肝,从那之后就开始重视起自己的身体健康了,不仅积极地配合医生进行治疗,还十分注重饮食。
老刘认为鸡蛋营养丰富,蛋白质含量也高,每天吃一个鸡蛋有助于病情的好转,就每天吃一个鸡蛋。但最近朋友告诉他,鸡蛋里的胆固醇含量很高,会影响肝脏的代谢,乙肝患者不能吃鸡蛋。他担心自己之前吃的鸡蛋会不会影响肝脏健康,因此,特意来到医院咨询医生。
乙肝患者,每天吃一个鸡蛋会怎样?
鸡蛋物美价廉,是国民喜爱的一种滋补食品。而且,鸡蛋有多种人体所需的氨基酸,不饱和脂肪酸和各种维生素。鸡蛋的蛋白质是众多食物中营养价值最高的,与人体蛋白质氨基酸的模式最为接近,能很好补充肝脏日常运转所需的营养。鸡蛋的胆固醇主要集中在蛋黄中,每颗蛋黄约含200mg的胆固醇,胆固醇会加速脂肪的囤积,给肝细胞带来工作负担,诱发肝炎、肝硬化。但每天一个鸡蛋,并不会诱发高血脂、脂肪肝,原因有以下两点。
1、人体自身也会合成胆固醇,有调节功能
相关研究表明,人体血清胆固醇水平与摄入的食物没有明显的联系,胆固醇是人体运转所必需的物质。当血液中的胆固醇含量较低时,人体就会合成并吸收胆固醇,使其保持在一定浓度。当胆固醇含量过多时,人体就会减少胆固醇的合成与吸收。但是,如果身体大量摄入胆固醇的话,会损害身体的调节功能。
2、鸡蛋中的磷酸酯可以降低胆固醇
鸡蛋中含有的不饱和脂肪酸,可以降低人体内血清胆固醇的含量。蛋黄中含有磷酸酯可以阻止血清胆固醇的沉淀,是一种强乳化剂,可以防止脂肪堆积,堵塞血管,进而减少肝脏受到的损伤。此外,鸡蛋中还含有大量的天然甾醇,对人体十分有益,可以降低患心脑血管疾病的风险。

医生:想要肝好,2个习惯趁早改
1、熬夜俗话说“人卧血归于肝”,夜间是肝脏进行解毒、排毒的黄金时间,此时如果不及时进行休息,就会影响肝脏的代谢,毒素长期累积在肝脏,就会引起肝部炎症,造成肝脏损伤,进而导致肝病不断恶化。因此,对于肝病患者来说,养成一个良好的作息习惯有助于身体健康。

2、酗酒
酒精对人体的损害是非常大的,人体在摄入酒精后,90%需要肝脏来分解,过度饮用,会加重肝脏的负担。酒精对肝细胞有损害作用,存积在肝脏会不断损伤肝细胞,增大肝脏病变的几率。此外,酒精在转化过程中会产生乙醛,这是一种致癌物,长期摄入会增大肝部癌变的风险。
-
丙酚替诺福韦(TAF)作为强效低耐药的核苷酸类似物药物,在慢性乙型肝炎(CHB)中的治疗价值已得到高度认可,但随着抗病毒治疗效果的改善,CHB治疗中也出现了一些需要应对的新问题,如对慢性非传染性疾病较多的老年患者、肝/肾功能损伤患者等群体,抗病毒方案的选择就需要细化。近年来多项临床研究已显示,TAF用于CHB多种不同患者人群有着良好的有效性和安全性[1-2],而各种真实世界研究进一步证实了TAF的治疗价值,本文将对多项相关研究进行解读。
低病毒血症患者改用TAF,可改善病毒学应答状况
对经治且存在低病毒血症(LLV,美国AASLD指南定义为HBVDNA20~2000IU/mL[3])的患者,换用TAF治疗有望提升完全病毒学应答(CVR)比例。如日本多中心、回顾性KULDS研究,共入组313例≥20岁,治疗至少2年的经治CHB患者,其中191例接受恩替卡韦(ETV)治疗,122例接受其他核苷(酸)类似物(NA)联合治疗治疗。
研究评估患者换用TAF治疗48周时的疗效及肾脏安全性,其中ETV经治患者基线有34例LLV患者,换用TAF治疗48周后33例达到CVR(HBVDNA≤20IU/mL),比例高达97.1%;基于TDF或ADV的NA联合治疗组基线有9例LLV患者,换用TAF治疗后也有7例达到CVR[4]。
我国学者开展的一项前瞻性、单中心真实世界研究[5],共入组211例ETV单药治疗≥48周后为LLV的CHB患者,按患者意愿继续ETV单药治疗(109例)或换用TAF(102例),评价治疗24周时的CVR(HBVDNA<20IU/mL)比例,次要终点包括HBVDNA下降程度及ALT复常率,安全性终点包括治疗不良事件、肾功能变化等,其中150例患者纳入倾向性评分匹配(PSM)队列,继续ETV治疗和换用TAF的患者各有75例,组间基线特征整体相近。
不论是在PSM队列还是在原始队列(RAW队列)中,治疗12、24周时换用TAF组患者的CVR比例(见图1)均显著高于ETV单药治疗组;治疗24周时在PSM队列中,换用TAF患者HBVDNA定量平均降幅为1.99log10IU/ml,显著高于ETV组的0.76log10IU/ml(p=0.002),RAW队列中降幅则分别为2.2log10IU/ml和0.74log10IU/ml,TAF组降幅仍显著更高(p<0.001)。
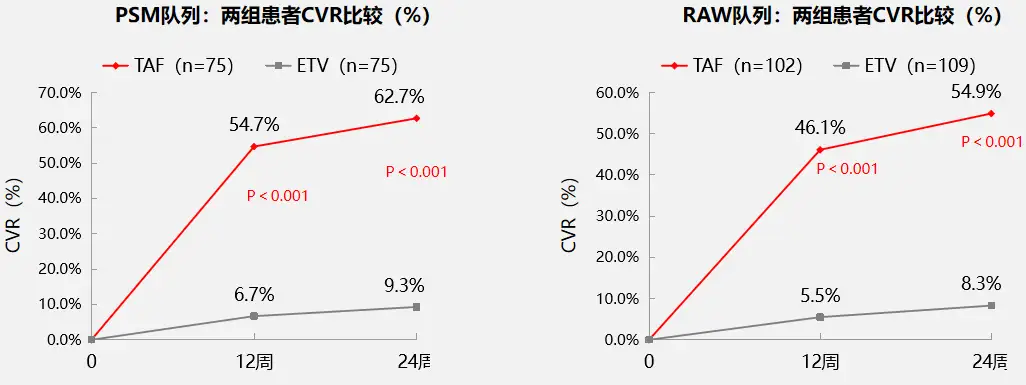
图1两组LLV患者CVR情况比较
按中心实验室标准或2018年AASLD标准评价的ALT复常率,至24周时不论是PSM队列还是RAW队列,TAF组均显著高于ETV组(见图2,12周时PSM队列TAF组的ALT复常率数值上更高,但差异尚未达到统计学显著性),但无论在PSM或RAW队列中,两组患者HBeAg转阴率/血清转换率、qHBsAg变化等HBV生物标志物变化,肝硬度测量等无创性肝纤维化测量结果均无显著差异。
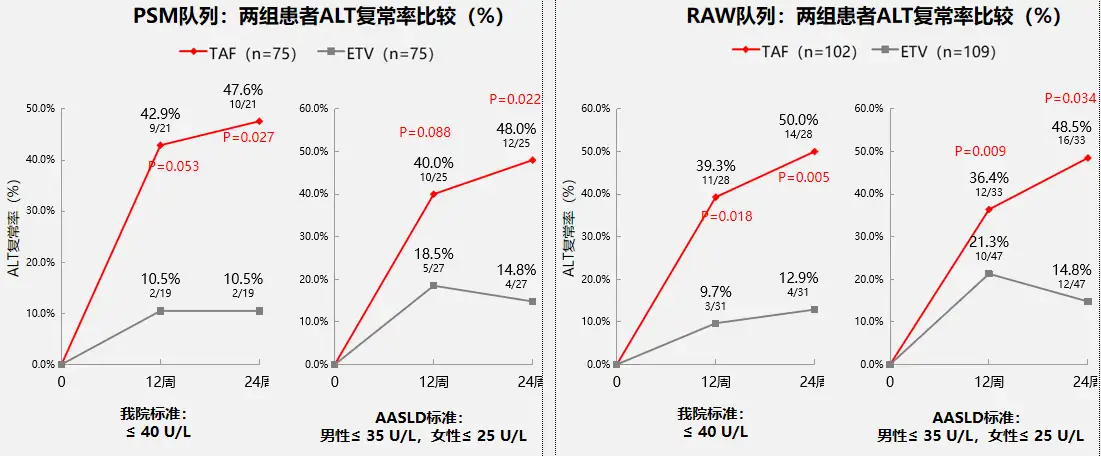
图2两组患者ALT复常率比较
安全性终点方面数据显示,换用TAF组与继续ETV单药治疗耐受性均较好,两组不良事件、严重不良事件和实验室指标异常的发生率相似,且绝大部分不良事件均为轻中度,在整个随访期间两组均无患者因不良事件而停药,PSM队列中治疗24周时,两组平均估算肾小球滤过率(eGFR)下降程度无显著差异(1.1%/1.5%,p=0.707)。这项研究数据为ETV治疗后出现LLV的患者,换用TAF治疗提供了疗效和安全性证据。
其它NA应答不佳患者,换用TAF可实现良好病毒学应答
虽然近年来在CHB抗病毒治疗中,TAF等高耐药屏障药物已经成为主要选择,但我国曾广泛应用LAM等低耐药屏障药物,多项HBV耐药监测研究显示,我国经治CHB患者中约40%存在耐药相关突变,其中LAM耐药相关位点最为常见[6-7],且ETV与LAM等药物存在交叉耐药。而目前尚未发现TAF存在与其它NAs的交叉耐药,因此对存在LAM、ETV等药物耐药位点,其它NAs治疗应答不佳的患者,使用TAF可能是较好的治疗选择。
2020年AASLD年会上发表的一项日本前瞻性真实世界研究[8],共纳入38例其它NAs应答不佳(定义为病毒学突破,即HBVDNA相对最低值上升≥1log10IU/mL和/或NAs经治超过1年HBVDNA仍≥2log10IU/ml,维持不完全病毒学抑制)的CHB患者,评估换用TAF治疗1年后的病毒学应答(HBVDNA<10IU/mL)情况,并根据患者基因型耐药位点,对疗效进行分层分析。
7例此前接受过TDF治疗的患者,仅2例(28.6%)接受TAF治疗后达到病毒学应答;31例此前治疗方案不含TDF的患者,换用TAF治疗后25例(80.6%)达到病毒学应答(p=0.014),根据耐药位点进行的分层分析如图[YL27]3所示,基线高HBVDNA[YL28][V29]水平(≥4.3log10IU/ml)且[YL30]HBeAg阳性和对TDF应答不佳,[YL31]与换用TAF治疗病毒学应答比例较低有关。因此对其它NAs应答不佳,尤其是LAM/ETV耐药的难治患者,换用TAF可取得良好的病毒学应答。
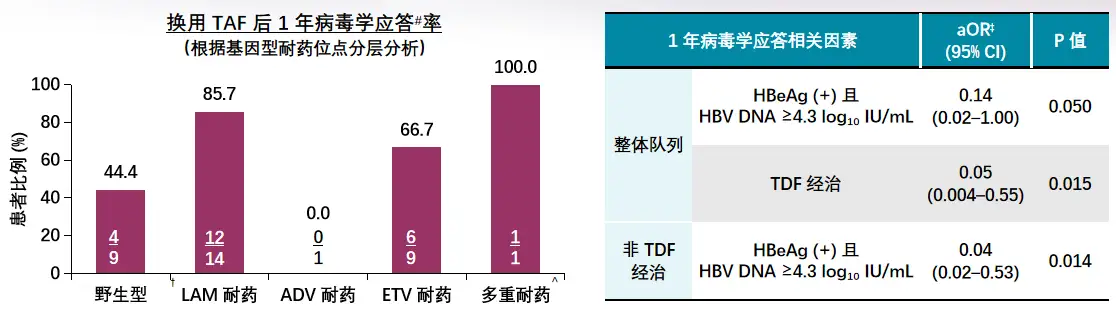
图3其它NAs应答不佳患者换用TAF治疗后的病毒学应答情况
经治患者换用TAF,短期和长期数据均提示肾脏安全性改善
上文列举的多项经治CHB患者换用TAF真实世界研究,大多对eGFR等肾功能指标进行过分析,评价TAF治疗的肾脏安全性,还有一些真实世界研究则专门从这一角度出发,评价CHB患者换用TAF后,肾功能指标、近端肾小管标志物的变化情况。
例如一项入组72例TDF经治CHB患者的单中心、前瞻性真实世界研究显示,患者换用TAF治疗24周后,近端肾小管标志物水平即显著下降,β2M:Cr比值从基线时的1.5降至1.1(p<0.01)、视黄醇结合蛋白(RBP):Cr比值从基线时的1.7降至1.4(P<0.01)[9],治疗72周时两种标志物仍维持较基线时显著下降的状态(P<0.01),且仅有两例CKD2期患者进展至3期,提示患者整体肾功能维持较好[10]。
一项加拿大真实世界研究[11]共纳入176例基线eGFR为60-90mL/min/1.73㎡,即已存在轻度肾功能损伤,且使用TAF治疗的CHB患者,其中126例(73%)为TDF换用TAF,43例(25%)为其它NAs换用TAF,其余为初治CHB患者,随访评估TAF治疗期间(最长随访160周)的肾功能指标变化情况。
研究数据显示,患者此前在TDF治疗期间,eGFR每月平均下降0.18mL/min/1.73㎡(p=0.008),但换用TAF治疗后,eGFR指标维持稳定(±0.00mL/min/1.73㎡,p=0.02,见图13),血磷也有改善趋势(TAF治疗后上升1.0log10IU/mL,p=0.2),提示从TDF换用TAF后患者肾功能指标有改善趋势。
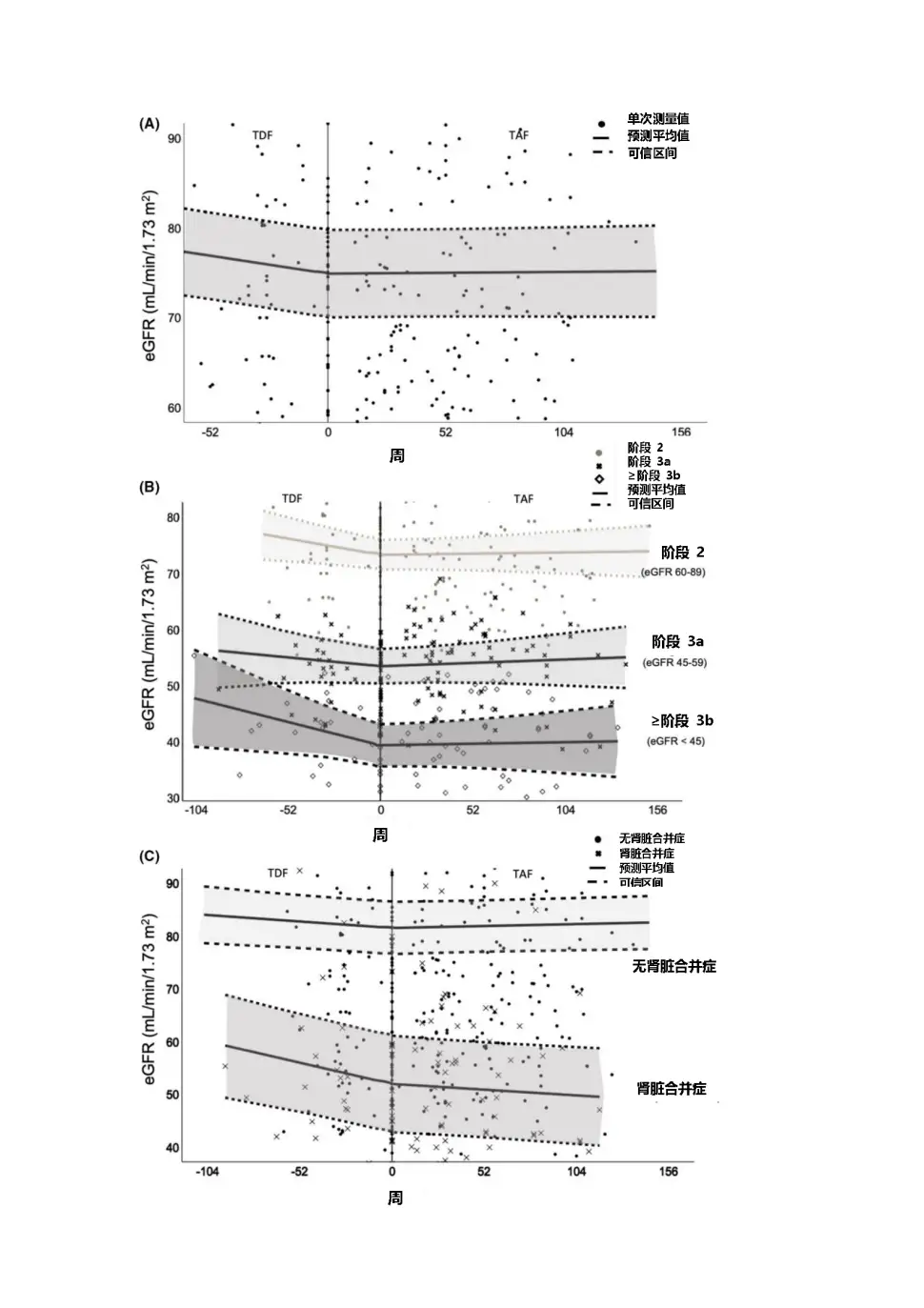
图4患者换用TAF前后的eGFR指标变化情况
2020年AASLD年会上一项意大利前瞻性、真实世界研究[12],评价了从TDF±ADV换用TAF治疗后,患者近端肾小管标志物的早期变化,研究共入组146例TDF经治CHB患者,基线特征如表1所示,患者主要因符合2017年EASL指南中年龄或骨肾风险标准而换用TAF治疗。
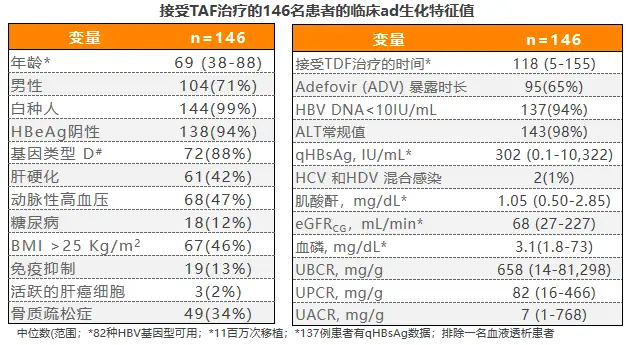
表1患者基线特征情况
患者换用TAF治疗6个月时,病毒学应答率维持稳定,ALT无明显变化,无患者因治疗不良事件停药。换用TAF治疗2个月后,患者β2M:Cr由基线时的658mg/g降至433mg/g,治疗6个月时进一步降至315mg/g;77例基线β2M:Cr异常患者中,24例在6个月时复常;此外患者尿蛋白/肌酐比(UPCR)整体明显下降,MDRD公式估算的eGFR维持稳定,提示换用TAF后肾功能保持良好,换用TAF能快速改善近端肾小管功能(见表2)。
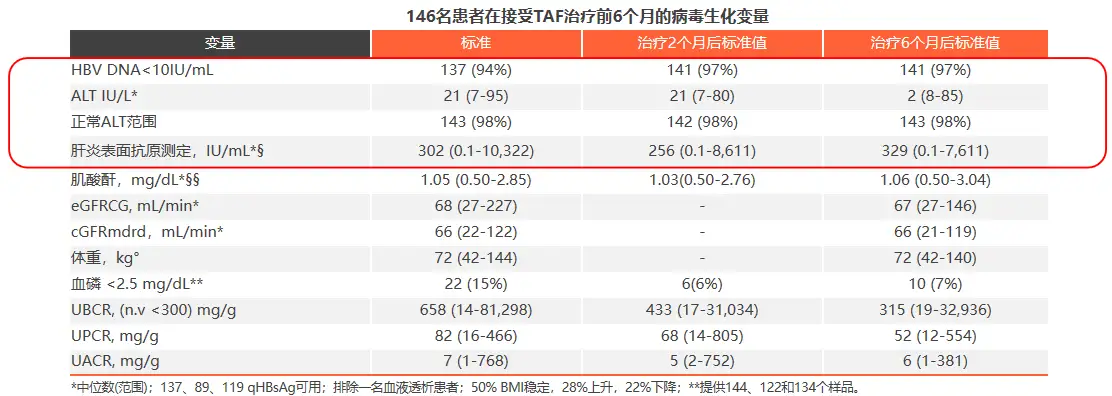
表2患者病毒学与生化特征指标变化情况
换用TAF治疗对血脂影响小,合并糖尿病的患者用药安全性良好
在TAF的关键临床研究108/110中,患者由TDF转换为TAF治疗时,会出现总胆固醇(TC)、甘油三酯(TG)、低密度脂蛋白胆固醇(LDL-C)、高密度脂蛋白胆固醇(HDL-C)等血脂指标的小幅上升[13],但有研究认为其原因是TDF治疗导致的血脂下降,并不能认为TAF有“升高患者血脂”,甚至增加心血管风险的作用[14]。
2021年亚太肝病研究学会(APASL)年会上,两项来自中国的真实世界研究提供了TAF治疗对CHB患者血脂水平影响的最新数据,第一项单中心、回顾性队列研究[15]共纳入499例ETV单药治疗≥12个月,且应答不佳(定义为HBVDNA水平30-2000IU/mL)的CHB患者,其中104例换用TAF治疗,剩余患者继续使用ETV,两组患者除年龄外的基线特征无显著差异,研究评价治疗24周时治疗的病毒学、生化学应答和患者血脂变化情况。
由ETV转换为TAF治疗24周后,79.4%患者达到病毒学应答(HBVDNA<30IU/mL),显著优于继续使用ETV组的9.1%(p<0.001);TAF治疗组24周时ALT正常(<40U/L)比例为92.6%,显著优于ETV组的80.6%(p=0.014),提示换用TAF后治疗生化学应答有所改善。而对换用TAF治疗组中31例患者进行的血脂水平分析显示,治疗24周时患者TC、TG、LDL-C、HDL-C水平较基线时无显著变化(见表3)。
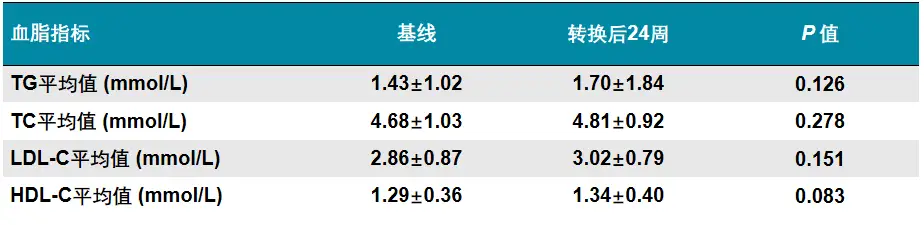
表3ETV治疗应答不佳患者换用TAF后血脂变化
另一项我国单中心真实世界研究[16],则评价了TAF用于合并糖尿病CHB患者的血脂水平变化情况,入组的34例患者中有28例为其它NA经治患者。换用TAF治疗24周时的血脂指标显示,患者TC、TG、LDL-C、HDL-C水平及TC/HDL比值较基线时无显著变化(见表4),且初治CHB患者、由TDF换用TAF患者、由ETV换用TAF患者亚组结论与整体人群相似。此研究结果显示TAF用于慢性肾脏病风险相对较高的糖尿病患者,不会显著影响血脂水平。
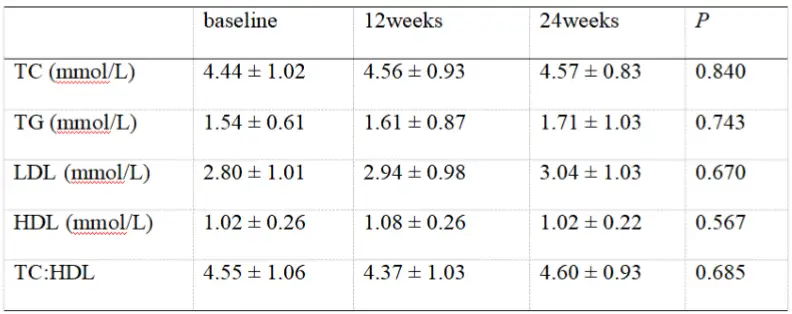
表4TAF治疗合并糖尿病CHB患者24周时的血脂变化
结语
用于LLV患者、其它NAs应答不佳患者等临床情况状况各异的人群时,TAF治疗都体现了良好的抗病毒效果和肾脏安全性,这为TAF成为多种不同患者人群的优选治疗方案提供了重要依据,对临床实践也有很大的参考意义。未来随着TAF治疗的数据和经验不断积累,还会有更多真实世界研究提供更全面、细致的信息,更好地指导TAF的临床应用。
参考文献:
1.JanssenHLA,etal.EASL2021,AbstractPO-2395.
2.LimYS,etal.EASL2021,AbstractPO-2338.
3.TerraultNA,LokASF,McMahonBJ,etal.Updateonprevention,diagnosis,andtreatmentofchronichepatitisB:AASLD2018hepatitisBguidance[J].Hepatology,2018,67(4):1560-1599.
4.OgawaE,NomuraH,NakamutaM,etal.Tenofoviralafenamideafterswitchingfromentecavirornucleos(t)idecombinationtherapyforpatientswithchronichepatitisB[J].LiverInternational,2020,40(7):1578-1589.
5.LiZB,LiL,NiuXX,etal.SwitchingfromentecavirtotenofoviralafenamideforchronichepatitisBpatientswithlow‐levelviraemia[J].LiverInternational,2021,41(6):1254-1264.
6.LiX,LiuY,XinS,etal.Comparisonofdetectionrateandmutationalpatternofdrug-resistantmutationsbetweenalargecohortofgenotypeBandgenotypeChepatitisBvirus-infectedpatientsinNorthChina[J].MicrobialDrugResistance,2017,23(4):516-522.
7.GuoX,WuJ,WeiF,etal.TrendsinhepatitisBvirusresistancetonucleoside/nucleotideanaloguesinNorthChinafrom2009–2016:aretrospectivestudy[J].InternationalJournalofAntimicrobialAgents,2018,52(2):201-209.
8.HosakaT,etal.AASLD2020,Abstract817.
9.FongTL,etal.DDW2018,AbstractSa1499.
10.LeeBT,ChangM,LimC,etal.Boneandrenalsafetyprofileat72weeksafterswitchingtotenofoviralafenamideinchronichepatitisBpatients[J].JGHOpen,2021,5(2):258-263.
11.FaragMS,FungS,TamE,etal.EffectivenessandRenalSafetyofTenofovirAlafenamideFumarateamongChronicHepatitisBPatients:Real‐WorldStudy[J].JournalofViralHepatitis,2021,28(6):942-950.
12.LoglioA,etal.AASLD2020.Abstract791.
13.AgarwalK,BrunettoM,SetoWK,etal.96weekstreatmentoftenofoviralafenamidevs.tenofovirdisoproxilfumarateforhepatitisBvirusinfection[J].JournalofHepatology,2018,68(4):672-681.
14.TaramassoL,DiBiagioA,RiccardiN,etal.Lipidprofilechangingsafterswitchingfromrilpivirine/tenofovirdisoproxilfumarate/emtricitabinetorilpivirine/tenofoviralafenamide/emtricitabine:Differenteffectsinpatientswithorwithoutbaselinehypercholesterolemia[J].PloSOne,2019,14(10):e0223181.
15.Yanetal.APASL2021,PosterH-36.
16.ZhaoJ,etal.APASL2021,PosterH-2.
-
丙酚替诺福韦(TAF)作为强效低耐药的核苷酸类似物药物 ,在慢性乙型肝炎(CHB)中的治疗价值已得到高度认可,但随着抗病毒治疗效果的改善,CHB治疗中也出现了一些需要应对的新问题,如对慢性非传染性疾病较多的老年患者、肝/肾功能损伤患者等群体,抗病毒方案的选择就需要细化。近年来多项临床研究已显示,TAF用于CHB多种不同患者人群有着良好的有效性和安全性[1-2],而各种真实世界研究进一步证实了TAF的治疗价值,本文将对多项相关研究进行解读。
低病毒血症患者改用TAF,可改善病毒学应答状况
对经治且存在低病毒血症(LLV,美国AASLD指南定义为HBV DNA20~2000 IU/mL[3])的患者,换用TAF治疗有望提升完全病毒学应答(CVR)比例。如日本多中心、回顾性KULDS研究,共入组313例≥20岁,治疗至少2年的经治CHB患者,其中191例接受恩替卡韦(ETV)治疗,122例接受其他核苷(酸)类似物(NA)联合治疗治疗。
研究评估患者换用TAF治疗48周时的疗效及肾脏安全性,其中ETV经治患者基线有34例LLV患者,换用TAF治疗48周后33例达到CVR(HBV DNA≤20 IU/mL),比例高达97.1%;基于TDF或ADV的NA联合治疗组基线有9例LLV患者,换用TAF治疗后也有7例达到CVR[4]。
我国学者开展的一项前瞻性、单中心真实世界研究[5],共入组211例ETV单药治疗≥48周后为LLV的CHB患者,按患者意愿继续ETV单药治疗(109例)或换用TAF(102例),评价治疗24周时的CVR(HBV DNA <20 IU/mL)比例,次要终点包括HBV DNA下降程度及ALT 复常率,安全性终点包括治疗不良事件、肾功能变化等,其中150例患者纳入倾向性评分匹配(PSM)队列,继续ETV治疗和换用TAF的患者各有75例,组间基线特征整体相近。
不论是在PSM队列还是在原始队列(RAW队列)中,治疗12、24周时换用TAF组患者的CVR比例(见图1)均显著高于ETV单药治疗组;治疗24周时在PSM队列中,换用TAF患者HBV DNA定量平均降幅为1.99 log10 IU/ml,显著高于ETV组的0.76 log10 IU/ml(p=0.002),RAW队列中降幅则分别为2.2 log10 IU/ml和0.74 log10 IU/ml,TAF组降幅仍显著更高(p<0.001)。
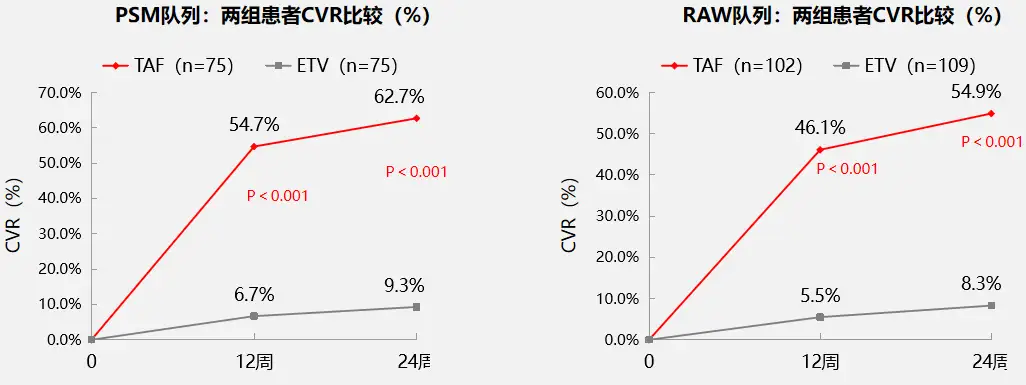
图1 两组LLV患者CVR情况比较
按中心实验室标准或2018年AASLD标准评价的ALT复常率,至24周时不论是PSM队列还是RAW队列,TAF组均显著高于ETV组(见图2,12周时PSM队列TAF组的ALT复常率数值上更高,但差异尚未达到统计学显著性),但无论在PSM或RAW队列中,两组患者HBeAg转阴率/血清转换率、qHBsAg变化等HBV生物标志物变化,肝硬度测量等无创性肝纤维化测量结果均无显著差异。
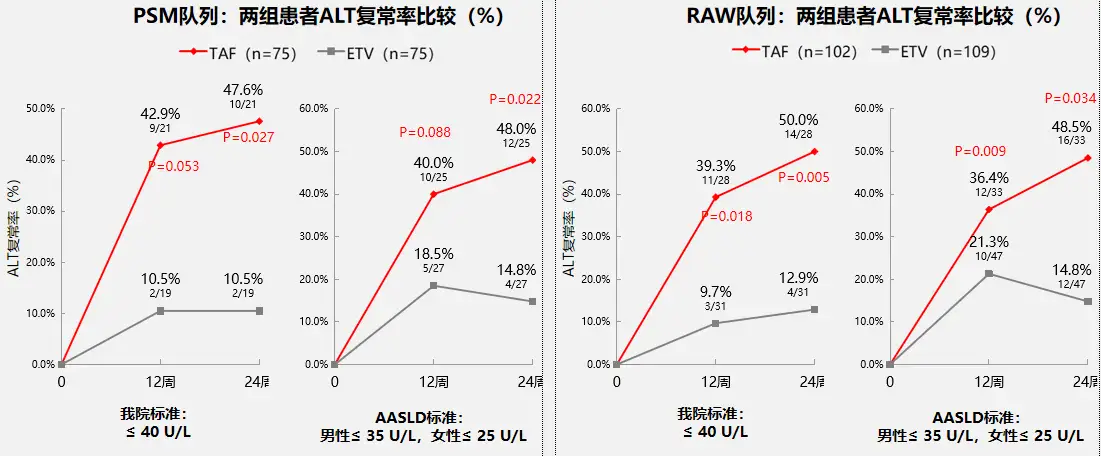
图2 两组患者ALT复常率比较
安全性终点方面数据显示,换用TAF组与继续ETV单药治疗耐受性均较好,两组不良事件、严重不良事件和实验室指标异常的发生率相似,且绝大部分不良事件均为轻中度,在整个随访期间两组均无患者因不良事件而停药,PSM队列中治疗24周时,两组平均估算肾小球滤过率(eGFR)下降程度无显著差异(1.1%/1.5%,p=0.707)。这项研究数据为ETV治疗后出现LLV的患者,换用TAF治疗提供了疗效和安全性证据。
其它NA应答不佳患者 ,换用TAF可实现良好病毒学应答
虽然近年来在CHB抗病毒治疗中,TAF等高耐药屏障药物已经成为主要选择,但我国曾广泛应用LAM等低耐药屏障药物,多项HBV耐药监测研究显示,我国经治CHB患者中约40%存在耐药相关突变,其中LAM耐药相关位点最为常见[6-7],且ETV与LAM等药物存在交叉耐药。而目前尚未发现TAF存在与其它NAs的交叉耐药,因此对存在LAM、ETV等药物耐药位点,其它NAs治疗应答不佳的患者,使用TAF可能是较好的治疗选择。
2020年AASLD年会上发表的一项日本前瞻性真实世界研究[8],共纳入38例其它NAs应答不佳(定义为病毒学突破,即HBV DNA相对最低值上升≥1 log10 IU/mL和/或NAs经治超过1年HBV DNA仍≥2 log10 IU/ml,维持不完全病毒学抑制)的CHB患者,评估换用TAF治疗1年后的病毒学应答(HBV DNA <10 IU/mL)情况,并根据患者基因型耐药位点,对疗效进行分层分析。
7例此前接受过TDF治疗的患者,仅2例(28.6%)接受TAF治疗后达到病毒学应答;31例此前治疗方案不含TDF的患者,换用TAF治疗后25例(80.6%)达到病毒学应答(p=0.014),根据耐药位点进行的分层分析如图[YL27] 3所示,基线高HBV DNA[YL28] [V29] 水平(≥4.3 log10 IU/ml)且[YL30] HBeAg阳性和对TDF应答不佳,[YL31] 与换用TAF治疗病毒学应答比例较低有关。因此对其它NAs应答不佳,尤其是LAM/ETV耐药的难治患者,换用TAF可取得良好的病毒学应答。
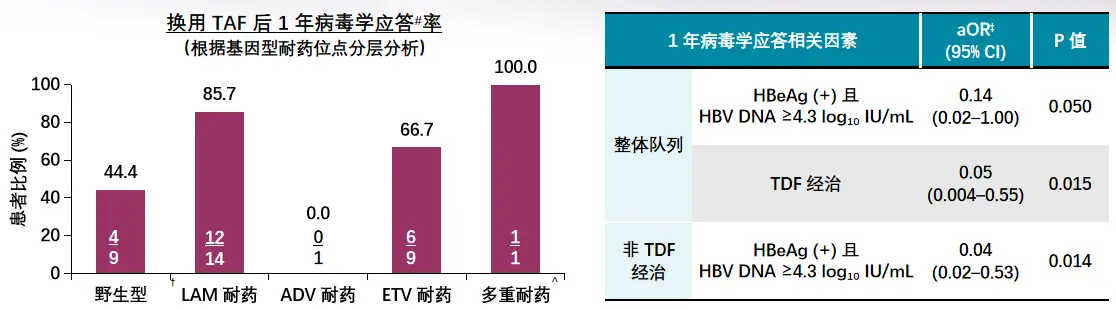
图3 其它NAs应答不佳患者换用TAF治疗后的病毒学应答情况
经治患者换用TAF,短期和长期数据均提示肾脏安全性改善
上文列举的多项经治CHB患者换用TAF真实世界研究,大多对eGFR等肾功能指标进行过分析,评价TAF治疗的肾脏安全性,还有一些真实世界研究则专门从这一角度出发,评价CHB患者换用TAF后,肾功能指标、近端肾小管标志物的变化情况。
例如一项入组72例TDF经治CHB患者的单中心、前瞻性真实世界研究显示,患者换用TAF治疗24周后,近端肾小管标志物水平即显著下降,β2M:Cr比值从基线时的1.5降至1.1(p<0.01)、视黄醇结合蛋白(RBP):Cr比值从基线时的1.7降至1.4(P<0.01)[9],治疗72周时两种标志物仍维持较基线时显著下降的状态(P<0.01),且仅有两例CKD2期患者进展至3期,提示患者整体肾功能维持较好[10]。
一项加拿大真实世界研究[11]共纳入176例基线eGFR为60-90 mL/min/1.73㎡,即已存在轻度肾功能损伤,且使用TAF治疗的CHB患者,其中126例(73%)为TDF换用TAF,43例(25%)为其它NAs换用TAF,其余为初治CHB患者 ,随访评估TAF治疗期间(最长随访160周)的肾功能指标变化情况。
研究数据显示,患者此前在TDF治疗期间,eGFR每月平均下降0.18 mL/min/1.73㎡(p=0.008),但换用TAF治疗后 ,eGFR指标维持稳定(±0.00 mL/min/1.73㎡,p=0.02,见图13),血磷也有改善趋势(TAF治疗后上升1.0 log10 IU/mL,p=0.2),提示从TDF换用TAF后患者肾功能指标有改善趋势。
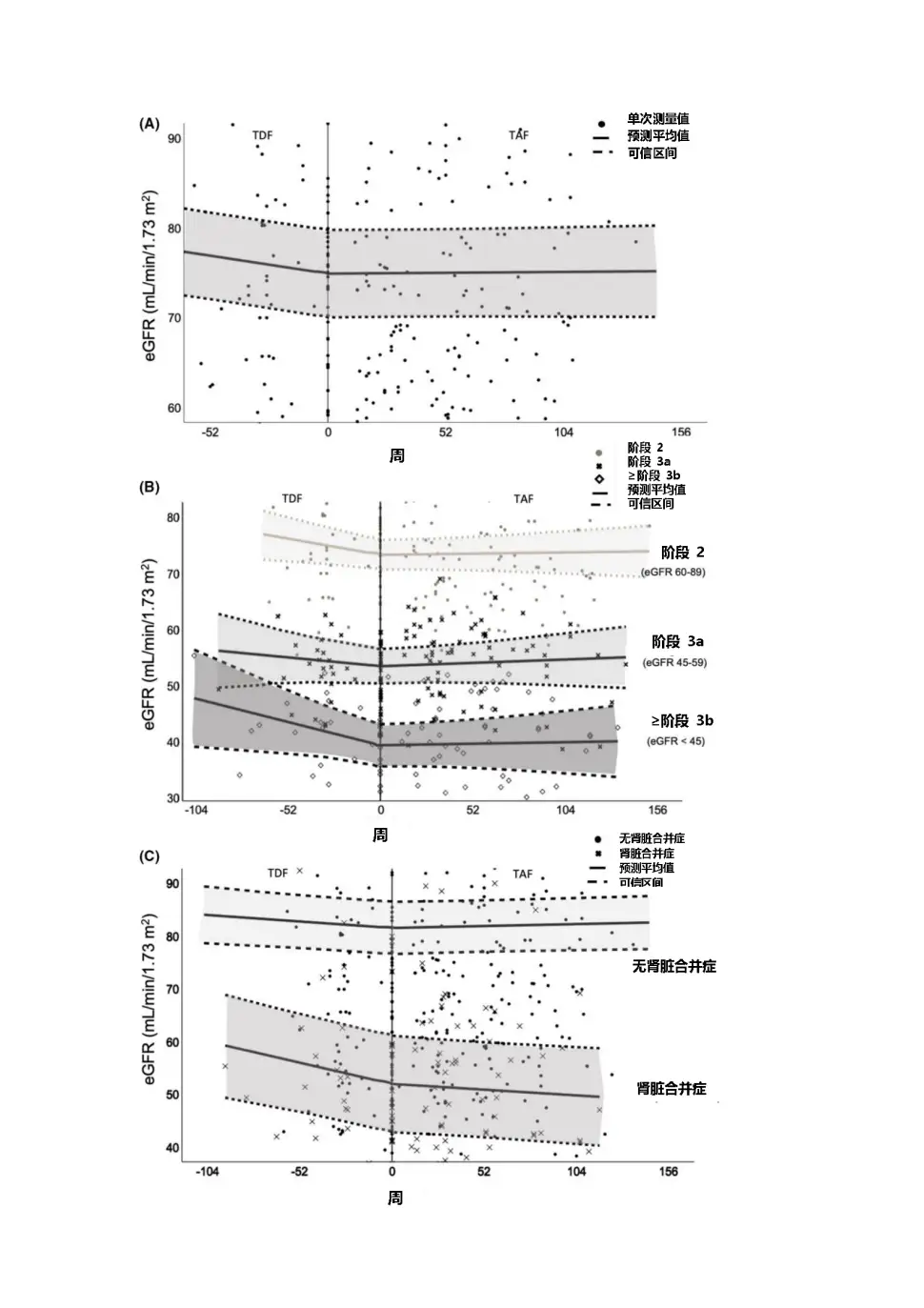
图4 患者换用TAF前后的eGFR指标变化情况
2020年AASLD年会上一项意大利前瞻性、真实世界研究[12],评价了从TDF±ADV换用TAF治疗后,患者近端肾小管标志物的早期变化,研究共入组146例TDF经治CHB患者 ,基线特征如表1所示,患者主要因符合2017年EASL指南中年龄或骨肾风险标准而换用TAF治疗。
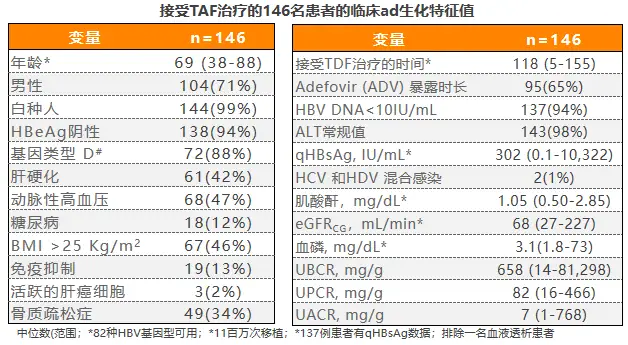
表1 患者基线特征情况
患者换用TAF治疗6个月时,病毒学应答率维持稳定,ALT无明显变化,无患者因治疗不良事件停药。换用TAF治疗2个月后,患者β2M:Cr由基线时的658mg/g降至433mg/g,治疗6个月时进一步降至315mg/g;77例基线β2M:Cr异常患者中,24例在6个月时复常;此外患者尿蛋白/肌酐比(UPCR)整体明显下降,MDRD公式估算的eGFR维持稳定,提示换用TAF后肾功能保持良好,换用TAF能快速改善近端肾小管功能(见表2)。

表2 患者病毒学与生化特征指标变化情况
换用TAF治疗对血脂影响小,合并糖尿病的患者用药安全性良好
在TAF的关键临床研究108/110中,患者由TDF转换为TAF治疗时,会出现总胆固醇(TC)、甘油三酯(TG)、低密度脂蛋白胆固醇(LDL-C)、高密度脂蛋白胆固醇(HDL-C)等血脂指标的小幅上升[13], 但有研究认为其原因是TDF治疗导致的血脂下降,并不能认为TAF有“升高患者血脂”,甚至增加心血管风险的作用[14]。
2021年亚太肝病研究学会(APASL)年会上,两项来自中国的真实世界研究提供了TAF治疗对CHB患者血脂水平影响的最新数据,第一项单中心、回顾性队列研究[15]共纳入499例ETV单药治疗≥12个月,且应答不佳(定义为HBV DNA水平30-2000 IU/mL)的CHB患者,其中104例换用TAF治疗,剩余患者继续使用ETV,两组患者除年龄外的基线特征无显著差异 ,研究评价治疗24周时治疗的病毒学、生化学应答和患者血脂变化情况。
由ETV转换为TAF治疗24周后,79.4%患者达到病毒学应答(HBV DNA <30 IU/mL),显著优于继续使用ETV组的9.1%(p<0.001);TAF治疗组24周时ALT正常(<40 U/L)比例为92.6%,显著优于ETV组的80.6%(p=0.014),提示换用TAF后治疗生化学应答有所改善。而对换用TAF治疗组中31例患者进行的血脂水平分析显示,治疗24周时患者TC、TG、LDL-C、HDL-C水平较基线时无显著变化(见表3)。
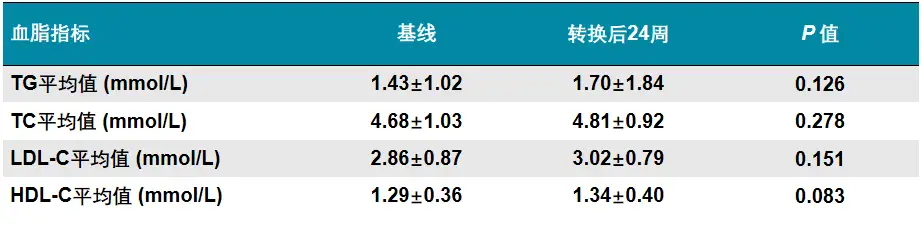
表3 ETV治疗应答不佳患者换用TAF后血脂变化
另一项我国单中心真实世界研究[16],则评价了TAF用于合并糖尿病CHB患者的血脂水平变化情况,入组的34例患者中有28例为其它NA经治患者。换用TAF治疗24周时的血脂指标显示,患者TC、TG、LDL-C、HDL-C水平及TC/HDL比值较基线时无显著变化(见表4),且初治CHB患者、由TDF换用TAF患者、由ETV换用TAF患者亚组结论与整体人群相似 。此研究结果显示TAF用于慢性肾脏病风险相对较高的糖尿病患者,不会显著影响血脂水平。
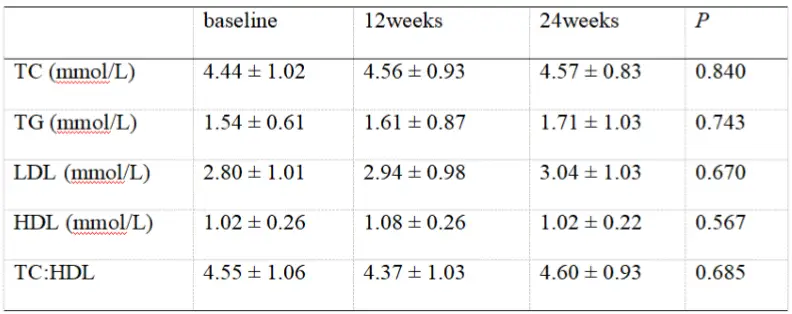
表4 TAF治疗合并糖尿病CHB患者24周时的血脂变化
结语
用于LLV患者、其它NAs应答不佳患者等临床情况状况各异的人群时,TAF治疗都体现了良好的抗病毒效果和肾脏安全性,这为TAF成为多种不同患者人群的优选治疗方案提供了重要依据,对临床实践也有很大的参考意义。未来随着TAF治疗的数据和经验不断积累,还会有更多真实世界研究提供更全面、细致的信息,更好地指导TAF的临床应用。
参考文献:
1. Janssen H L A, et al. EASL 2021, Abstract PO-2395.
2. Lim Y S, et al. EASL 2021, Abstract PO-2338.
3. Terrault N A, Lok A S F, McMahon B J, et al. Update on prevention, diagnosis, and treatment of chronic hepatitis B: AASLD 2018 hepatitis B guidance[J]. Hepatology, 2018, 67(4): 1560-1599.
4. Ogawa E, Nomura H, Nakamuta M, et al. Tenofovir alafenamide after switching from entecavir or nucleos (t) ide combination therapy for patients with chronic hepatitis B[J]. Liver International, 2020, 40(7): 1578-1589.
5. Li Z B, Li L, Niu X X, et al. Switching from entecavir to tenofovir alafenamide for chronic hepatitis B patients with low‐level viraemia[J]. Liver International, 2021, 41(6): 1254-1264.
6. Li X, Liu Y, Xin S, et al. Comparison of detection rate and mutational pattern of drug-resistant mutations between a large cohort of genotype B and genotype C hepatitis B virus-infected patients in North China[J]. Microbial Drug Resistance, 2017, 23(4): 516-522.
7. Guo X, Wu J, Wei F, et al. Trends in hepatitis B virus resistance to nucleoside/nucleotide analogues in North China from 2009–2016: a retrospective study[J]. International Journal of Antimicrobial Agents, 2018, 52(2): 201-209.
8. Hosaka T, et al. AASLD 2020, Abstract 817.
9. Fong T L, et al. DDW 2018, Abstract Sa1499.
10. Lee B T, Chang M, Lim C, et al. Bone and renal safety profile at 72 weeks after switching to tenofovir alafenamide in chronic hepatitis B patients[J]. JGH Open, 2021, 5(2): 258-263.
11. Farag M S, Fung S, Tam E, et al. Effectiveness and Renal Safety of Tenofovir Alafenamide Fumarate among Chronic Hepatitis B Patients: Real‐World Study[J]. Journal of Viral Hepatitis, 2021, 28(6): 942-950.
12. Loglio A, et al. AASLD 2020. Abstract 791.
13. Agarwal K, Brunetto M, Seto W K, et al. 96 weeks treatment of tenofovir alafenamide vs. tenofovir disoproxil fumarate for hepatitis B virus infection[J]. Journal of Hepatology, 2018, 68(4): 672-681.
14. Taramasso L, Di Biagio A, Riccardi N, et al. Lipid profile changings after switching from rilpivirine/tenofovir disoproxil fumarate/emtricitabine to rilpivirine/tenofovir alafenamide/emtricitabine: Different effects in patients with or without baseline hypercholesterolemia[J]. PloS One, 2019, 14(10): e0223181.
15. Yan et al. APASL 2021, Poster H-36.
16. Zhao J, et al. APASL 2021, Poster H-2. -
我一直觉得自己很健康,直到那天我突然感到全身乏力,头晕目眩,连站起来都成问题。我的心跳加速,手脚冰冷,仿佛世界都在旋转。我知道这不是普通的感冒或疲劳,于是决定寻求专业的医疗帮助。
在普陀区的一家医院,我遇到了医生医生。他们非常耐心地听我描述症状,并要求我进行一系列检查。经过血液测试和其他诊断程序,医生医生告诉我我患有乙型肝炎,并需要长期服用倍信富马酸替福韦二吡呋酯片来控制病情。
我对这个消息感到震惊和恐惧,但医生医生安慰我说,虽然乙型肝炎是一种慢性病,但只要我按照医嘱服药并定期复查,我的生活质量可以保持正常。他们还给了我一些建议,如何通过健康的生活方式来帮助我更好地管理病情。
在接下来的几个月里,我严格遵守医生的建议,定期服药并进行复查。虽然有时候我会忘记服药或感到沮丧,但每次我都能想起医生医生的鼓励和支持,重新振作起来。
现在,我已经可以正常工作和生活了。虽然乙型肝炎仍然存在于我的体内,但我知道只要我坚持治疗和健康的生活方式,我就能与它共存,并过上正常的生活。

-
我是来自汉中市的一位乙肝患者,最近在网上看到了一个关于乙肝两对半1345阳性的问题,深深地触动了我。我的故事开始于几年前,当我第一次被诊断出乙肝时,我的世界仿佛崩塌了。从那时起,我开始了漫长而艰难的治疗之路。
在这段时间里,我经历了无数的焦虑和恐惧。每次去医院检查,都会有种不祥的预感,担心自己的病情会恶化。然而,随着时间的推移,我逐渐学会了如何与这个疾病共存,如何正确地管理自己的健康。
在一次偶然的机会中,我接触到了京东互联网医院的线上问诊服务。起初,我对这种方式持怀疑态度,但当我真正尝试后,发现它非常方便和有效。通过视频或文字交流,我可以随时随地向专业的医生咨询问题,获取最新的治疗建议和用药指导。
这次,我向医生询问了关于乙肝两对半1345阳性的问题。医生告诉我,这意味着我有慢性乙型肝炎,病毒复制活跃,需要继续服用抗病毒药物来控制病情。虽然我已经在服用恩替卡韦分散片好几年了,但医生建议我不要轻易更改治疗方案,除非有明确的医学指示。
在医生的建议下,我也尝试了一些中成药来辅助治疗,例如蚂蚁养肝胶囊和维肝福泰片。虽然医生认为这些药物并不是必须的,但我个人感觉它们对我的身体有所帮助,可能是因为它们能够改善肝脏的代谢功能和增强免疫力。
总的来说,通过线上问诊和正确的治疗方法,我已经能够很好地控制自己的乙肝病情。虽然这个疾病仍然存在,但我不再感到恐惧和无助。我希望我的经历能够帮助其他乙肝患者,鼓励他们积极面对疾病,寻求专业的医疗帮助,并保持乐观的心态。

-
我的线上问诊之旅 那天,阳光明媚,我像往常一样,拿起手机预约了京东互联网医院的一位感染内科专家。自从有了这个便捷的平台,我再也不用为了看病而奔波于各大医院之间。
专家医生***,她总是那么耐心,尽管我有时候表达不清楚,但她总能听出我的问题所在。那天,我告诉她最近体检结果显示胆红素略高,心里有些忐忑。
医生***仔细询问了我的生活习惯,并让我上传了肝胆B超检查结果。她告诉我,胆红素略高可能是熬夜引起的,让我注意休息。同时,她还提醒我乙肝抗体检测呈阴性,需要接种乙肝疫苗。
我有些惊讶,因为去年体检时还有乙肝抗体。医生告诉我,抗体可能已经消失了,建议我接种疫苗。我立刻预约了疫苗接种,并感到安心了许多。
接下来几天,我腰酸痛的问题又困扰了我。我再次联系了医生***,她告诉我腰痛与乙肝疫苗无关,让我不必担心。
通过京东互联网医院,我不仅得到了专业的医疗建议,还感受到了医生的关怀。这种线上问诊的方式,让我在家就能享受到优质医疗服务,真是方便又贴心。
-
那是一个普通的周二下午,我坐在电脑前,心情有些沉重。自从转氨酶指标飙升到900,我就开始担心自己的健康。在朋友的推荐下,我尝试了线上问诊,希望能够得到一些专业的建议。
医生***的态度非常专业和友好,他没有直接给出治疗方案,而是耐心地询问了我的症状和病史。当我提到转氨酶指标过高时,他皱了皱眉,告诉我这需要进一步检查肝功能各项指标。
随着对话的深入,我了解到自己之所以会有这么高的指标,是因为乙肝病毒导致的。医生***建议我尽快复查,并告诉我这个药只是治标不治本,长期下去可能会引发更严重的后果。
在得知我5个月来转氨酶指标一直未降时,医生***显得有些担忧。他强调了我需要尽快去医院检查,并告诉我治疗乙肝需要住院治疗,因为这样高的指标非常危险,如果不控制住,甚至可能导致肝衰竭。
除了乙肝的问题,我还向医生咨询了关于高血压的问题。医生告诉我,我的血压虽然偏高一些,但不用担心,主要是肝功能的问题。在询问了我的血压情况后,他推荐了我可以尝试的药物。
整个问诊过程,我感受到了医生***的耐心和专业。他不仅为我提供了治疗方案,还给了我很多生活的建议。我对他非常满意,也更加坚定了治疗的决心。
医生的回复仅为建议;如您对该医生的服务满意,可在问诊记录中发起复诊;如需诊疗,请前往医院就诊。
-
我曾经是一个健康活泼的人,直到那一天我被诊断出患有慢性乙型病毒性肝炎(小三阳)。起初我并没有太在意,毕竟我从来没有感到过任何不适。但是,随着时间的推移,我的肝功能开始出现问题,DNA水平也开始上升。这种情况让我感到非常焦虑和无助。
我开始四处寻找治疗方法,去过多家医院,接受了各种检查和治疗。但是,效果并不理想。直到有一天,我在网上偶然发现了京东互联网医院,决定试一试线上问诊。
我与一位经验丰富的医生进行了交流,详细描述了我的病情和症状。医生非常耐心地听我讲述,并给出了专业的建议。他们推荐我使用恩替卡韦或替诺福韦等抗病毒药物进行治疗,并告知我要注意生活习惯,避免熬夜和饮酒,定期进行体检。
我按照医生的建议开始了治疗,并且严格遵守了他们的指导。几个月后,我的肝功能恢复正常,DNA水平也开始下降。现在,我已经完全康复了,生活也恢复了正常。
这次经历让我深刻体会到,互联网医院和线上问诊的重要性。它们不仅可以为我们提供便捷的医疗服务,还可以让我们在家中就能得到专业的医生指导和治疗。同时,我也意识到,慢性乙型病毒性肝炎并不可怕,只要我们及时采取正确的治疗措施,就可以战胜它。

-
我是一名小三阳患者,自从得知这个消息后,我的生活就像被打乱了节奏的钟表。每天都在担心、焦虑中度过,生怕病情恶化。直到有一天,我在网上偶然发现了京东互联网医院的在线问诊服务,决定试一试。
我选择了一个经验丰富的医生进行咨询,向他描述了我的症状和担忧。医生非常耐心地听完了我的描述,并详细解释了小三阳的病因、发展过程以及治疗方案。他告诉我,虽然小三阳无法根治,但通过定期检查和合理的生活方式,可以有效控制病情的进展。
在医生的指导下,我开始了新的生活方式。每天按时服药,注意饮食健康,避免过度劳累和情绪波动。同时,我也定期进行肝功能检查和乙肝病毒DNA检测,确保病情稳定。
随着时间的推移,我的病情逐渐稳定下来,生活也恢复了正常。现在,我已经可以像普通人一样工作、学习和娱乐了。感谢京东互联网医院的在线问诊服务,让我找到了正确的治疗方向和生活方式。

-
慢性乙肝是一种常见的传染性疾病,严重威胁着人类健康。近年来,随着医学研究的不断深入,我们对慢性乙肝疾病有了更全面的认识,这也促使抗乙肝病毒治疗的适应症不断扩大。
新版指南与2015年版相比,抗病毒治疗的适应症扩大主要体现在以下几个方面:
1. 基于药物可及性的实现:近年来,抗乙肝病毒药物的研发取得了显著进展,药物种类和疗效不断提高,使得更多患者能够获得有效的治疗。
2. 对疾病而言,以期通过尽早抗病毒治疗减缓疾病进展风险:慢性乙肝患者存在一定的疾病进展风险,如肝硬化、肝癌等。尽早进行抗病毒治疗,可以有效减缓疾病进展,降低并发症的发生率。
3. 反复肝功能异常,ALT>ULN,排除了其他影响因素者,建议抗病毒治疗:肝功能异常是慢性乙肝患者常见的临床表现,当ALT(谷丙转氨酶)水平超过正常上限(ULN)时,建议进行抗病毒治疗。
4. 对判定有疾病进展风险,如肝癌、肝硬化家族史者,HBV-DNA(+),也建议抗病毒:HBV-DNA(乙型肝炎病毒DNA)阳性是慢性乙肝患者存在疾病进展风险的标志,对于有肝癌、肝硬化家族史的患者,更应积极进行抗病毒治疗。
5. 抗病毒治疗目的是改善远期预后:慢性乙肝是一种慢性疾病,抗病毒治疗的目的是为了改善患者的远期预后,降低并发症的发生率。
此外,对于慢性乙肝患者,定期监测随访也非常重要。希望广大慢乙肝病友正视疾病本身,以阳光心态积极随访,积极配合医师的抗病毒处方,共同维护肝脏健康。
-
我曾经是一名慢性乙型肝炎患者,长期服用富马酸替诺福韦二吡呋酯片来控制病情。然而,最近我在郑州市的一家医院就诊时,医生建议我换用恩替卡韦片0.5mg*28片X1。起初,我对这种改变感到困惑和不安。毕竟,我已经习惯了使用旧药物,并且担心新药物的效果和副作用。
在与医生的交流中,我了解到恩替卡韦片相比于富马酸替诺福韦二吡呋酯片,具有更好的肾脏安全性和更高的抗病毒活性。医生还告知我,虽然这两种药物的剂量单位不同,但恩替卡韦片每天只需服用一粒,非常方便。
我决定听从医生的建议,开始使用恩替卡韦片。经过一段时间的服用,我发现自己的病情得到了有效控制,且没有出现明显的副作用。同时,医生也提醒我定期复查乙肝五项和病毒量,以确保治疗效果和身体状况。
这次换药经历让我深刻体会到,随着医学技术的发展,新的治疗方法和药物不断涌现。作为患者,我们需要保持开放的心态,积极配合医生的治疗方案,才能更好地管理和控制疾病。

-
我是一名中年男性,居住在齐齐哈尔市。几个月前,我开始感到疲惫无力,食欲不振,体重也在下降。起初,我并没有太在意,认为可能是工作压力大或是生活习惯不规律所致。但是,随着时间的推移,我的症状越来越明显,甚至出现了黄疸和肝区疼痛。我意识到这可能是严重的健康问题,于是决定寻求专业的医疗帮助。
在网上搜索相关信息时,我了解到恩替卡韦片是一种常用的抗病毒药物,适用于治疗乙型肝炎等疾病。由于我没有处方单,无法在药店购买这种药物。于是,我决定尝试在线问诊,希望能得到医生的帮助和指导。
通过京东互联网医院的平台,我联系了一位全科医生。医生详细询问了我的症状和病史,并告诉我需要进行肝功能检查和病毒学检测以确定诊断。医生还建议我在等待检查结果期间,保持良好的生活习惯,避免饮酒和高脂肪食物,多休息,保持心情愉快。
在医生的指导下,我完成了相关检查,并最终被确诊为乙型肝炎。医生开具了恩替卡韦片的处方,并详细解释了用药方法和注意事项。同时,医生也给予了我一些健康指导,包括如何预防疾病传播、如何改善生活方式等。
通过这次在线问诊的经历,我深刻体会到互联网医院的便利性和专业性。即使身处偏远地区,也可以轻松地获得优质的医疗服务。同时,我也意识到,面对健康问题,及时寻求专业帮助是非常重要的。只有这样,才能更好地保护自己的健康和生命。

-
那是一个平凡的下午,我坐在电脑前,心情有些忐忑。自从我发现自己是乙肝大三阳患者后,我就一直关注着相关的医疗信息。那天,我决定尝试线上问诊,希望能找到一位专业的医生为我解答心中的疑惑。
在京东互联网医院,我顺利地预约了一位肝病科的医生。医生***的态度非常和蔼,他耐心地听我讲述病情,并对我的问题一一做出解答。我告诉他,我已经有一个孩子,现在有打算要二胎,想了解一下怀孕前是否需要提前换药。
医生***告诉我,富马酸替诺福韦是可以哺乳的,如果我的DNA检测结果为阴性,那么我可以继续使用这种药物。听到这个消息,我心中的石头终于落地了。随后,我又询问了关于生完孩子是否可以换回恩替卡韦的问题,医生***建议我可以考虑换更好的丙酚替诺福韦或艾米替诺福韦。
医生***还提醒我,作为乙肝患者,我需要每三个月进行肝功、肝胆脾彩超、甲胎蛋白、乙肝五项定量、乙肝病毒定量等检查。这些信息让我对病情有了更深入的了解,也让我对未来的治疗有了信心。
在整个问诊过程中,医生***的耐心和专业让我深受感动。他不仅为我解答了所有的疑问,还为我提供了个性化的治疗方案。我知道,有了他的帮助,我的病情一定会得到更好的控制。
这次线上问诊的经历让我深刻体会到了互联网医疗的便利。在这个信息时代,我们足不出户就能享受到优质的医疗服务,这真是科技进步带给我们的福利。







































