
右侧大腿根部外侧出现了疼痛方面的临床症状,可能的原因如下:
- 右髋关节炎
- 右侧股骨头病变
- 右侧髋关节周围无菌性炎症
- 右侧梨状肌综合症
- 腰椎间盘突出压迫神经根
为了确诊和治疗这个问题,建议进行以下检查:
- 骨盆 CT 检查
- 抽血做血沉、尿酸、风湿系列的检查
- 详细了解右侧髋关节情况
- 必要时完善腰椎和右下肢神经方面的检查
根据检查结果,选择合适的药物进行治疗。除了药物治疗,还需要配合相关的康复治疗,例如:
- 疼痛区域针灸
- 推拿
- 穴位注射
- 拔火罐
- 中频等治疗
综合性的处理才能有效治疗,同时还建议减少站立行走时间,多休息,并注意身体的防风保暖,不要直接吹空调或风扇。及时处理问题,以免延误病情。

在日常生活中,坐久以后也有可能会出现髋关节疼痛方面的临床症状。
出现了髋关节疼痛方面的临床症状,需要及时检查治疗,以免延误病情。需要做骨盆 CT 检查,抽血做血沉,尿酸,风湿系列的检查,详细的了解一下髋关节和血液方面的情况,必要时还需要完善腰椎和下肢神经方面的检查,根据检查的结果看是药物保守治疗还是手术治疗。
当然,即使做了手术以后相关的药物治疗也是不能够少的,药物治疗是基础。在药物治疗的基础上,还需要配合做相关的康复治疗,比如说髋关节周围针灸,推拿,穴位注射,中频,超声波等治疗,综合性的处理,这样治疗才有效果。
减少站立行走时间多休息,要注意身体的防风保暖,不要直接吹空调吹风扇。出现了髋关节疼痛方面的临床症状,需要及时到当地三甲医院的康复科或者是疼痛科治疗,以免延误病情。
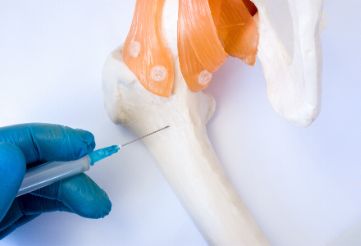
当股骨头坏死的患者进入到第3期或者是第4期的时候,需要做关节置换,有一个问题呢就提上日程,这个问题就是换一个人工髋关节到底需要多少钱?
进行全髋关节置换手术,在不同级别的医院,在不同的省市,价格可能会有所差别。我先跟大家声明的是,这种差别不是医院的自主行为定价,而是由各地的物价局以及医院的招标情况所决定的。但是总体来讲呢,全国大部分省市这种差别不会很大。主要差别在于不同等级的医院之间,花费是不相同的。
关节置换的费用其实分两部分,第1部分就是住院费,前面也提到了,住院费主要是由物价局的定价所决定的,不同级别的医院其收费是不相同的,从一两万到两三万不等。
除了这部分费用,髋关节置换还需要支付人工髋关节的商品费用,这部分费用主要是和材料以及假体设计,涂层等多种因素有关,不同的材料价格不同,从1万多到十几万的都有。一般来讲金属关节是最便宜的,半陶瓷稍贵,全陶瓷关节最贵。
所以整体的花费就由这两部分费用的加和所构成。在省级三甲医院总的花费区间应该是在从4五万到十几万之间。
很多人会问,价格这么多,怎么去选关节呢?
如同其他所有的商品一样,昂贵的关节,性价比一定不是最高,但是便宜的关节一定不是最好的,在这一点上我觉得是不能够去单纯追求性价比的,因为毕竟人工关节要植入体内一辈子。

这种场景你一定不会陌生——外公外婆带着活泼的外孙出去玩,还没玩多久,外公外婆就忍不住要扶着后背,嘴上说:“老了,不中用,得赶快找一个好地方坐一会。

走路快,腰臀痛,走路或爬高时屁股两侧不舒服等,都是髋关节炎的症状。臀部是人体在站立或活动时最重要的关节,它主要支撑人体的重量,并且能做多方向的运动,如蹲、跑、跳、跪、外展、前弯和后伸等。
但是,在日积月累的支撑和使用之后,髋关节变成了一个很容易退化的关节,这种疾病以退化性关节炎最常见,其发生与年龄密切相关,通常发生在50-60岁之间。
睡在床上真难受!
除日常生活的种种不便外,髋关节关节炎患者,也无法逃脱所有骨性关节炎患者的命运,睡眠质量严重受损。骨性关节炎患者常常难以入睡,因为脚踝、腿部、髋部、背部和颈部的疼痛使得他们很难找到舒适的睡眠姿势,英国关节炎研究基金会指出。即便是睡得很好,睡觉时很轻微的干扰或翻身,也会引起疼痛。
臀部炎症的病人平躺在床上时,需要保持髋外展的姿势,即把一只枕头平放在两腿之间,翻身侧卧时也要注意保持两腿之间的距离,大约两个枕头的高度,以保持髋外展的姿势。
此外,沐浴时建议用淋浴方式更安全方便,绝对不要坐在浴缸里;坐着或站着时要小心,千万不要突然扭动臀部,同时要保持两大腿张开的姿势;不要做让膝关节超过臀部的动作,例如:坐在过低的椅子上,蹲下马桶,或者随意做弯腰蹲下的动作。
调节生活习惯,避免症状加重。
假如已经有退化性关节炎的症状,千万不要病急乱投医,许多患者听信秘方,误服了含有类固醇成分的药物,虽然在服药初期疼痛得到明显改善,但随后却引发了一些类固醇严重的副作用,如血压升高,肾功能受损等,损害了身体的健康。

「对退化性关节炎要有正确的认识,尽量调整生活习惯,保持适当的体重,减轻关节的负担,避免因肥胖而加速发生关节炎,并使症状加重」,另外,生活中也应避免外伤及过度劳累所致的关节损伤,例如长期半蹲、全蹲或跪等姿势。
定期做一些适度的减压运动,比如简单的体操,可以增加关节周围肌肉和韧带的力量和强度,也可以减缓退化性关节炎的恶化,过一个舒适和有质量的生活。
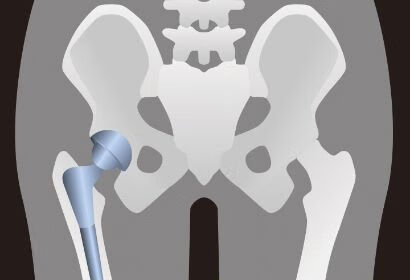
髋关节置换又称作人工髋关节置换,是将人工假体,包含股骨部分和髋臼部分,利用骨水泥和螺丝钉固定在正常的骨质上,以取代病变的关节,重建患者髋关节的正常功能,是一种较成熟丶可靠的治疗手段。
髋关节置换术适合哪些疾病呢?
- 髋关节炎,尤其是退变性的髋骨关节炎,晚期患者疼痛很严重,影响日常生活及行走。此时关节间隙变窄,甚至有些已经硬化塌陷。
- 股骨头坏死,股骨头坏死的晚期,三期、四期一般都是需要置换的,此时减压、植骨效果都不佳,股骨头已经塌陷,无法再恢复原来的形状和负重的力线。
- 股骨颈骨折,老年人的股骨颈骨折,老年人股骨颈骨折愈合比较困难,如果想要快速下地行走,建议还是进行全髋关节置换或者半髋置换。
- 风湿类的疾病,特别是强直性脊柱炎,髋关节完全融合之后,必须进行髋关节置换。
- 陈旧性骨颈骨折,影响功能。
- 退行性骨关节炎,多见于老年人。
- 慢性髋关节脱位。

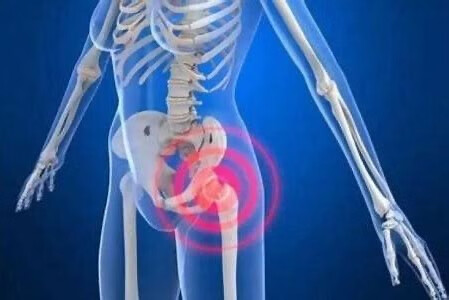
1、什么叫暂时性髋关节滑膜炎:
是儿童时期的一种常见病,表现为跛行,可以伴有或不伴有肢体疼痛。轻者髋关节检查正常。严重者可有骨盆倾斜,即患侧肢体看起来比健侧长。Thomas征(+),也就是一侧髋关节屈曲时,患侧髋关节不能伸直。或髋关节各方向活动均有受限情况。B超检查可以发现髋关节前隐窝有积液或前关节囊有增厚表现,X线检查多数正常。
2、病因:
目前对髋关节暂时性滑膜炎的发病机制还不很清楚,公认的是一种毒血症造成或创伤造成关节滑膜水肿。已知的原因按引起的频率由高到低排列依次为上呼吸道感染,特别是起病前半个月左右时间的上呼吸道感染;创伤;和原因不明。
3、治疗:
根据大量的临床总结,时间短,病变轻的病人可以采用药物治疗,大部分病儿可以在3-5天恢复正常,但为防止复发,一般主张休息两周,因此,没有必要住院治疗。对于病程超过一周和临床症状较严重者在进行药物治疗的同时还应进行牵引治疗,这些病儿才需要住院治疗。
4、与股骨头坏死关系:
多数学者在临床和试验研究中证明,髋关节暂时性滑膜炎不会引起股骨头缺血坏死。但有的病人确实存在先诊断髋关节暂时性滑膜炎,后来又确实患有股骨头缺血性坏死,这是怎么回事呢?原来股骨头缺血性坏死与髋关节暂时性滑膜炎的早期临床表现非常相似,以致于医师也无法将两者区分,也就是说有少部分被诊断为暂时性髋关节滑膜炎的病儿其实在一开始就是股骨头缺血性坏死,而不是暂时性髋关节滑膜炎。只是早期无法将两者区分,后来被证实患有股骨头缺血性坏死。因而被误认为是由暂时性髋关节滑膜炎引起的股骨头缺血性坏死。
5、后遗症:
髋关节暂时性滑膜炎是由毒血症所造成的,因此不会像化脓性感染那样治愈后会产生一些后遗症,一般治愈后不会产生后遗症,但还有少部分患儿可以有反复发作的的情况,这就需要临床医生给予注意,进行必要的检查。暂时性髋关节滑膜炎人类对它的认识也是有一个漫长的过程。在学术上使用过的名称很多,其中有一个名称叫“鬼怪髋”,是指有些病人忽好忽坏,有些病人也可以迁延几个月也不恢复正常。长期的暂时性髋关节滑膜炎可以导致关节软骨的营养障碍,从而导致以后关节退行变的提早发生。因此应该及时治疗。
6、哪些需要复查:
暂时性髋关节滑膜炎治愈后一般很少有复发的情况,治愈后一般也不会引起并发症。因此也不必到医院复查。但有些病人可能是早期的股骨头缺血性坏死患儿,不应该被医生所忽视。对于有以下情况者,临床医生应该给予重视,应按时到医院进行复查:①诊断为暂时性髋关节滑膜炎几个月不恢复正常者;②B超检查髋关节前隐窝有积液,持续6周不消失者;③短期内反复发生暂时性髋关节滑膜炎者。对有以上三种情况的患儿应定期到医院进行复查。根据股骨头缺血性坏死的临床规律,应该每3个月到医院检查一次。

作者 | 王健
文章首发于 | 骨科王健医生头条号
80岁的秦奶奶,虽然年纪大,但心态非常好,看起来身体也比较硬朗。因有3个女儿嫁在外地,所以时常会在孙子孙女的陪伴下在各个城市之间游玩。说是游玩,其实也是为了好好和自己的女儿、外孙相处,享受儿孙满堂的欢乐。

但4年前,秦奶奶右髋部出现了疼痛情况,一开始总以为是人老了,关节难免有问题,就没太在意。这么一拖,就拖到了现在,疼痛却只增不减。最近,实在是觉得受罪,于是在孩子的陪同下来我院就诊。
入院查体:跛行步态,行走速度缓慢,骨盆无倾斜,双下肢等长,右侧髋关节主动、被动活动受限。随后完善相关检查,检查示:右侧股骨头无菌性坏死,具备手术指征,术前相关检验检查未见明显手术禁忌症。

把病情告知患者及其家属后,综合各方面原因建议手术,患者及其家属都同意了。于是,在全麻下行右侧全髋关节置换术,术程顺利,术后予以止痛、护胃、补液等治疗。目前,患者恢复良好,病情稳定。

术后复查X线提示置换关节位置良好,却发现肝功异常。于是转入其他科继续保肝治疗,康复治疗。
此外,嘱咐其注意休息,清淡饮食,加强饮食营养补充,适度活动,避免长时间保持同一姿势。 在双拐支持下不全负重下下地行走,循序渐进地进行双下肢功能锻炼。
本文转载自其他网站,不可二次转载。文章内容仅供参考,具体治疗请咨询医生或相关专业人士。如有问题,可联系jdh-hezuo@jd.com。

三个月30斤,变化真的很大

39岁的邢丕侠于2024年10月6日入职冠捷科技有限公司,10月16日上午在工作中身体不适请假回宿舍休息,当天下午被送往医院抢救无效身亡,经诊断为心源性猝死。 冠捷科技工作人员表示,公司是委托中介公司招的人,员工是与中介公司签的合同,邢丕侠的情况,属于劳务派遣形式。 报道发出后,数千位网友参与该事件的评论,重点关注邢丕侠心源性猝死的原因,劳务派遣用工形式的争议,以及邢丕侠的权益该如何获得保障等。
30岁出头的小韩怀了二胎,怀孕初期经当地医院检查后考虑“先兆流产”保胎治疗。此后,生过一娃的小韩觉得自己经验丰富,竟然没做一次产检。眼看怀孕8个月,肚子还没大,小韩前往医院检查后,显示小韩没有怀孕,还有宫腔病变。 浙江省立同德医院妇科吕雯主任仔细询问了小韩情况后,又结合检查结果,告诉小韩这叫“稽留流产”,即胚胎或胎儿死亡而滞留在宫腔没有及时自然排出。而小韩胎停后遗留时间太长,需要做宫腔镜手术清除妊娠物和粘连。顺利进行手术后,吕雯主任提醒小韩,如再怀孕,一定要做好定期产检。
展开更多













