2024年10月4日,百济神州正式宣布替雷利珠单抗在美国上市[1],用于既往接受过系统化疗(不含PD-1/L1抑制剂)后不可切除或转移性食管鳞状细胞癌(ESCC)的成人患者的治疗。

作为百济神州重要管线,替雷利珠单抗适应证包括非小细胞肺癌、食管鳞状细胞癌、肝癌等领域,大多临床试验处于Ⅲ期。替雷利珠单抗这次获批是基于RATIONALE-302试验,一起来看这个单抗的有效性数据和安全信息。
有效性方面,该试验在意向治疗 (ITT) 人群中达到了主要终点:在 ITT 人群中,替雷利珠单抗组的中位总生存期 (OS) 为 8.6 个月 (95% CI: 7.5, 10.4),而化疗组为 6.3 个月 (95% CI: 5.3, 7.0) (p=0.0001;风险比 [HR]=0.70 [95% CI: 0.57, 0.85])[1]。
安全性方面,替雷利珠单抗的安全性优于化疗[1]。但本次官宣中花了很大篇幅将这个药的注意事项和不良反应,大多不良反应多为免疫相关。究其原因还是从药理机制角度解释,和很多PD-1单抗一样,替雷利珠单抗作为一种单克隆抗体,属于一类与程序性死亡受体-1 (PD-1) 或 PD-配体 1 (PD-L1) 结合的药物,阻断 PD-1/PD-L1 通路,从而消除免疫反应的抑制,可能打破外周耐受性并诱导免疫介导的不良反应。
小编将这些整理成表,用药期间如果出现其中的症状等,需要及时告知医生。
不良反应 |
发生率 |
严重程度/不良反应等级 |
措施 |
免疫介导性肺炎 |
3.8% |
可致命,2-4级 |
使用全身性皮质类固醇治疗 |
免疫介导的结肠炎 |
0.9% |
可致命,2-3级 |
停药/全身性皮质类固醇治疗 |
免疫介导的肝炎 |
1.7% |
可致命,2-4级 |
使用全身性皮质类固醇治疗 |
肾上腺皮质功能减退症 |
0.3% |
可致命,2-4级 |
使用全身性皮质类固醇治疗 |
免疫介导的垂体炎 |
0.1% |
2级 |
根据临床指征用激素替代治疗 |
免疫介导的甲状腺疾病 |
0.4% |
2级 |
使用全身性皮质类固醇治疗 |
免疫介导的甲状腺功能亢进症 |
0.6% |
2-3级 |
使用全身性皮质类固醇治疗 |
免疫介导的甲减 |
7% |
2级/4级 |
使用全身性皮质类固醇治疗 |
糖尿病酮症酸中毒 |
/ |
/ |
胰岛素治疗 |
免疫介导的肾炎 |
0.4% |
可致命,2-4级 |
使用全身性皮质类固醇治疗 |
免疫介导的皮疹或皮炎 |
1.2% |
2-4级 |
使用全身性皮质类固醇治疗 |
输液相关反应 |
4.2% |
3级及以上 |
轻度(1级)减慢输注速度; 中度(2级)输注相关反应中断输注; 对于严重(3级)或危及生命(4级)的输液相关反应,停止输注并停药。 |
如果需要停药,则给予全身性皮质类固醇治疗(1-2mg/kg/天泼尼松或等效激素类药物),直至改善至1级或更低。在改善至1级或更低级别时,开始皮质类固醇减量,并在至少1个月内继续减量。对于免疫介导的不良反应不能用皮质类固醇控制的患者,考虑给予其他全身性免疫抑制剂。
参考来源:
1.BeiGene Announces Availability of TEVIMBRA® in U.S.
2.https://www.beigenemedical.com/pipeline#container-content-2
2024年10月3日,FDA批准纳武利尤单抗(Opdivo)用于可切除非小细胞肺癌的新辅助(治疗)/ 辅助(治疗)[1]。纳武利尤单抗联合铂类双药化疗作为新辅助治疗,此后可在手术后单独使用纳武利尤单抗作为辅助治疗,用于可切除(肿瘤≥ 4cm 和/或淋巴结阳性)非小细胞肺癌 (NSCLC) 且无已知表皮生长因子受体 (EGFR) 突变或间变性淋巴瘤激酶 (ALK) 重排的成人患者。

该项获批基于Ⅲ期随机双盲试验,试验目的是围辅助治疗(新辅助治疗,然后是辅助治疗)免疫疗法是否会延长早期非小细胞肺癌患者的无事件生存期。试验主要结果主要包括无事件生存期(EFS),时间范围从随机分组至疾病进展、恶化、复发或任何原因导致的死亡(最长约 44 个月)[2]。

试验纳入了 461 例既往未经治疗且可切除的 NSCLC 患者 (IIA 期至选择 IIIB 期)。患者被随机分配 (1:1) 接受纳武利尤单抗组/对照组,接受铂类化疗,每3周一次,最多4个周期(新辅助治疗),然后继续接受纳武利尤单抗单药或安慰剂,每4周一次,最多13个周期(辅助治疗)。试验结果表明,纳武利尤单抗组未达到中位EFS (95% CI: 28.9, 不可估计 [NE]),化疗组未达到 18.4 个月 (95% CI: 13.6, 28.1) (风险比 0.58 [95% CI: 0.43, 0.78];p 值 0.00025)[2]。
安全性方面,在接受新辅助纳武利尤单抗治疗的患者中,5.3%的患者因不良反应而无法接受手术,而安慰剂组为3.5%。此外,纳武利尤单抗组接受新辅助治疗和手术的患者有4.5%因不良反应而延误手术,而安慰剂组为 3.9%[1]。
根据该药说明书,纳武利尤单抗是一种单克隆抗体,与程序性死亡受体 1 (PD-1) 或 PD 配体 1 (PD-L1) 结合的药物,阻断 PD-1/PD-L1 通路,从而消除免疫反应的抑制,可能打破外周耐受性并诱导免疫介导的不良反应。因此不良反应主要和免疫反应有关,总结如下,临床应用过程中需按医嘱用药。
A.可引起免疫介导的肺炎,发生率约为3.1%;
B.可引起免疫介导性结肠炎,发生率约为2.9%;
C.可引起免疫介导性肝炎,发生率约为1.8%
D.可导致原发性或继发性肾上腺皮质功能减退症,发生率约为1%。对于2级或更高级别的肾上腺皮质功能减退症,开始对症治疗,包括根据临床指征进行激素替代治疗。
E.可引起免疫介导的垂体炎。垂体炎可表现为与占位效应相关的急性症状,例如头痛、畏光或视野缺损。垂体炎可导致垂体功能减退症。
F.可引起免疫介导的肾炎。
G.可引起免疫介导的皮疹或皮炎,PD-1/PD-L1 阻断抗体曾发生剥脱性皮炎,包括 Stevens-Johnson 综合征、中毒性表皮坏死松解症 (TEN) 和 DRESS(伴有嗜酸性粒细胞增多症和全身症状的药疹)。
若因出现免疫反应而需停药,给予全身性皮质类固醇治疗(1 至 2 mg/kg/天泼尼松或等效药物),直到改善至1级或更低,并开始皮质类固醇减量,并在至少1个月内继续减量。对于皮质类固醇治疗无法控制免疫介导的不良反应的患者,考虑使用其他全身性免疫抑制剂。
此外,该药可引起严重的输液相关反应,在临床试验中,<1.0% 的患者报告了这种反应。对于有严重或危及生命的输液相关反应的患者,应停止使用。
参考来源:
1.FDA approves neoadjuvant/adjuvant nivolumab for resectable non-small cell lung cancer
2.A Study of Neoadjuvant Chemotherapy Plus Nivolumab Versus Neoadjuvant Chemotherapy Plus Placebo, Followed by Surgical Removal and Adjuvant Treatment With Nivolumab or Placebo for Participants With Surgically Removable Early Stage Non-small Cell Lung Cancer
3.product information:OPDIVO- nivolumab injection

欧洲药品管理局人用药品委员会 (CHMP) 发布了一条肯定意见:建议批准斯鲁利单抗(serplulimab)用于广泛期小细胞肺癌 (ES-SCLC) 患者的一线治疗[1]。
这项推荐是源于ASTRUM-005临床试验,ASTRUM-005是一项随机、双盲、多中心、III期临床研究,主要比较HLX10(重组人源化抗PD-1单克隆抗体注射液,即serplulimab)联合化疗(卡铂-依托泊苷)在先前未经治疗的广泛期小细胞肺癌(ES-SCLC)患者中的临床疗效和安全性[2]。
将符合入组条件的受试者将按照2:1的比例随机分配为2组:

A组(HLX10组):HLX10 + 化疗(卡铂-依托泊苷);
B组(安慰剂组):安慰剂 + 化疗(卡铂-依托泊苷)。
研究结果显示[3],在中位随访 12.3 个月时,治疗组患者(n = 389) 的中位总生存期 (OS) 为 15.4 个月 (95% CI,13.3-无法评估),而对照组患者为10.9个月 (n = 196,心率,0.63;95% CI,0.49-0.82;P< 0.001)。

此外,治疗组的中位无进展生存期 (PFS) 为 5.7 个月 (95% CI,5.5-6.9),对照组为 4.3 个月 (95% CI,4.2-4.5) (HR,0.48;95% CI,0.38-0.59)。这个研究结果是22年的数据,最新在2024 年 ASCO 年会上公布:治疗组患者的中位 OS 为 15.8 个月(95% CI,13.9-17.4),而安慰剂组为 11.1 个月(95% CI,10.0-12.4)(HR,0.61;95% CI,0.50-0.74;P<0.001)[4]。

安全性方面,治疗相关不良反应事件(TRAE) 的发生率为 69.9%,对照组为 56.1%。3 级及以上 TRAE 的比率分别为 33.2% 和 27.6%[4]。最常见的3级或更高级别TRAEs 包括中性粒细胞计数降低、白细胞计数降低 、血小板计数降低和贫血。
关于小细胞肺癌
小细胞肺癌 (SCLC) 是最具侵袭性的肺癌亚型,约占所有肺癌病例的 15%,其特点是快速增殖和转移。基于疾病特点,SCLC 患者通常在诊断时表现为广泛期疾病,5 年生存率仅为 7%。自 1990 年代以来,广泛期 SCLC 的标准一线治疗仍然是铂类+依托泊苷的化疗,中位总生存期约为 10 个月[3]。
关于公司
复宏汉霖(2696.HK)是一家全球性的生物制药公司,专注于为全球患者提供高质量、价格合理、创新的生物药物,专注于肿瘤、自身免疫性疾病和眼科疾病。截至目前,已有 6 个产品在中国上市,3 个产品已获准在海外市场上市,24 个适应症已在全球范围内获批,3 个产品上市申请已分别在中国和欧盟获批。自2010年成立以来,复宏汉霖已构建了集高效、创新为核心能力的生物医药一体化平台,贯穿研发、生产和商业化等产品全生命周期。它建立了全球创新中心和位于上海的商业制造设施,并通过了中国、欧盟和美国 GMP 认证。
参考文献:
1.Henlius Receives Positive CHMP Opinion for HANSIZHUANG as First-Line Treatment for Extensive-Stage Small Cell Lung Cancer
2.A Randomized, Double-blind, Placebo Controlled Phase III Study to Investigate Efficacy and Safety of HLX10 + Chemotherapy (Carboplatin- Etoposide) in Patients With Extensive Stage Small Cell Lung Cancer (ES-SCLC)
3.Cheng Y, Han L, Wu L, Chen J, Sun H, Wen G, Ji Y, Dvorkin M, Shi J, Pan Z, Shi J, Wang X, Bai Y, Melkadze T, Pan Y, Min X, Viguro M, Li X, Zhao Y, Yang J, Makharadze T, Arkania E, Kang W, Wang Q, Zhu J; ASTRUM-005 Study Group. Effect of First-Line Serplulimab vs Placebo Added to Chemotherapy on Survival in Patients With Extensive-Stage Small Cell Lung Cancer: The ASTRUM-005 Randomized Clinical Trial. JAMA. 2022 Sep 27;328(12):1223-1232. doi: 10.1001/jama.2022.16464. PMID: 36166026; PMCID: PMC9516323.
4.First-Line Serplulimab Receives Positive CHMP Opinion for ES-SCLC

2024年9月19日,强生宣布埃万妥单抗与标准化疗(卡铂和培美曲塞)联合治疗获批FDA[1],适应证为患有表皮生长因子受体(EGFR)19号外显子缺失(ex19del)或L858R替代突变的局部晚期/转移性非小细胞肺癌(NSCLC)成年患者,且这些患者在已接受/接受过 EGFR 酪氨酸激酶抑制剂 (TKI) 治疗期间。
这项获批基于MARIPOSA-2 研究,据强生官网报道,这也是今年获批的第四个适应证。
MARIPOSA-2 研究是一项开放标签、随机Ⅲ期研究,研究的主要目的是评估在奥希替尼治疗失败后的局部晚期或转移性表皮生长因子受体(EGFR)外显子 19 缺失(Exon 19del)或L858R 替代型非NSCLC患者中,埃万妥单抗与标准化疗的疗效。研究的主要结果包括无进展生存期(PFS)[2]。
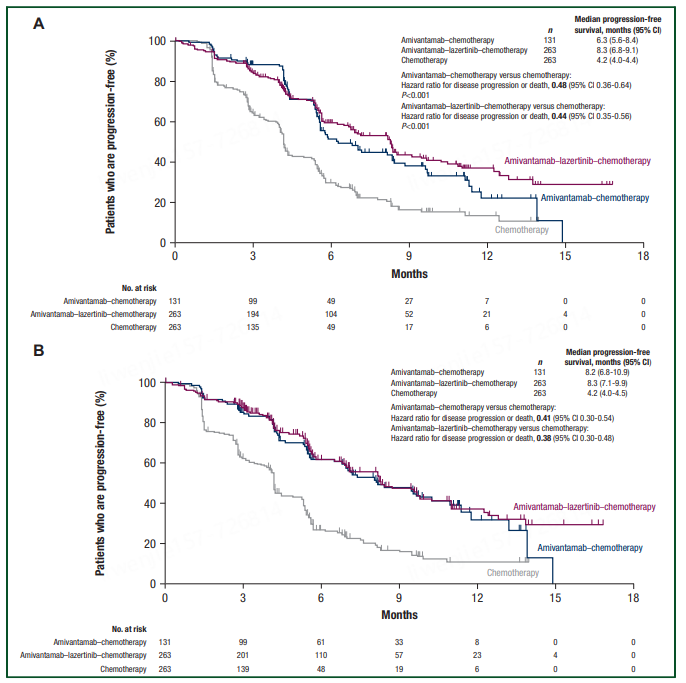
从研究结果来看,与单独化疗相比,埃万妥单抗联合化疗将疾病进展或死亡的风险(无进展生存期 [PFS])降低了 52%。且接受埃万妥单抗联合化疗的患者的中位 PFS 为 6.3 个月,而单独化疗的患者为 4.2 个月。此外,埃万妥单抗组的确认总缓解率 (ORR) 为 53%,而单独化疗为 29%[3]。埃万妥单抗联合化疗也被纳入NCCN指南[1]。
再回归到这个药物本身,埃万妥单抗是一种双特异性抗体,可与肿瘤细胞表面的EGFR和MET的结构域结合,进而通过抗体依赖性细胞毒性 (ADCC) 和胞吞作用机制分别靶向这些细胞,以被免疫效应细胞(如自然杀伤细胞和巨噬细胞)破坏[4]。目前FDA更新的说明书种,其适应证包括:
1.1 表皮生长因子受体(EGFR)外显子 19 缺失或外显子 21 L858R 替代突变的非小细胞肺癌(NSCLC)的一线治疗
1.2 表皮生长因子受体(EGFR)外显子 20 插入突变的非小细胞肺癌(NSCLC)的一线治疗
经 FDA 批准的检测方法检测,RYBREVANT 适用于与卡铂和培美曲塞联合,用于患有表皮生长因子受体(EGFR)外显子 20 插入突变的局部晚期或转移性非小细胞肺癌(NSCLC)成年患者的一线治疗。
1.3 既往接受过治疗的表皮生长因子受体(EGFR)外显子 20 插入突变的非小细胞肺癌(NSCLC)。
此外,应用该药时还要注意下列事项:
输液相关反应
该药可引发输液相关反应(IRR);输液相关反应的体征和症状包括呼吸困难、潮红、发热、寒颤、恶心、胸部不适、低血压和呕吐。输液相关反应发作的中位时间约为1小时。
间质性肺病/肺炎
该药可导致严重且致命的间质性肺病(ILD)/肺炎。
同时使用该药和拉泽替尼(Lazertinib)时的静脉血栓栓塞(VTE)事件
该药与拉泽替尼联合使用可引发严重且致命的静脉血栓栓塞(VTE)事件,包括深静脉血栓形成和肺栓塞。这些事件大多发生在治疗的前四个月内。
皮肤不良反应
该药可引起严重皮疹,包括中毒性表皮坏死松解症(TEN)、痤疮样皮炎、瘙痒和皮肤干燥。
眼毒性
该药可导致眼毒性,包括角膜炎、睑缘炎、干眼症状、结膜发红、视力模糊、视力损害、眼痒、眼部瘙痒和葡萄膜炎。
胚胎 - 胎儿毒性
基于其作用机制和动物模型的研究结果,该药用于孕妇时可能对胎儿造成伤害。将其他表皮生长因子受体(EGFR)抑制剂分子用于怀孕动物时,已导致胚胎 - 胎儿发育受损、胚胎致死和流产的发生率增加。告知有生育潜力的女性胎儿面临的潜在风险。建议有生育潜力的女性患者在接受该药治疗期间以及最后一剂该药用药后3个月内采取有效的避孕措施。
最后再来看一下公司信息:强生公司成立于1886年,是全球最具综合性、业务分布范围广的医疗健康产品企业之一,业务覆盖医疗科技和创新制药,总部位于美国新泽西州新布仑兹维克市。2023年,强生顺利完成消费者健康业务分拆,并宣布品牌焕新,将旗下医疗科技和创新制药两大业务整合至强生名下,开启百年强生的崭新征程。
参考文献:
1.RYBREVANT®(amivantamab-vmjw) plus standard of care approved in the U.S. as first and only targeted regimen to cut risk of disease progression by more than half in second-line EGFR-mutated advanced lung cancer
2.A Study of Amivantamab and Lazertinib in Combination With Platinum-Based Chemotherapy Compared With Platinum-Based Chemotherapy in Patients With Epidermal Growth Factor Receptor (EGFR)-Mutated Locally Advanced or Metastatic Non- Small Cell Lung Cancer After Osimertinib Failure (MARIPOSA-2)
3.Passaro A, Wang J, et al; MARIPOSA-2 Investigators. Amivantamab plus chemotherapy with and without lazertinib in EGFR-mutant advanced NSCLC after disease progression on osimertinib: primary results from the phase III MARIPOSA-2 study. Ann Oncol. 2024 Jan;35(1):77-90. doi: 10.1016/j.annonc.2023.10.117. Epub 2023 Oct 23. PMID: 37879444.
4.Product Information:RYBREVANT- amivantamab injection,Janssen Biotech, Inc.Updated August 23, 2024
当地时间9月12日,FDA批准首个皮下注射抗PD1免疫疗法,用于特定类型肺癌、肝癌、黑色素瘤、软组织癌。这个皮下疗法组合包括两部分组成:一部分是阿替利珠单抗;另一个是 Halozyme公司自己研制的重组人透明质酸酶rHuPH20[1]。
皮下疗法应用Halozyme的ENHANZE药物递送技术,可将原本30mim的静注时间缩短为7min。让我们一起来看支撑这项研究背后的临床试验结果。
相似的血药浓度、有效性和安全性
该获批基于一项随机多中心 Ib/III 期的试验,研究的主要目的要看看阿替利珠单抗这个药,打在皮下和打在静脉里在一些特定患者身上效果有什么不一样。这些特定患者为局部晚期或者已经转移的非小细胞肺癌患者,他们之前没做过癌症免疫治疗,而且之前用含铂类的药治疗也没效果。
试验的主要结果显示,皮下注射atezolizumab和静脉注射 atezolizumab 的几何平均比值 (GMR) 为1.05 (90% CI,0.88-1.24),AUC 0-21 天为 0.87 (90% CI,0.83-0.92),这表明皮下注射可以达静脉注射相当的血药浓度。有效性方面,皮下和静脉的总缓解率 (ORR) 、无进展生存期 (PFS) 和总生存期 (OS) 数据相似[2]。
安全性方面,最常见的任何级别不良反应是疲劳、肌肉骨骼疼痛、咳嗽、呼吸困难和食欲下降。
关于阿替利珠单抗
根据FDA获批信息,该药适应证如下,本次的获批主要是制剂类型的不同。
适应证[3]
1. 非小细胞肺癌(NSCLC):
- 单药用于经手术及含铂化疗后的Ⅱ至ⅢA期NSCLC成人患者辅助治疗(肿瘤细胞PD-L1表达≥1%)。
- 单药一线治疗高表达PD-L1、无EGFR或ALK畸变的转移性NSCLC成人患者。
- 与贝伐珠单抗等联合用于无EGFR或ALK畸变的转移性非鳞状NSCLC成人患者一线治疗。
- 单药治疗含铂化疗期间或后进展的转移性NSCLC成人患者(有EGFR或ALK畸变患者应在对应FDA批准疗法进展后使用)。
2. 小细胞肺癌(SCLC):与卡铂和依托泊苷联合用于广泛期SCLC成人患者一线治疗。
3. 肝细胞癌(HCC):与贝伐珠单抗联合用于未接受全身治疗的不可切除或转移性HCC成人患者。
4. 黑色素瘤:与考比替尼和维莫非尼联合用于BRAF V600突变阳性的不可切除或转移性黑色素瘤成人患者。
5. 肺泡软组织肉瘤(ASPS):单药用于2岁及以上不可切除或转移性ASPS成人及儿童患者。
关于Halozyme[4]
Halozyme 是一家生物制药公司,致力于提供颠覆性解决方案,以改善新兴和成熟疗法的患者体验和结果。作为采用专有酶 rHuPH20 的 ENHANZE药物输送技术的创新者,Halozyme 经过商业验证的解决方案用于促进注射药物和液体的皮下输送,目的是通过快速皮下输送和减轻治疗负担来改善患者体验。
Halozyme 已在全球 100 多个市场的 8 种商业化产品中触及超过 800,000名患者的上市后使用,其 ENHANZE技术已授权给领先的制药和生物技术公司,包括罗氏、武田、辉瑞、杨森、艾伯维、礼来等。
参考文献:
1.Halozyme Announces FDA Approval of Roche's Tecentriq Hybreza™ With ENHANZE® for Multiple Types of Cancer
2.FDA Approves Subcutaneous Atezolizumab and Hyaluronidase-tqjs for Use in All Indications of IV Atezolizumab
3.Product information:.TECENTRIQ- atezolizumab injection, solution
4.https://ir.halozyme.com/news/news-details/2024/Halozyme-Announces-FDA-Approval-of-Roches-Tecentriq-Hybreza-With-ENHANZE-for-Multiple-Types-of-Cancer/default.aspx
肺癌是国内第一大癌,这条管线的新药也是百家争鸣,24年8月29日,拜耳又有新布局,其III期SOHO-02研究迎来首位患者。
SOHO-02研究布局于HER2激活突变的晚期非小细胞肺癌(NSCLC)的跑道,旨在评估其新药的疗效和安全性,拜耳对照对比的竞品是帕博利珠单抗和铂类药物。由于研究结果还没有发布,我们先看看这个研究的设计部分。
SOHO-02研究[1]
SOHO-02研究是一项多中心随机对照Ⅲ试验,之所以选择这个赛道,是为了寻找HER2突变型晚期非小细胞肺癌(NSCLC)的更优治疗方法。晚期 NSCLC大家知道,已扩散到附近组织或身体的其他部位,不太能通过目前可用的治疗方法治愈或控制。而HER2 是一种帮助细胞生长和分裂的蛋白质。癌细胞中异常 HER2 的产生,从而导致异常的细胞生长和分裂。
拜耳所研究的治疗药物BAY 2927088 可能可阻断突变的 HER2 蛋白,从而可能阻止 NSCLC 的扩散。那么这个对照试验考察什么结果?
主要结果
研究还是选择了经典的RECIST 1.1 标准下的无进展生存期(PFS),预计时间为两年。次要结果包括OS、ORR等。
临床试验方法
将入组患者分为两组,一组接受BAY2927088 20 mg,每日两次,口服,直至根据 RECIST v1.1 标准出现疾病进展、不可接受的毒性或其他停药标准。
另外一组采用标准治疗法,静脉注射 帕博利珠单抗+顺铂+培美曲塞,每 21 天一个周期,直至根据 RECIST v1.1 标准出现疾病进展、不可接受的毒性或其他停药标准。
关于BAY 2927088
BAY 2927088目前还处于Ⅱ期试验中,因此没有对应药品名,没有适应证等信息。但这个药来头可不小, 源自拜耳与美国麻省理工学院、哈佛大学博德研究所的长期战略研究联盟。且在24年被FDA认定为“突破性疗法”。FDA 的突破性疗法认定旨在加速有望成为治疗严重或危及生命的疾病药物的开发和审查。
突破性疗法认定也是基于 BAY 2927088的 I 期临床,估了该药在 HER2/EGFR 型晚期非小细胞肺癌成年患者中的安全性、药代动力学和疗效。早期临床证据表明,该药有望HER2型突变非小细胞肺癌患者受益[2]。
关于非小细胞肺癌
肺癌是全球癌症相关死亡的主要原因。非小细胞肺癌是最常见的肺癌类型,占病例的85%以上。在 2%-4%的晚期非小细胞肺癌中发现激活型 HER2 突变[2]。
人表皮生长因子受体 2/ERB-B2 受体酪氨酸激酶2(HER2/ERBB2)是 EGFR(表皮生长因子受体)家族中的一种酪氨酸激酶受体,是一个比较火的治疗靶点 。HER2没有已知的可溶性配体,其下游信号传导是通过与其他配体结合的 HER 家族成员二聚化而触发的,这导致下游 PI3K/AKT 和 MEK/ERK 通路的磷酸化和激活。HER2 通路的改变通过增加二聚化和自磷酸化来驱动肿瘤发生,导致细胞生长失控[3]。
关于拜耳
拜耳是一家全球性企业,在医疗保健和农业生命科学领域拥有核心竞争力。其设计产品和服务,旨在帮助应对世界上一些最大的挑战,并满足人类健康和营养的最基本需求。拜耳致力于推动可持续发展,并通过业务产生积极影响。借助科学的力量,拜耳开创了推动生命进步的新可能性。这意味着通过增强日常健康、改进患者护理方法以及寻找更好的方式来滋养世界各地的社区,重新构想如何关爱自己和彼此[4]。
参考文献:
1.A Study to Learn More About How Well BAY 2927088 Works and How Safe it is Compared With Standard Treatment, in Participants Who Have Advanced Non-small Cell Lung Cancer (NSCLC) With Mutations in the Genes of Human Epidermal Growth Factor Receptor 2 (HER2) (SOHO-02)
2.Bayer receives U.S. FDA Breakthrough Therapy designation for BAY 2927088 for non-small cell lung cancer harboring HER2 activating mutations
3.Uy NF, Merkhofer CM, Baik CS. HER2 in Non-Small Cell Lung Cancer: A Review of Emerging Therapies. Cancers (Basel). 2022 Aug 27;14(17):4155. doi: 10.3390/cancers14174155. PMID: 36077691; PMCID: PMC9454740.
24年8月30日,皮尔法伯制药近期官宣:欧盟委员会批准“恩考芬尼与比美替尼联合疗法”扩展适应症,可用于治疗携带 BRAF V600E 突变的晚期非小细胞肺癌(NSCLC)成年患者。
欧盟批准基于II期 PHAROS 试验的结果,今天让我们一起聊聊这个新药组合。
PHAROS研究
PHAROS研究是一项多中心非随机的II期研究,由辉瑞赞助,主要想确定恩考芬尼+比美替尼联合疗法治疗 BRAFV600E 突变的转移性非小细胞肺癌的安全性、有效性和耐受性。
主要结果
为了确定药物的有效性,选择“客观缓解(OR)的参与者百分比”这个指标作为主要结果,怎么理解ORR百分比?它指的是患者用药后实现完全缓解 [CR] 或部分缓解 [PR]占总参与人数的百分比。
这个完全缓解和部分缓解也不是凭空捏造的,完全缓解是所有非淋巴结靶病灶消失(所有靶病灶记录长度为 0 毫米,任何病理淋巴结 [记录为靶病灶] 的短轴必须缩小至 < 10 mm),并且所有非靶病灶完全消失(所有非靶病灶标记为 “消失”,所有淋巴结的大小必须为非病理性 [<10 毫米短轴])。部分缓解是靶病灶直径总和(SOD)减少 30% 或更多,以基线 SOD 为参考[1]。
试验结果不超过36个月,将试验分为两组(详见临床试验方法部分)——初始治疗组和已接受其他治疗组,结果显示,该联合疗法具有显著的临床益处,初治治疗组的ORR为 75%[15% 的完全缓解(CRs)和 59% 的部分缓解(PRs)],已接受其他治疗组为 46%(10% 的 CRs 和 36% 的 PRs)[2]。
安全性方面,最常见的治疗相关不良事件(TRAEs ≥20%)为恶心(50%)、腹泻(43%)、疲劳(32%)和呕吐(29%)。14% 的患者发生了治疗相关的严重不良事件,最常见的是结肠炎(3%)[2]。
临床试验方法
将招募初治患者,或接受过以下治疗的患者:
- 一线标准铂类化疗;
- 一线抗程序性细胞死亡蛋白 1(PD - 1)/ 程序性细胞死亡蛋白配体 1(PD - L1)抑制剂单独治疗或与铂类化疗联合治疗。
接受组合药物治疗的剂量如下:
- 恩考芬尼 450 mg,每日一次(qd)
- 比美替尼 45 mg,每日两次(bid)
28 天(±3 天)为一个治疗周期,持续到患者符合结果部分里介绍的治疗退出标准。
关于恩考芬尼与比美替尼
恩考芬尼是一种强效且高度选择性的 BRAF 抑制剂,比美替尼是一种强效且选择性的 MEK 抑制剂,它们抑制 MAPK 通路中的激酶 在 BRAFV600E 突变的 NSCLC 中该通路被持续激活,从而产生临床相关的抗肿瘤活性。2018 年,欧盟委员会(EC)批准恩考芬尼 + 比美替尼用于治疗携带 BRAFV600 突变的不可切除或转移性黑色素瘤成年患者。2020 年,欧盟委员会批准恩考芬尼与西妥昔单抗联合用于治疗既往接受过系统治疗的携带 BRAFV600E 突变的转移性 CRC 成年患者。
恩考芬尼的用药信息[4]
适应证:
BRAF V600E 或 V600K 突变阳性的不可切除或转移性黑色素瘤、BRAF V600E 突变阳性的转移性结直肠癌(CRC)、BRAF V600E 突变阳性的转移性非小细胞肺癌(NSCLC)。
注意事项
- 新发原发性恶性肿瘤:在使用BRAF抑制剂治疗的患者中观察到新发的皮肤和非皮肤原发性恶性肿瘤,BRAFTOVI也可能导致此类情况发生。
- 心肌病:与比美替尼联合用药,在治疗的患者中出现心肌病,表现为与症状性或无症状性射血分数降低相关的左心室功能障碍。在开始治疗前、开始治疗后一个月以及治疗期间每2-3个月通过超声心动图或MUGA扫描评估射血分数。根据不良反应的严重程度,暂停、减少剂量或永久停药。
- 肝毒性 与比美替尼联合用药,可能会发生肝毒性。用药前、治疗期间每月以及根据临床指征监测肝功能实验室检查。根据不良反应的严重程度,暂停、减少剂量或永久停药。
- 出血:根据不良反应的严重程度,暂停、减少剂量或永久停药。
- 葡萄膜炎 治疗患者有出现葡萄膜炎,包括虹膜炎和虹膜睫状体炎。每次就诊时评估视觉症状。定期进行眼科评估,对于新出现或恶化的视觉障碍,以及跟踪新出现或持续的眼科发现。根据不良反应的严重程度,暂停、减少剂量或永久停药。
比美替尼的用药信息[5]
适应证
- BRAF V600E 或 V600K 突变阳性的不可切除或转移性黑色素瘤、BRAF V600E 突变阳性的转移性非小细胞肺癌(NSCLC)。
注意事项:
- 新发原发性恶性肿瘤:与恩考芬尼联合使用时,可能会发生皮肤和非皮肤的新发原发性恶性肿瘤。在开始治疗前、治疗期间和停药后监测患者是否出现新的恶性肿瘤。
- 心肌病:在开始治疗前、开始治疗后一个月以及治疗期间每2-3个月通过超声心动图或MUGA扫描评估射血分数。治疗期间应密切监测有心血管危险因素的患者。根据不良反应的严重程度,暂停、减少剂量或永久停药。
- 间质性肺病:对于新出现或进展性的无法解释的肺部症状或发现,评估是否可能为间质性肺病(ILD)。根据不良反应的严重程度,暂停、减少剂量或永久停药。
- 肝毒性:可能会发生肝毒性。用药前、治疗期间每月以及根据临床指征监测肝功能实验室检查。根据不良反应的严重程度,暂停、减少剂量或永久停药
- 横纹肌溶解:用药前、治疗期间定期以及根据临床指征监测CPK和肌酐水平。根据不良反应的严重程度,暂停、减少剂量或永久停药。
关于非小细胞肺癌
在非小细胞肺癌(NSCLC)患者中,激活型 BRAF 驱动突变发生在大约3%- 4%的患者。虽然他们在所有 NSCLC患者中只占一小部分,但由于 NSCLC 患病人群较多,如全球每年新增病例超过 200 万例,死亡人数超过 170 万例 ,故BRAF 突变型 NSCLC 患者的数量相对较多[2]。
关于皮尔法伯 [5]
皮尔法伯集团(Pierre Fabre)拥有世界第二大护肤品及化妆品实验室,也是全法第二大私营制药集团。集团业务涵盖处方药、医学护肤品及公共健康三个领域,产品销往130多个国家和地区,于全球45个国家设有子公司。
集团旗下皮尔法伯制药公司致力于植物研究,是植物药研发领域的行业翘楚。大自然就是我们的灵感源泉,为我们提供朝健康和美丽迈进的方向,也是我们业务模式一直以来的核心。我们致力于研究天然物质,为达成皮尔法伯的绿色使命打下坚实的基础。
参考文献:
- An Open-label Study of Encorafenib + Binimetinib in Patients With BRAFV600-mutant Non-small Cell Lung Cancer
- Riely GJ, Ahn MJ, Felip E, Ramalingam SS, Smit EF, Tsao AS, Alcasid A, Usari T, Wissel PS, Wilner KD, Johnson BE. Encorafenib plus binimetinib in patients withBRAFV600-mutant non-small cell lung cancer: phase II PHAROS study design. Future Oncol. 2022 Mar;18(7):781-791. doi: 10.2217/fon-2021-1250. Epub 2021 Dec 17. PMID: 34918546.
- Product information:BRAFTOVI- encorafenib capsule
- Product information:MEKTOVI- binimetinib tablet, film coated
- https://www.pierre-fabre.com/zh-cn/jituanpinpai
- https://mma.prnewswire.com/media/2493339/Pierre_Fabre_Approval.pdf

以下内容来源于PubMed。
High-dose hyperfractionated simultaneous integrated boost radiotherapy versus standard-dose radiotherapy for limited-stage small-cell lung cancer in China: a multicentre, open-label, randomised, phase 3 trial
Abstract
Background: For the past 20 years, twice-daily thoracic radiotherapy with concurrent chemotherapy has been the treatment of choice for limited-stage small-cell lung cancer (LS-SCLC), which has a poor prognosis. We aimed to assess the efficacy and safety of high-dose, accelerated, hyperfractionated, twice-daily thoracic radiotherapy (54 Gy in 30 fractions) versus standard-dose radiotherapy (45 Gy in 30 fractions) as a first-line treatment for LS-SCLC.
Methods: This open-label, randomised, phase 3 trial was performed at 16 public hospitals in China. The key inclusion criteria were patients aged 18-70 years, with histologically or cytologically confirmed LS-SCLC, who had an Eastern Cooperative Oncology Group (ECOG) performance status of 0-1, and who were previously untreated or had received one course of cisplatin or carboplatin and etoposide. Eligible patients were randomly assigned (1:1) to receive volumetric-modulated arc radiotherapy (VMAT) of 45 Gy in 30 fractions to the gross tumour volume or VMAT with a simultaneous integrated boost of 54 Gy in 30 fractions to the gross tumour volume starting 0-42 days after the first chemotherapy course. Both groups received 10 fractions of twice-daily thoracic radiotherapy per week. The planning target volume was 45 Gy in 30 fractions in both groups. Patients with responsive disease received prophylactic cranial radiotherapy (25 Gy in 10 fractions). Randomisation was performed using a centralised interactive web response system, stratified by ECOG performance status, disease stage, previous chemotherapy course, and chemotherapy choice. The primary outcome was overall survival in the intention-to-treat population. Safety was analysed in the as-treated population. This study was registered at ClinicalTrials.gov, NCT03214003.
Findings: From June 30, 2017, to April 6, 2021, 224 patients (102 [46%] females and 122 [54%] males; median age 64 years [IQR 58-68]) were enrolled and randomly assigned to the 54 Gy group (n=108) or 45 Gy (n=116) group. The median follow-up was 46 months (IQR 33-56). The median overall survival was significantly longer in the 54 Gy group (60·7 months [95% CI 49·2-62·0]) than in the 45 Gy group (39·5 months [27·5-51·4]; hazard ratio 0·55 [95% CI 0·37-0·72]; p=0·003). Treatment was tolerable, and the chemotherapy-related and radiotherapy-related toxicities were similar between the groups. The grade 3-4 radiotherapy toxicities were oesophagitis (14 [13%] of 108 patients in the 54 Gy group vs 14 [12%] of 116 patients in the 45 Gy group; p=0·84) and pneumonitis (five [5%] of 108 patients vs seven [6%] of 116 patients; p=0·663). Only one treatment-related death occurred in the 54 Gy group (myocardial infarction). The study was prematurely terminated by an independent data safety monitoring board on April 30, 2021, based on evidence of sufficient clinical benefit.
Interpretation: Compared with standard-dose thoracic radiotherapy (45 Gy), high-dose radiotherapy (54 Gy) improved overall survival without increasing toxicity in a cohort of patients aged 18-70 years with LS-SCLC. Our results support the use of twice-daily accelerated thoracic radiotherapy (54 Gy) with concurrent chemotherapy as an alternative first-line LS-SCLC treatment option.
Funding: Chinese Society of Clinical Oncology-Linghang Cancer Research, the Wu Jieping Medical Foundation, and Clinical Research Fund For Distinguished Young Scholars of Peking University Cancer Hospital and Beijing Municipal Administration of Hospitals Incubating Program.

老赵脑预防放疗出院回家一周了,几乎每天我都打电话给他,给妈妈。今天阿姨去我家了,我给妈妈打视频电话时,阿姨说:“看看你爸爸,走路像个小伙子”镜头转向爸爸,我看到他的背影,笑起来,转头又想哭😭谁能想到看着如此健康的人患恶性程度这么高的病呢?晚上睡觉前又给妈妈打视频,由于放疗,化疗后长出来的头发又掉光了,还是一片片掉的,很滑稽,我笑他,像哪吒。妈妈在旁边接话,你爸说从合肥回来家都瘦了,说我没有女儿照顾的好,等去住院给称称,你再给补回来,我笑说,好。要挂电话前爸爸说他头疼,我一下子心提到嗓子眼,怕脑转移,问清楚之后放下心了,原来是头皮一点点位置疼,摁压疼,不碰没感觉,我说没事放心吧!估计放疗灼伤了,25号入院开始第九次免疫啦!顺便复查,希望爸爸复查顺利,控制长长久久。

小细胞肺癌复发后,再化疗有效吗?
展开更多











