简称:
合肥经开普仁外科医院前身为合肥经开外科医院,2015年原经安做省卫健委批准设置的一所集医疗、科研、预防、保健、康复于一体专科医院。经合肥市卫健委审批为120急救中心经开外科分站,是省异地就医结算、省直职工、合肥市城镇职工、城镇居民、工伤保险、平安产险、人寿财险和大地财险定点医院
-
*芝云回复质量:非常满意服务态度:非常满意回复速度:非常满意functions/format.html图文问诊
-
*明回复质量:非常满意服务态度:非常满意回复速度:非常满意functions/format.html图文问诊
-
*桂菊回复质量:非常满意服务态度:非常满意回复速度:非常满意functions/format.html图文问诊
-
*利娴回复质量:非常满意服务态度:非常满意回复速度:非常满意functions/format.html图文问诊
-
*宽全回复质量:暂无服务态度:暂无回复速度:暂无functions/format.html图文问诊
-
*祥兴回复质量:非常满意服务态度:非常满意回复速度:非常满意functions/format.html图文问诊
-
*军玲回复质量:非常满意服务态度:非常满意回复速度:非常满意functions/format.html图文问诊
-
*正芳回复质量:非常满意服务态度:非常满意回复速度:非常满意functions/format.html图文问诊
-
*圣杰回复质量:非常满意服务态度:非常满意回复速度:非常满意functions/format.html图文问诊
-
*星回复质量:非常满意服务态度:非常满意回复速度:非常满意functions/format.html图文问诊
展开更多
-
 1.成骨不全在目前没有特殊的治疗,对激素及多种药物的疗效未确定。发生骨折时,在治疗上建议骨折时固定的时间应尽量缩短,以免发生广泛骨萎缩,复位时应慎重,尽量减少骨骼畸形。存在多发骨折时建议可用髓内针做内固定。2.成骨不全分为先天性成骨不全以及迟发性成骨不全两类。先天性成骨不全属于严重型,在出生时就有多发骨折,产程中或者子宫内的轻微外伤就可引起骨折,一般肢体较短,有畸形和摩擦音。先天性成骨不全的孩子可出生时死胎,成活者多在婴儿期死亡 如果能存活到青春期,多数都长期卧床。迟发型成骨不全,不如先天性严重,一般出生时正常,轻型发生骨折时间较晚,或者只有巩膜发蓝,而不发生骨折,迟发型患儿的主诉为走路晚,一般都在骨折后才就医。迟发性的成骨不全,青春期后由于性激素的作用,骨折多逐渐减少。在成人由于自我的保护意识增强,骨折的发生率也很低。成骨不全的孩子常体型特殊,骨折后肢体弯曲,可以伴有驼背、脊柱侧弯和后凸,前额增宽,额骨前凸明显,颞骨向两侧突出,枕骨后突,使头颅增大,左右径增宽,前后径变窄,以致面颅不成比例,成三角形。3.四肢长骨的x线检查可有特殊表现,可见多处病理性骨折和大量骨痂形成以及骨骼畸形,皮质薄,松质骨密度减低,骨小梁稀疏或消失。
1.成骨不全在目前没有特殊的治疗,对激素及多种药物的疗效未确定。发生骨折时,在治疗上建议骨折时固定的时间应尽量缩短,以免发生广泛骨萎缩,复位时应慎重,尽量减少骨骼畸形。存在多发骨折时建议可用髓内针做内固定。2.成骨不全分为先天性成骨不全以及迟发性成骨不全两类。先天性成骨不全属于严重型,在出生时就有多发骨折,产程中或者子宫内的轻微外伤就可引起骨折,一般肢体较短,有畸形和摩擦音。先天性成骨不全的孩子可出生时死胎,成活者多在婴儿期死亡 如果能存活到青春期,多数都长期卧床。迟发型成骨不全,不如先天性严重,一般出生时正常,轻型发生骨折时间较晚,或者只有巩膜发蓝,而不发生骨折,迟发型患儿的主诉为走路晚,一般都在骨折后才就医。迟发性的成骨不全,青春期后由于性激素的作用,骨折多逐渐减少。在成人由于自我的保护意识增强,骨折的发生率也很低。成骨不全的孩子常体型特殊,骨折后肢体弯曲,可以伴有驼背、脊柱侧弯和后凸,前额增宽,额骨前凸明显,颞骨向两侧突出,枕骨后突,使头颅增大,左右径增宽,前后径变窄,以致面颅不成比例,成三角形。3.四肢长骨的x线检查可有特殊表现,可见多处病理性骨折和大量骨痂形成以及骨骼畸形,皮质薄,松质骨密度减低,骨小梁稀疏或消失。 -

主动脉夹层(AD)患者,通常需要长期的药物治疗,以减少主动脉壁的压力,防止主动脉扩张或破裂。但近期的研究证据表明肾素-血管紧张素系统与主动脉瘤(AAs)的发生有关。在遗传学研究中,血管紧张素转换酶(ACE)的多态性与AA有关。对于马凡综合征患者,使用ACE抑制剂(ACEI)或血管紧张素受体阻滞剂(ARB)治疗似乎可以减缓主动脉扩张及其并发症的进展。另外的几项动物研究表明,使用ACEI或ARB治疗可以减缓AA的进展并防止其破裂。一项评估厄贝沙坦治疗马凡综合征的随机临床试验表明,ARBs降低了主动脉扩张。
下面就一项回顾性队列研究,对β受体阻滞剂、ACEI或ARB与其他抗高血压药物的相关性,以及它们与AD患者远期结局的关系进行详细分析。
数据来源
研究数据采集时间为2001年1月1日至2013年12月31日,共有6978例首次出现AD的患者符合分析条件。具体流程见(图1)
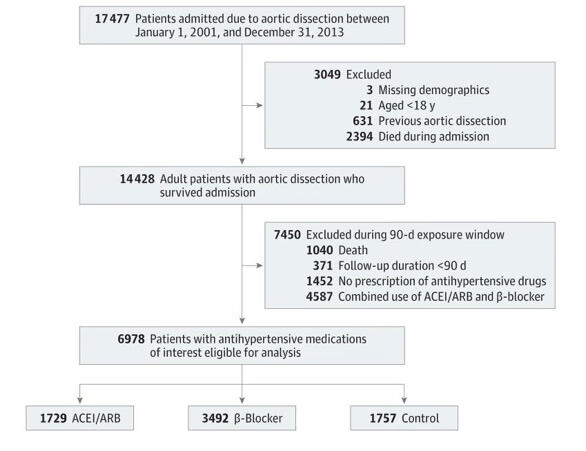
图1(图片来源于参考文献)
分析结果
-
根据使用ACEIs或ARB、β受体阻滞剂或其他抗高血压药物分层的AD患者的临床特征在图2中给出。总共1729名患者使用了ACEIs或ARB,3492名患者使用了β受体阻滞剂类,1757名患者使用了不同的降压药。单因素分析中,3个研究组的大部分临床特征均有显著性差异。年轻患者的β-受体阻滞剂组显著(平均(SD)的年龄,62.1[13.9]年β阻滞剂,68.7[13.5]年acei或arb,和69.9[13.8]年其他降压药),主要由男性患者(2520名患者(72.2%)为β阻滞剂,1161名患者(67.1%)为acei或arb,和1224名患者(69.7%)其他降压药)。药物性高血压患病率在ACEI或ARB组最高(1039例[60.1%]),其次是对照组(896例[51.0%]),而β阻断剂组最低(1577例[45.2%])。接受手术的A型AD患者更有可能使用β受体阻滞剂(1134例[32.5%]),而不是其他降压药(376例[21.4%])和ACEIs或ARBs(309例[17.9%])。调整多倾向评分后,3组间任何临床特征均无显著差异。
-
从2001年到2013年,β阻断剂的使用稳步增加(52%-64.2%;P < 0.001为趋势)。从2001年到2013年,ACEI或ARB联合组的使用也有所增加(39.6%-51.2%;P < 0.001为趋势)。2001年至2013年,仅采用ARB评估法的患者人数稳步上升(18.8%-47.2%;P < 0.001为趋势),而单独使用ACEI评估的患者在这些年间减少了(22.4%5.0%;P < 0.001为趋势)。
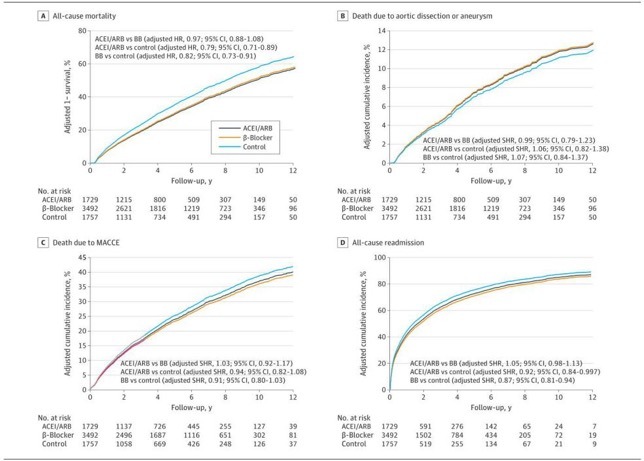
图2(图片来源于参考文献)
-
在ACEI或ARB组和β阻滞剂组之间,有价值的分析指标包括全原因死亡率、AD或AA死亡、重复主动脉手术、MACCE、因任何原因再次住院以及新发生的透析,没有显著差异(图1)。然而,血管紧张素转换酶抑制剂或血管紧张素转换酶抑制剂组(危险比为0.79;95%可信区间为0.71-0.89)和β阻滞剂组(危险比为0.82;95%可信区间为0.73-0.91)均低于对照组(图2A)。虽然AD或AA导致的死亡和综合预后风险在3组之间没有显著差异,但ACEI或ARB组(亚分布HR,0.92;95%CI,0.84-0.997)和β阻滞剂组(亚分布HR,0.87;95%CI,0.81-0.94)的全原因再住院风险显著低于对照组(图2B-D)。不同组之间阴性对照结果(即骨折或恶性肿瘤)的风险没有差异。
-
使用ARB或ACEI的AD患者的基线特征在反转治疗加权概率后,两组之间没有显著差异。图3显示了结果分析的结果。ARB组的死亡率低于ACEI组(HR,0.85;95%CI,0.76-0.95)。ARB组的AD或AA死亡率似乎较低(亚分布HR,0.81;95%CI,0.64-1.03),尽管这一发现没有统计学意义(P=0.09)。此外,两组之间阴性对照结果的风险没有差异(图3)。
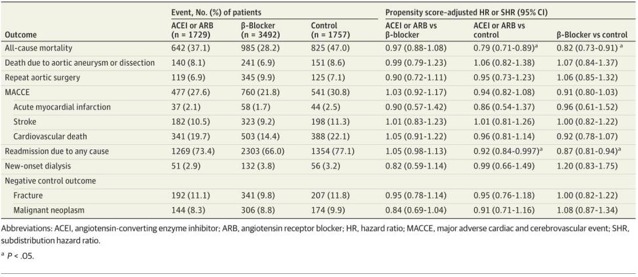
图3(图片来源于参考文献)
-
全因死亡率和由AD或AA引起的死亡的敏感性分析数据是通过使用药物使用作为治疗的时变暴露而获得的。单独使用血管紧张素转换酶抑制剂或血管紧张素转换酶抑制剂或单独使用β阻滞剂与全因死亡率和死于AD或AA的风险较低(但在统计学上不显着)相关。然而,使用血管紧张素转换酶抑制剂或血管紧张素转换酶结合β阻滞剂显著降低了全因死亡率(HR,0.68;95%CI,0.56-0.83)和死于AD或AA的风险(HR,0.64;95%CI,0.47-0.88)。ARB与ACEI的比较结果与初步分析一致,即ARB显著降低全因死亡率(HR,0.72;95%CI,0.63-0.82)和AD或AA死亡(HR,0.71;95%CI,0.58-0.87)。
-
与使用CCB相比,使用血管紧张素转换酶抑制剂或血管紧张素转换酶抑制剂(HR,0.76;95%CI,0.65-0.88)或使用β阻滞剂(HR,0.86;95%CI,0.75-0.995)可显著降低全因死亡的风险。使用血管紧张素转换酶抑制剂或血管紧张素转换酶抑制剂而不是β阻滞剂与较低的AD或AA死亡风险相关(HR,0.67;95%CI,0.48-0.94)。
结果讨论
-
在分析结果中可发现,β阻滞剂和血管紧张素转换酶抑制剂或血管紧张素转换酶抑制剂与其倾向得分匹配的对照组相比,全因死亡率和因任何原因再次住院的风险都较低。ARB治疗组的全因死亡风险低于ACEI治疗组,与ACEI相比,ARB的全因死亡率较低。
-
在肾素-血管紧张素系统中,ACEI具有AT1R和AT2R双重阻断作用,而ARB则具有AT1R阻断作用。只有氯沙坦可以通过AT2Rs持续传递信号来唯一地抑制转化生长因子-β介导的细胞外信号调节激酶的激活。这些结果表明,在通过转化生长因子-β介导的细胞外信号调节激酶的激活来防止主动脉根部扩张方面,氯沙坦可能优于ACEIs。尽管这些研究表明ARB是改善马凡综合征病程的一种有前途的药物,但ACEI或ARB治疗其他动脉瘤的意义尚不清楚。氯沙坦不仅阻断转化生长因子-β信号转导,而且通过阻断AT1R来阻止血管紧张素Ⅱ信号转导,AT1R可能在某些形式的动脉瘤中被激活。合理推测ARB可能对治疗更常见的非遗传性AA有有益效果。
-
β阻滞剂的使用与A型AD手术后存活率的提高有关,而CCBS的使用与B型AD的内科治疗患者存活率的提高有关,血管紧张素转换酶抑制剂的使用与生存无关。然而,CCBS的这种益处还没有在其他研究中显示出来,CCBS不推荐用于遗传性胸主动脉疾病患者。ACEI、ARB或β阻滞剂的使用是与A型和B型AD的全因死亡率降低有关。
-
使用ACEI或ARB和β阻滞剂,而不是使用CCB,与显著降低全因死亡率相关。
总结
与对照组相比,使用β阻滞剂和血管紧张素转换酶抑制剂(ACEI)或血管紧张素转换酶抑制剂(ARB)可降低死亡率和因任何原因再次住院的风险。这些数据提供了证据,表明血管紧张素转换酶抑制剂和血管紧张素转换酶B疗法可能是长期治疗AD的β阻滞剂的替代品。
参考文献:JAMA Network Open.2021;4(3):e210469. doi:10.1001/jamanetworkopen.2021.0469
京东健康互联网医院医学中心
作者简介:陈民,天津医科大学,硕士研究生,硕士研究生期间主攻方向为心内科,对冠心病、心衰、先天性心脏病等常见心内科疾病有深入的研究及丰富的临床经验。
-
-


近年来,越来越多的研究表明,吃坚果有助于降低心脏方面的疾病,尤其是吃树生坚果对心脏有着重要的保护意义。在新英格兰医学杂志中,更是将坚果和种子类食物吃得过少,列为了心血管疾病的十二大元凶之一,认为坚果吃的少对身体的危害甚至高于高胆固醇血症。

坚果的营养价值
坚果是除了植物油之外含有油脂最为丰富的植物类食物,虽然坚果所含的总油脂量很高,但其脂肪组成却没有害处,几乎其总脂肪的一般都为不饱和脂肪,包括单不饱和脂肪酸和多不饱和脂肪酸,而饱和脂肪酸的含量却很低,仅占4%-16%左右。坚果中还含有一定量的植物固醇,以及丰富的优质蛋白以及精氨酸。此外,坚果还是一类含有丰富膳食纤维的食物,每28g坚果就可以为人体提供每日膳食纤维总需要量的5%-10%。坚果中的微量元素也十分丰富,如坚果中不但含有丰富的叶酸、维生素E,它还是高钙镁钾、低钠食物。这种营养构成对人体无疑是非常有益的。

坚果与心血管疾病
相关研究显示,每日吃适量坚果(该量一般被定为28g)可以有效降低人体内的胆固醇含量及血脂的浓度,有利于改善人体血脂的异常。在坚果与心血管疾病的关系研究中,学者对一个包括英国和美国居民在内的6个队列的研究显示,每天摄入28g坚果的人与几乎不吃坚果的人相比,心血管疾病的发病风险降低了28%;而在对包括美国和巴西人群在内的9个队列的另一个研究中则发现,每天坚持吃28g坚果的人比每天几乎不吃坚果的人,心血管疾病的发病风险降低了30%。
此外,在哈佛大学公共卫生学院营养学系的研究者做的研究中发现,每周坚持吃5次树生坚果的人,与每周吃树生坚果不到1次的人相比,其脑血管疾病的患病风险降低了17%,冠心病的患病风险降低了20%,而因脑血管疾病死亡的风险降低了34%,全因死亡的风险则降低了31%。

坚果与其他疾病
除了心脏方面的疾病外,坚持每天吃28g树坚果,每周吃至少5次,对于降低全因死亡率、预防糖尿病人罹患心血管方面的并发症、降低糖尿病患者心血管疾病死亡率、以及降低女性结肠癌的发病风险都有着积极的促进作用。很多人都担心坚果的油脂含量太高,所以多吃会发胖,但实际上,只要严格控制每日饮食总热量的摄入,每天吃28g的树生坚果并不会让人发胖。另外,与树生坚果相比,种子类坚果如花生的摄入,虽然可明显降低全死因死亡率,但其他方面对人体的好处却均不如树生坚果显著,这大概与其所含的营养成分低于树生坚果有关。
-


酱油,是人们在烹调时最常用到的调味品之一,无论炒菜、做汤、又或者是凉拌等,各种菜品都离不开酱油的协同调味作用,可以说酱油是厨师们或者家庭掌勺者们离不开的好帮手,有着重要的增色、添鲜作用。但是,在市面上混的“风生水起”的食品谣言也来了,有传言说吃酱油会让皮肤变黑;有传言说受伤的人吃了酱油连伤口都会长成黑的。听了这些传言之后,酱油如果有眼泪,也应该是泪流满面了吧。好吧,接下来我们就一起重新认识一下感觉自己比窦娥还冤的酱油吧。

酱油的真相
酱油,是我国人民生活中常见的一种传统调味品,颜色呈红褐色,且有特有的酱香,可以增进人们的食欲。酱油是由蛋白质、淀粉原料发酵而成,这些发酵原料一般包括大豆、豆粕、小麦、麸皮等,所以酱油中含有氨基酸、B族维生素、糖、有机酸、醇、酚以及棕红色素等多种物质,无论是炒菜,还是调拌饺子馅儿时放一点,既能起到调色的作用,又能增加香气和鲜味。市面上销售的酱油,除了上述的发酵原料外,还包括食盐,所以酱油中其实是含有一定量隐形盐的,在炒菜或者拌馅时,如果放了酱油可以少放一点食盐。

人的皮肤为什么会变黑
人的皮肤中存在一种黑色素细胞,其中含有的酪氨酸在酪氨酸酶的激活作用下,会产生一种叫“黑色素”的物质,这种黑色素产生的越多,人的皮肤的肤色就会越深,也就是人们常说的“皮肤变黑”。人们皮肤中黑色素量的多少,不但取决于酪氨酸的多少和酪氨酸酶的活性,还与人的遗传基因、太阳光的照射等情况关系密切。

之所以会有“吃酱油会让人的皮肤变黑”的传言,主要是因为酱油中含有丰富的氨基酸,当然也有一定量的酪氨酸。的确,酱油中含有部分酪氨酸,但是仅凭此点就断定“吃酱油会变黑”是不科学的,因为酪氨酸的含量再多,如果酪氨酸酶的活性不够,也不能产生黑色素,而酪氨酸酶的活性绝对不是吃酱油多少能够决定的。再者,含有酪氨酸的食物有很多,它是蛋白质的构成单位之一,所以几乎所有蛋白质食物都有这种氨基酸,最明显的例子就是:牛奶。牛奶在人们的日常饮食中也是非常常见的食物,但也没见有人说喝牛奶会让人变黑,不是吗?

伤口变黑与酱油也没有半毛钱关系
皮肤变黑与酱油没有关系,伤口的颜色变深与酱油其实也没有什么关系。伤口的愈合其实是细胞的增生活动,人体内的细胞是有寿命的,在细胞不断的死亡和分裂增殖的过程中,人体有条不紊的进行着新陈代谢。当身体因出现伤口而改变了那个身体部位原有的状态时,细胞就会不断增生,随之新的组织也会开始不断的分裂、愈合,从而对伤口除做着修复工作,直至其愈合。在伤口愈合的整个过程当中,会出现色素的沉淀,从而使伤口处的颜色表现的比较深沉,与吃不吃酱油真的一点关系都没有。
-

妊娠期间急性肾损伤(AKI)是孕产妇以及胎儿发病和死亡的一个重要原因。AKI与慢性肾病(CKD)和终末期肾病(ESKD)、不良心血管事件的风险增加、住院时间更长相关。早期识别和治疗妊娠期AKI至关重要,是挽救生命的潜在措施。
由于产前诊疗的改善,发达国家妊娠相关AKI的发病率较低,但最近十年来,研究发现,美国的发病率几乎增加了3倍,可能是因为以下原因所致:孕妇年龄较大,合并症较多,AKI检出率较高,妊娠期高血压的发病率增加,肥胖率增加。相比之下,发展中国家近年来妊娠相关AKI总体上有所下降,但发病率仍然高于发达国家。在印度,住院女性中妊娠相关AKI从20世纪80年代的15%下降到21世纪初的1.5%。一项来自中国的研究显示,妊娠相关AKI的发病率下降了0.2%-1.8%。
妊娠期AKI的诊断
临床实践中,妊娠期AKI的诊断并未标准化,因为妊娠相关AKI的定义不一致。而且妊娠期肾小球超滤导致血清肌酐的生理性降低,会影响AKI的检测。 目前妊娠期AKI的诊断尚无明确的标准。应注意妊娠期血清肌酐水平的变化趋势,在特定的临床环境下,即使肌酐的微小变化也能敏感地反映早期肾损伤。例如,在新发高血压的女性患者中,伴随着血清肌酐增加0.3 mg/dL、肝酶增加以及血小板减少,就反映了AKI的可能,需要密切随访肾功能。对AKI的初步评估应包括,全面回顾患者的CKD、慢性高血压、糖尿病、先兆子痫、系统性红斑狼疮和肾小球疾病史。
妊娠剧吐和感染性流产是妊娠早期发生AKI的常见原因。大多数发生在妊娠中期和晚期的AKI,与先兆子痫、HELLP综合征(以溶血、肝酶升高和血小板减少为特点)、AFLP(急性妊娠脂肪肝)、TTP(血栓性血小板减少性紫癜)等血栓性微血管病和胎盘早剥等妊娠并发症有关。非典型溶血尿毒综合征 (aHUS)和非甾体抗炎药(NSAID)引起的肾损伤,是产后AKI的常见原因。
诊断评估应包括尿液分析、尿液显微镜检查、全面代谢检查、凝血检查、适当的血清学检查以及对用药史的全面检查。妊娠期血清补体水平升高是因为肝脏合成增加,这使得狼疮性肾炎的诊断变得复杂。 应当进行肾脏超声检查以排除梗阻性原因所致AKI,例如病理性肾积水。由于妊娠期高凝状态,如怀疑栓塞性疾病, 应行多普勒超声检查。妊娠中晚期AKI的常见原因,如先兆子痫、HELLP综合征、TTP、aHUS、AFLP和狼疮性肾炎,可能会有重叠表现,需要详细评估。
当实验室评估AKI无法下诊断时,可以考虑肾活检,因为明确诊断有助于采取合适的治疗,超过活检带来的风险。肾活检的决策要基于妊娠时期、可用的治疗方案和妊娠活力。妊娠晚期的活检有更高的并发症风险,尤其是妊娠25周后, 建议活检在妊娠早期和中期进行,最好避免在妊娠晚期进行活检,除非AKI治疗可显著改善母婴结局。
根据胎儿成熟度和肾功能下降对胎儿和母亲的影响,在可行的情况下,应 权衡提前分娩的可能性。对于妊娠晚期的孕妇来说,在活检前分娩可能是一个更为谨慎的选择,尤其是在胎儿已经达到存活能力的情况下。应与患者充分讨论并发症和风险,包括大出血需要输血、栓塞、严重产科并发症和胎儿死亡的风险。 AKI发生风险高的女性应在产后进行评估,定期监测血压、肾功能和蛋白尿情况,包括怀孕前患有CKD的女性和怀孕期间出现先兆子痫的女性。
妊娠期AKI的处理
妊娠期AKI的治疗应该由一个多学科团队来进行,由肾脏科医生、产科医生和新生儿医生组成。 治疗妊娠相关AKI的一般措施包括:确定肾损伤的原因,静脉液体复苏,必要时及时开始透析,必要时提前分娩。
静脉液体复苏对于肾前性AKI至关重要,但对于有先兆子痫的女性,因为有发生肺水肿的风险,因此应谨慎进行静脉液体复苏。肾损伤并发症的治疗方法与非妊娠患者相似,例如,对代谢性酸中毒使用补碱疗法,对容量超负荷使用袢利尿剂,对贫血患者输血,对高钾血症使用钾结合剂。
AKI的特异性治疗取决于肾损伤的根本原因。 肾小球肾炎的治疗包括类固醇和免疫抑制剂,当对孕妇使用时,应权衡风险和益处。抗代谢药物,如霉酚酸酯,由于其致畸性,在妊娠期间禁用。妊娠期间或可使用低剂量类固醇,但需监测妊娠期糖尿病的发生。 硫唑嘌呤和钙调神经磷酸酶抑制剂(环孢素和他克莫司)不是致畸药物,是妊娠期常用的免疫抑制药物。妊娠期间需要较高剂量的他克莫司和环孢素来达到治疗目标,因此应经常监测药谷浓度。
重度先兆子痫、HELLP综合征和AFLP的治疗,需要及时分娩。 如果在妊娠34周前分娩,则应给予糖皮质激素以降低新生儿呼吸窘迫综合征的风险。
血栓性微血管病(包括TTP)和非典型HUS的治疗,包括血浆置换和依库珠单抗(用于aHUS)。ADAMTS13缺乏性血栓性微血管病(TMA)的患者,治疗目标是通过血浆置换恢复酶活性,如果血浆置换失败, 利妥昔单抗是一种治疗选择。但妊娠相关TMA应谨慎使用利妥昔单抗,在不到10%的新生儿中观察到了胎儿毒性(血小板减少、嗜中性粒细胞减少和B细胞减少),短期获益还是存在的,目前还没有研究对利妥昔单抗在新生儿中的长期安全性进行评估。
总结
妊娠期AKI与孕产妇死亡率增加以及孕产妇和胎儿不良结局有关。在怀孕期间,应定期监测肾功能,特别是高危女性。妊娠期AKI的诊疗需要一个多学科团队来对孕妇进行管理,以改善产妇和胎儿结局。目前,妊娠期AKI仍然没有得到充分的认识,需要继续探索其长期影响。
参考文献:
Adv Chronic Kidney Dis. 2020;27(6):455-460.
京东健康互联网医院医学中心
作者:杨超,毕业于北京大学医学部,现在北京大学第一医院工作,研究方向为慢性肾脏病。
-

全球范围内,三分之一的女性死亡原因是缺血性心脏病(IHD)。虽然育龄女性IHD的患病率较低,但就目前的趋势而言,如孕妇年龄增加,孕妇糖尿病、肥胖和高血压患病率增加,可能导致了这类群体中冠状动脉疾病的患病率增加。此外,有研究证实,怀孕本身就会比同龄非怀孕女性的急性心肌梗死(AMI)风险更高。心脏病是孕产妇死亡的主要原因,IHD占心脏病病因的五分之一以上。
妊娠期心肌梗死的患病率
据报道, 妊娠期心肌梗死的发病率为6.2/10万妊娠。动脉粥样硬化仍然是妊娠期AMI的最主要原因,其他原因也比非妊娠人群更为常见。孕妇AMI的各种病因患病率如下:冠状动脉粥样硬化伴或不伴冠状动脉内血栓(27%–40%)、自发性冠状动脉夹层 (SCAD,27%–43%)、冠状动脉内血栓不伴动脉粥样硬化(8%–17%),冠状动脉痉挛 (2%)。
对2006-2011年间150例AMI患者的类型和时间进行分析发现,大多数患者表现为ST段抬高型心肌梗死(STEMI,75%),其余患者表现为非ST段抬高型心肌梗死(NSTEMI)。大多数事件发生在妊娠晚期(STEMI,25%;NSTEMI,32%)或产后(STEMI,45%;NSTEMI,55%)。梗死累及左室前壁(69%)、下壁(27%)、侧壁(4%)。
冠状动脉疾病的药物治疗和孕期安全性
大多数用于IHD的药物,不管是治疗AMI或用于心血管疾病的二级预防,可以在怀孕和哺乳期间继续使用,但有一些药物例外。如果有致畸性或其他对胎儿有害的影响,建议停止该药物。此外,可能需要调整药物剂量,因为妊娠期间的血流动力学变化会影响药代动力学。 他汀类药物在孕期和哺乳期禁用,但是这些女性在孕期和产后停药,发生AMI的风险可能会增加。
使用冠状动脉造影的注意事项
对于急性斑块破裂导致的STEMI,建议通过经皮冠状动脉介入治疗(PCI)和支架植入及时进行冠状动脉再灌注。基于妊娠期间事件发生的时间以及出血风险,选择药物洗脱支架(DES)还是裸金属支架(BMS)。DES再狭窄的风险较低;然而,与BMS相比,会需要更长时间的抗血小板药物治疗(12个月vs 1个月)。考虑到BMS可缩短抗凝治疗时间,BMS可能是有优势的,尤其是在分娩期间。
血管造影是妊娠期IHD诊断的金标准。然而,只有60%的AMI女性接受了冠状动脉造影,部分原因是担心会对胎儿产生危险。目前可接受的妊娠期辐射累积剂量为50mGy,一个重要影响因素是妊娠所处时期。在妊娠的头2周,无论辐射剂量多大,都可能导致自发流产。妊娠第3周到第8周,出生缺陷、流产或生长迟缓的风险较低,除非辐射量超过200 mSv。妊娠8至15周,对中枢神经系统(CNS)的风险较高,包括小头畸形和其他CNS畸形,辐射阈值为300 mSv。
重组组织型纤溶酶原激活剂进行溶栓
在无法进行PCI的情况下,必要时可考虑使用组织型纤溶酶原激活剂(TPA)。以前人们认为妊娠期间应禁止溶栓,但新数据表明,妊娠期使用TPA的风险并不高于非妊娠女性。要注意的是,在冠状动脉夹层所致心肌梗死患者中,溶栓可能会加重出血和夹层。
妊娠期自发性冠状动脉夹层
普通人群中,自发性冠状动脉夹层(SCAD)并不是AMI的常见病因; 但妊娠期AMI中 ,SCAD可占到27%-43%。SCAD的典型表现与AMI相似,伴有胸痛、呼吸困难和出汗。SCAD诊断通常比较困难,因为典型患者通常是年轻人,没有其他可识别的心血管危险因素。
基于研究的发现,对于患有纤维肌发育不良(25%–86%)、处于妊娠期(2%–8%)、有结缔组织疾病(1.2%–3%)、全身炎症(<1%–8.9%)、服用外源性激素(10.7%–12.6%)和诱发应激事件的患者,应怀疑SCAD的可能性。超过50%的患者会报告有促发因素,包括分娩、服用外源性激素、高强度运动。妊娠期SCAD的潜在机制尚不完全清楚,可能是妊娠期间动脉壁激素减弱时血液动力学压力增加的结果。
自发性冠状动脉夹层最初的临床表现为心源性休克(2%-5%)、STEMI(26%-87%)、室性心律失常或心源性猝死(3%-11%)。在一项包括168名患者的队列研究中,所有患者都出现了肌钙蛋白I水平升高。患者的左心室射血分数通常保持不变,但超声心动图或早期血管造影可发现左心室壁运动异常。
任何动脉都可能受到影响, 左前降支最常见,可占到32%-46%。与非孕期SCAD的管理类似,建议大多数孕妇采用 保守治疗并住院监测。在一项包括131例SCAD病例的观察性研究中,自发性愈合率为88.5%,35天后,所有患者的血管造影均观察到愈合。在需要做血管造影的病例中,需要注意球囊膨胀或支架扩张所产生的径向力可能导致夹层;在PCI前对SCAD提高警惕是有必要的。
在对孕期自发性冠状动脉夹层 (P-SCAD)与非孕期自发性冠状动脉夹层 (NP-SCAD)的比较中,P-SCAD更多表现为急症,包括STEMI (57% vs 36%),左主血管或多血管SCAD (24% vs 5%),以及左心室功能≤35% (26% vs 10%)。
P-SCAD最常发生在产后第一个月。在2000-2015年进行的一项荟萃分析中,有超过120例发生了妊娠期SCAD,超过87名患者(72.5%)发生在产后第3天至第210天之间。与NP-SCAD相比,P-SCAD患者伴有纤维肌发育不良和冠状动脉外血管异常的可能性更小。
临床诊疗建议
1. 已有IHD的女性应在怀孕前接受全面的心脏评估。
2. 现有的工具如CARPREG Ⅰ、CARPREG Ⅱ、ZAHARA和改良WHO分类,通常可用于先天性心脏病、瓣膜病和心肌病的评估,但在IHD女性的风险评估中作用有限。
3. 从现有趋势来看,如孕妇年龄偏大、合并症患病率增加,可能导致妊娠期IHD的发病率增加。
4. 识别和治疗妊娠期间自发性冠状动脉夹层和冠状动脉痉挛非常重要,因为其临床表现可能不典型。
5. 大多数用于IHD或心血管疾病二级预防的药物可以在怀孕期间继续使用,但某些药物除外。
参考文献:
Cardiol Clin. 2021;39(1):91-108.京东健康互联网医院医学中心
作者:龚志忠,首都医科大学硕士,研究生期间在北京安贞医院主要从事心血管病流行病学研究,已参与发表英文SCI论文2篇,中文核心期刊论文3篇,参与编写出版著作2部。
-
日常病情监测
- 接受期待治疗或甲氨蝶呤药物治疗的患者,应注意定期进行血 HCG 检测和 B 超检查,并监测自身症状进展。若仍有反复阴道滴血或突发急性腹痛、晕倒等,应警惕治疗失败,及时就医。
- 药物注射治疗者,应同时注意监测有无恶心、腹泻、消化不良等副作用,及时反馈。
- 接受手术治疗的患者,需要重点监测手术伤口是否出现红、肿、痛、流脓破溃。1 个月后门诊复查,如有阴道出血、腹痛等不适随诊。
- 进行保守手术有妊娠组织残留风险,故术后应遵医嘱及时复查。
预防
- 科学避孕,建议习惯使用安全套。无避孕措施的不卫生性生活或反复流产,均容易引发输卵管炎、盆腔炎等妇科炎症,从而导致异位妊娠。服用紧急避孕药,避孕失败时可加大异位妊娠风险。而安全套可以预防感染,还能有效避孕。
- 及时治疗妇科疾病,如输卵管炎、盆腔炎、子宫内膜异位症等。
- 注意个人卫生,包括日常卫生和性卫生,每天清洁外阴,换洗内衣裤,限制性伴侣数量。
- 做好孕前检查。
- 保持良好的生活习惯,禁止吸烟、酗酒。
-
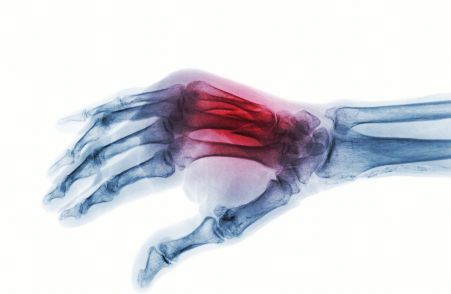
于某,男,42 岁,辽宁海城人事,X 线号 10112640,工人,工作中不慎铁器砸伤,右手拇指疼痛、肿胀、功能障碍两天来就诊。
查体:患者右手拇指近节肿痛、畸形、功能障碍、可触及骨擦感,局部压痛及轴向压痛(+)。
X 线 :右手拇指近节指骨粉碎骨折
诊断:右手拇指近节指骨粉碎骨折
治疗 手法复位,术者一手握其大鱼际,令一手拇示指握其断端,牵引,捺正手法后、触摸掌侧、背侧、尺桡侧第 1 近节指骨生理结构回复,手握绷带卷屈指位胶布牵引固定,外敷绷带加固。复查 X 线片号 10112736,示解剖复位。
-
产前进行乙肝表面抗原(HBsAg)筛查,能识别出感染乙肝病毒(HBV)的孕妇,从而能够进行新生儿免疫预防。但这无法反映出慢性感染所处的阶段、病毒基因型和病毒活性、肝脏炎症或其他并存的肝脏疾病;此外,还可能存在其他病毒和微生物的合并感染,这些因素都会影响妊娠结局。
妊娠并发症可能与母体HBV感染以及突发性肝炎存在相互作用,导致严重和致命性的不良结局。突发肝炎很常见,尤其是在产后,且不可预测,无法用抗病毒治疗来进行预防。目前已有HBsAg血清阳性与妊娠糖尿病、早产、胎儿生长增加和妊娠期高血压疾病之间的关联性证据。 基线期对肝功能以及病毒标志物和病毒活性进行评估,可以识别出真正的高危妊娠,从而能进行密切监测。
妊娠糖尿病(GDM)
一项病例对照研究和一项队列研究均发现,HBsAg血清阳性母亲的GDM风险显著增加。最新的荟萃分析证实, 在HBsAg血清阳性的女性中,GDM的风险增加了47%。这种关联与HBV标志物如HBeAg状态、病毒载量或HBV DNA无关,不过一项泰国研究发现HBeAg血清阳性时GDM风险增加了43.4%。通过普遍筛查诊断出的GDM病例中,有34%和54%会被基于风险因素的筛查方法所漏诊,因此, 对于HBsAg血清阳性的孕妇,应常规进行葡萄糖耐量试验(OGTT)检查。
早产风险
一项中国研究显示,1728名HBsAg血清阳性者和1497名对照者之间的早产率不存在差异(5.4% vs 5.0%),但孕中期的HBV DNA复制量增加,会导致早产风险增加。包含489965名女性的更大型研究发现, HBsAg血清阳性与早产风险增加26%相关。
一些荟萃分析也证实了早产风险的增加,仅HBsAg血清阳性可使早产风险增加16%,HBsAg和HBeAg均阳性可使早产风险增加21%。另一项中国研究显示,肝功能检查异常也是早产的独立风险因素。
产前出血、胎盘早剥和前置胎盘
据报道,仅感染HBV时,产前出血的风险增加2.18倍,合并感染HCV时风险增加2.82倍。最新的荟萃分析中 没有发现HBV感染与胎盘早剥或前置胎盘存在相关性。
妊娠期肝内胆汁淤积症(ICP)
一项包含3329名孕妇的队列研究显示,346名HBV携带者孕妇的ICP风险增加了70%,HBeAg阳性的女性比HBeAg阴性的女性风险更高。HBV感染和ICP有协同作用,两者同时存在时,胎膜早破、羊水胎粪污染和剖宫产的发生率显著升高。
剖宫产
美国的一项研究比较了814名HBV携带者和296218名非携带者,发现前者的剖宫产率减少了31%。一项包含9526名HBsAg血清阳性女性的研究发现, 择期剖宫产的发生率增加,紧急剖宫产的发生率降低。另一项对749名HBV和/或HCV携带者的研究发现,总体剖宫产率增加了50%。一些中国研究中也发现了剖宫产率的增加,剖宫产通常是根据产妇要求或产科医生建议进行,他们可能认为剖宫产可以减少母婴传播。但事实上由于及时的新生儿免疫预防,剖宫产并未影响母婴传播,因此, 用择期剖宫产来预防母婴传播并不合适。
产后出血
一项队列研究发现HBV携带者的产后出血率增加(4.0% vs 2.7%),另一项考察产妇年龄对产后出血影响的研究中也发现产后出血率增加了16%,不过还需要通过更多研究来进行证实。
流产和胎儿畸形
一项研究对513名HBV携带者与20491名对照者进行了比较,发现前者的 流产率增加了71%。接受体外受精(IVF)的HBV携带者女性中,也观察到早期流产和总流产率的增加,这归因于一些胚胎出现HBV感染,有研究发现,来源于HBV感染的母亲或父亲的卵裂胚胎中,分别有13.2%和5.6%检测到了HBV mRNA片段,这或许也解释了先天畸形率的增加。
低出生体重和小于胎龄儿
有报道称HBsAg血清阳性与低出生体重和小于胎龄儿有关;也有研究显示并未导致低出生体重新生儿的增加,但HBeAg血清阳性与低出生体重婴儿增加25.8%相关。然而,低出生体重对胎儿生长受限的影响还没有得到研究。
大于胎龄儿和巨大儿
伊朗一项病例对照研究发现,HBsAg血清阳性孕妇, 巨大儿的发生率增加了2.5倍。另一项队列研究也证实了相关性,即巨大儿和大于胎龄儿分别增加了15%和11%,低出生体重减少了14%。中国研究也发现会导致平均出生体重更高,巨大儿增加了68%,大于胎龄儿显著增加。另一个危险因素可能是母体ALT水平升高,研究显示,分娩大于胎龄儿的非GDM女性,平均ALT水平较高(>26 lU/L),可导致大于胎龄儿风险增加4倍。
胎儿窘迫和胎儿宫内死亡
已有报道称,HBsAg血清阳性孕妇,会导致胎儿窘迫发生风险增加。包含18项研究7600名HBV携带者的荟萃分析表明,胎儿窒息率增加了80%,此外,围产期死亡率、胎儿宫内死亡和死胎率均有所增加,因此对这类患者 应周密进行胎儿监测。
母乳喂养
尽管为了减少母婴传播,人们常常避免母乳喂养,但实际上并未发现母乳喂养会增加母婴传播率,这在一项包含751名母乳喂养和873名非母乳喂养婴儿的荟萃分析中得到了证实,该研究评估了6-12个月婴儿外周血HBsAg或HBvDNA阳性情况,以及6-12个月时的乙肝表面抗体阳性的情况。 在进行充分的新生儿免疫预防的情况下,允许进行母乳喂养。
总结
母体HBsAg血清阳性对母体健康和妊娠结局存在影响,后者还受到其他母体和病毒因素的影响。通过肝功能检查、HBeAg状态和HBV DNA水平进行初步评估,必要时进行肝脏超声检查,可以将真正的高危妊娠患者识别出来,从而可以进行密切监测和适当的治疗。
参考文献:
Best Pract Res Clin Obstet Gynaecol. 2020;68:66-77.
京东健康互联网医院医学中心
作者:卢秀玲,毕业自北京大学公共卫生学院,曾在某知名医学网站担任医学总编辑,负责过肿瘤、心血管、内分泌等多个频道的内容产出。
展开更多



















