
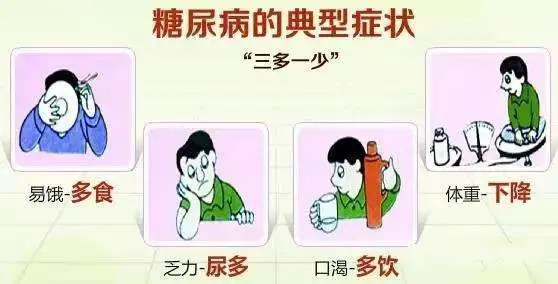
四岁baby得了糖尿病。
5年前主任管的病房里来了一个4岁的聪明伶俐活泼可爱的初发的一型糖尿病小朋友。父母很着急,打听到国外一家医院治疗1型糖尿病,给主任说想到这家医院就诊。
主任说国内国外治疗糖尿病的方案是同步的,建议可以通过远程咨询一下。孩子父母咨询国外医院,回答:
1首先确定孩子是1型糖尿病还是2型糖尿病需要查一下原因,查胰岛功能;
2儿童大部分是1型糖尿病,1型糖尿病是胰岛素的绝对缺乏,需要补充生理需要的胰岛素,同时配合饮食及运动;
3胰岛素的给药方式1皮下注射胰岛素注射笔;2无针注射器注射;3胰岛素泵注射。前两种儿童不方便,建议应用胰岛素泵。

内分泌主任医师解读:
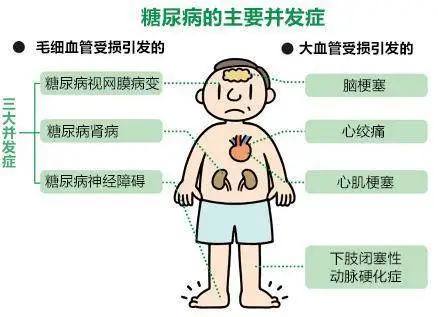
《糖尿病的发病因素有那些?》
糖尿病的发病因素包括遗传因素、环境因素和生活方式因素。具体来说,可能的发病因素包括:
1.遗传因素:有家族史的人更容易患上糖尿病。
2.自身免疫反应:1型糖尿病是自身免疫疾病,免疫系统攻击胰岛素生产的细胞。
3.胰岛素抵抗:2型糖尿病患者通常会有胰岛素抵抗,即身体对胰岛素的反应减弱。
4.胰岛素分泌不足:胰腺分泌的胰岛素量不足以维持正常的血糖水平。
5.肥胖:肥胖是2型糖尿病最主要的危险因素之一。
6.不良的饮食习惯:高糖分和高脂肪的饮食可能增加患糖尿病的风险。
7.缺乏运动:缺乏运动或久坐不动的生活方式也会增加患糖尿病的风险。
8.高血压和高胆固醇:这些因素也与糖尿病的发病有关。
综合来看,遗传因素、生活方式以及环境因素都在一定程度上影响着糖尿病的发病。
《糖尿病的诊断》
糖尿病的诊断主要基于测量血糖水平。以下是常用的诊断标准和分析:
1.空腹血糖(Fasting Blood Glucose,FBG):通常在早上空腹8小时以上后进行检测。诊断糖尿病的标准是空腹血糖≥7.0mmol/L(126mg/dL)。
2.餐后血糖(Postprandial Blood Glucose):在进餐后1-2小时内测量血糖。餐后2小时血糖≥11.1mmol/L(200mg/dL)可用于糖尿病的诊断。
3.随机血糖(Random Blood Glucose):在任何时间测量的血糖水平,随机血糖≥11.1mmol/L(200mg/dL),伴有糖尿病症状,如多尿、口渴、体重减轻等,也可用于诊断。
4.糖化血红蛋白(HbA1c):反映过去2-3个月内的平均血糖水平。诊断糖尿病的标准是HbA1c≥6.5%。
5.口服葡萄糖耐量试验(Oral Glucose Tolerance Test,OGTT):在空腹后饮用含75g葡萄糖的溶液,然后在2小时后测量血糖。餐后2小时血糖≥11.1mmol/L(200mg/dL)可诊断糖尿病。
除了这些标准外,医生还会考虑患者的临床症状、家族病史等因素进行综合分析,以确诊糖尿病。诊断糖尿病后,医生还会评估病情的严重程度,并制定相应的治疗计划。
《糖尿病的分型》
糖尿病主要分为两种类型:1型糖尿病和2型糖尿病。
1型糖尿病:也称为胰岛素依赖型糖尿病或青少年糖尿病。这种类型的糖尿病通常在年轻人中发作,由免疫系统攻击胰岛素生成细胞,导致胰岛素的严重缺乏。患者需要定期注射胰岛素来维持正常的血糖水平。
2型糖尿病:也称为非胰岛素依赖型糖尿病或成人型糖尿病。这种类型的糖尿病通常在成年人中更为常见,特征是胰岛素抵抗和胰岛素分泌不足。初期可以通过饮食管理、体育锻炼和口服降糖药物控制血糖,但在疾病进展后可能需要使用胰岛素治疗。
除了1型和2型糖尿病外,还有一些其他罕见的糖尿病类型,如妊娠糖尿病(发生在怀孕期间)、特发性糖尿病(原因不明的糖尿病)、遗传性糖尿病等。这些类型的糖尿病在临床上相对较少见。


约占所有糖尿病病例的5-10%,在所有年龄段都会发生,在青春期和成年早期发病率达到高峰。全球1型糖尿病的患病率为5.9/1万,而在过去50年来,发病率迅速上升,目前估计发病率为15/10万/年。
近日,美国糖尿病协会(ADA)和欧洲糖尿病研究协会(EASD)联合发布了一份≥18岁成人1型糖尿病管理的共识报告,下文主要总结了胰岛素治疗和辅助治疗的共识建议。
胰岛素治疗策略
治疗方案的选择
大多数1型糖尿病患者应使用尽可能达到模拟生理学胰岛素分泌的方案。 好的策略是皮下基础胰岛素类似物和餐时速效或超速效胰岛素类似物的每日多次胰岛素注射治疗(MDI),或通过泵持续皮下输注速效胰岛素类似物,将持续基础胰岛素与人工餐时注射相结合。
第一代基础胰岛素类似物和中效胰岛素(NPH)通常每天给药一次,如果每天给药两次,可能获得更大的灵活性和更好的基础胰岛素需求覆盖。试验表明,新型基础胰岛素类似物可能比第一代基础胰岛素类似物和 NPH 胰岛素引起的低血糖事件更少,而速效类似物比短效(普通)人胰岛素能实现更好的餐时覆盖和更少的餐后低血糖发生。 胰岛素类似物是胰岛素方案的首选。超速效胰岛素类似物的起效时间和作用峰值比速效类似物稍早。这些胰岛素可以减少餐后高血糖,但没有证据表明它们比速效类似物能更大程度地减少HbA1c或低血糖事件。
给药方式
胰岛素的给药方式有多种,对设备的选择应该是个性化的。 混合闭环胰岛素泵系统是将1型糖尿病患者的血糖维持在正常范围内的有效手段。MDI可以使用药瓶和胰岛素注射器或胰岛素笔,后者在剂量方面提供了更多的便利,但成本可能更高。
短至4mm的针头,以90°角注射,对大多数成年人来说,肌肉内注射的风险很小;使用较长的针头会增加肌内注射的风险。MDI方案可以通过新兴技术得到加强,如剂量计算器和记忆型笔,可以记录胰岛素的剂量。
目前一些研究组正在进行临床试验评估完全闭环的自动胰岛素输送系统,预计其中一些将在未来几年内获得监管部门的批准。
不良反应
与胰岛素治疗有关的主要不良反应是 低血糖。胰岛素治疗的安全性和有效性与糖尿病患者的血糖监测和胰岛素剂量的调整密切相关。因此,胰岛素剂量管理的教育是该疗法的一个重要组成部分,无论是在胰岛素治疗开始时还是在随访期间。这种教育包括在出现高血糖或低血糖情况下的救援策略,包括测量尿液或血液中的酮体。
其他给药途径
近一个世纪以来,皮下胰岛素一直是主要的给药途径,但这种模式并不能很好地模仿生理性胰岛素分泌。健康的β细胞会在葡萄糖摄入开始时向门静脉循环分泌胰岛素,大约70%的胰岛素会被肝脏清除而不进入系统循环,而皮下胰岛素进入系统循环则有一定的延迟,而且清除速度相对较慢。与皮下快速作用的胰岛素类似物相比,吸入式胰岛素起效非常快,持续时间短。 吸入式胰岛素能很好地改善早期的餐后高血糖,但其作用时间短,对后期餐后高血糖的控制较差。此外,吸入式胰岛素可引起咳嗽或咽喉痛,由于可能对肺功能产生影响, 必须定期进行肺功能测定来监测治疗。
辅助治疗方案
二甲双胍
二甲双胍在许多小型试验中对1型糖尿病患者进行了评估,希望其胰岛素敏感特性能够改善血糖管理和/或降低心血管风险。迄今为止最大的研究评估了428名1型糖尿病患者使用二甲双胍的疗效,每天两次,每次1g,治疗3年,主要终点是平均颈动脉内膜厚度的变化,这是心血管疾病风险的标志。研究结果发现,两组的主要终点没有差异,对HbA1c的影响很小且不持续,对体重的影响很小,每日胰岛素总剂量没有变化。
普兰林肽
普兰林肽是被美国食品和药物管理局(FDA)批准的1型糖尿病的辅助治疗方法。餐前注射可抑制胰高血糖素的分泌,延迟胃排空并促进饱腹感。临床试验显示,可降低HbA1c(0.3-0.4%),适度降低体重(约1kg)。由于其不良反应和需要额外的注射,普兰林肽的临床应用受到限制。目前正在开发该类药物与胰岛素的共同制剂,以及在胰岛素泵或人工胰腺系统中使用普兰林肽的可能性。
胰高血糖素样肽-1受体激动剂
胰高血糖素样肽-1受体激动剂(GLP-1 RA)已在1型糖尿病患者中探索了两种适应症,第一种旨在改善β细胞衰退,目前正在进行相关试验。在一项针对308名最近被诊断为1型糖尿病患者的研究中,利拉鲁肽与抗IL-21联合使用时,可保持β细胞功能。
第二个适应症是作为已确诊的1型糖尿病的辅助治疗,通过阻断胰高血糖素的分泌,减少胃排空,促进饱腹感和体重减轻。在1型糖尿病患者中进行的最大临床试验使用的是利拉鲁肽,结果显示,每日剂量为1.8mg时,可促进HbA1c下降(0.2-0.4%),体重下降(约5kg),胰岛素使用剂量减少。然而,低血糖症和酮症发生率也有所上升。
在2型糖尿病患者中进行的试验显示,一些GLP-1 RA可以减少心血管事件的发生;在1型糖尿病患者中是否也能观察到这些益处尚不清楚。GLP-1 RA已被批准用于肥胖的治疗,但还不包括1型糖尿病患者。基于对其他患者的临床试验结果,这些药物可能对合并肥胖的1型糖尿病患者也有一定作用。
SGLT抑制剂
一些针对1型糖尿病患者的III期研究中,使用SGLT-1或SGLT-1/2抑制剂可以降低HbA1c,改善葡萄糖目标范围内时间(TIR),减轻体重和改善血压。考虑到糖尿病酮症酸中毒(DKA)发生风险的增加,FDA尚未批准其用于1型糖尿病,欧洲药品管理局批准低剂量达格列净(5mg)和索格列净(200mg)用于BMI≥27kg/m2的患者。尚没有明确策略可以降低DKA的风险,一份关于SGLT2抑制剂和DKA的共识声明建议谨慎挑选患者,适当调整胰岛素剂量,从低剂量的SGLT2抑制剂开始,定期测量酮体并及时处理升高情况,作为预防DKA的合理预防措施。
SGLT抑制剂治疗2型糖尿病患者时,主要由于充血性心力衰竭的减少而改善心血管预后,并改善肾脏预后,这些发现是否能外推至1型糖尿病患者,相关证据有限。然而,越来越多关于SGLT2抑制剂的数据显示,非糖尿病患者也有肾脏和心力衰竭获益,这表明有这些合并症的1型糖尿病患者也可能获益。
参考文献:
Diabetes Care. 2021 Sep 30;dci210043. doi: 10.2337/dci21-0043.

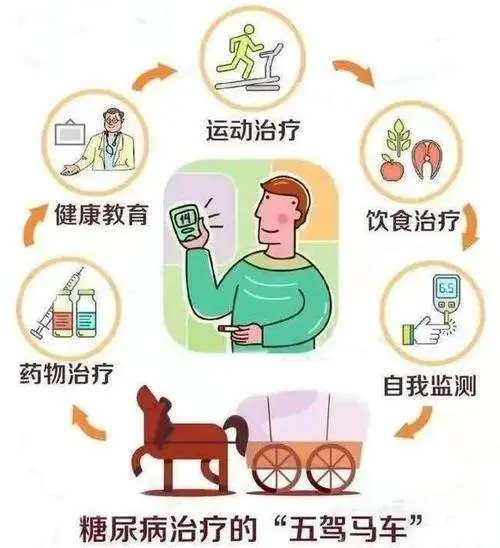
导语:医学营养治疗(MNT),俗称饮食治疗,是糖尿病治疗的基础,也是最难坚持的治疗,应严格和长期执行。

1 型糖尿病患者在合适的总热量,食物成分,规律的餐饮等要求的基础上,配合胰岛素治疗,有利于控制高血糖和防止低血糖。
2型糖尿病患者,尤其是超重或者肥胖者,MNT有利于减轻体重,改善高血糖,脂代谢紊乱,高血压和胰岛素抵抗,减少降糖药物的用量;消瘦患者有利于适当增加体重。
MNT实际是依据身体的健康需求制定的平衡膳食,即各种营养成分摄入都应该合理;同时尽量考虑患者的生活和饮食习惯;相同类别的食物替换时应等热量进行交换。
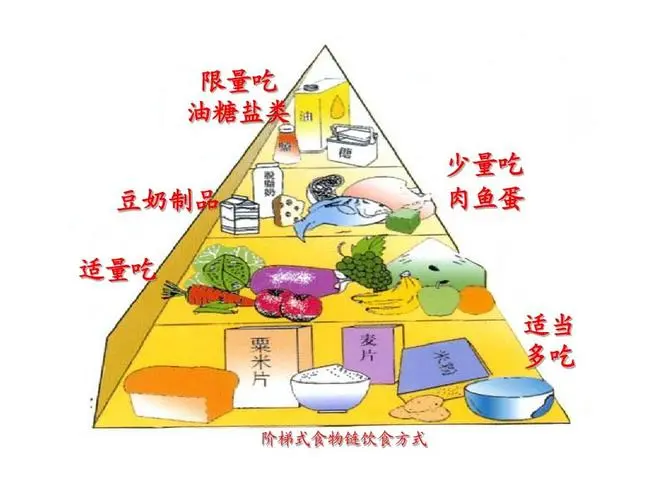
(1) 制定每日总热量:
①首先按性别,年龄和身高查表或计算理想体重,理想体重(㎏)=身高(cm)-105;然后根据理想体重和工作性质,参考原来的生活习惯,计算每日所需要的总热量。
②成人卧床休息状态每日每千克理想体重给予热量105~126kJ,轻体力劳动126~146kJ,中度体力劳动146~167kJ,重体力劳动167kJ以上。
③青少年,孕妇,哺乳,营养不良和消瘦及伴有消耗性疾病时应酌情增加,肥胖者酌减,使体重逐浙控制在理想体重的±5%范围内。

(2)营养素的热量分配:
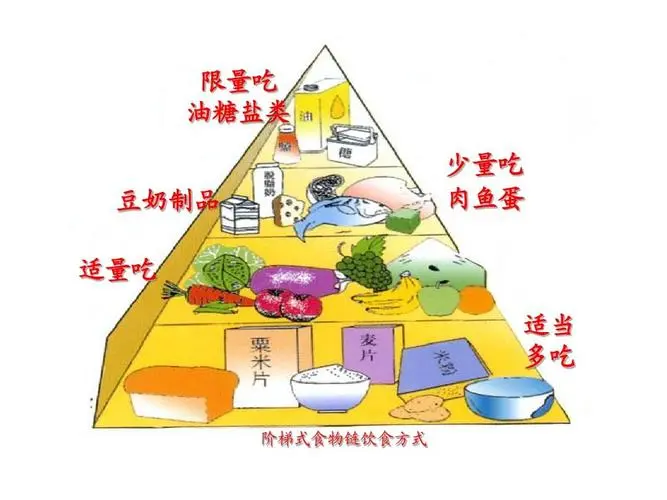
①糖类摄入量道常应占总热量的50%~60%,提倡食用粗制米,面和一定量杂粮,严格限制或避免蔗糖,葡萄糖,蜜糖及其制品(各种糖果,甜糕占,冰淇淋及含糖软饮料等)。
②脂肪的摄入量要严格限制在总热量的20%~30内,其中饱和脂肪酸<10%,单不饱和脂肪酸应尽量达到10%~15%,其余由多不饱和脂肪酸补充。
③限制食物的脂肪量,少食动物脂肪,尽量用植物油代替。
④一般糖尿病患者(无肾病及特殊需要者)每日蛋白质的摄入量应占热量的15%~20%(每日每千克理想体重0.8~1.2g),其中动物蛋白占1/3。
⑤临床糖尿病肾病(大量蛋白尿)者应该减少蛋白质的摄入量(每日每千克理想体重0.8g以下)。
⑥生长发育期的青少年,妊娠或哺乳,营养不良和伴消耗疾病者的蛋白质摄入量可适当增加。

(3)制定食谱:
①每日总热量及营养素组成确定后,根据各种食物的产热量确定食谱。
②每克糖类和蛋白质产热16.8kJ,每克脂肪产热37.8kJ。
③根据生活习惯,病情和药物治疗的需要,可按每日三餐分配为1/5,2/5,2/5或者1/3,1/3,1/3;也可以按4餐分配为1/7,2/7,2/7,2/7。

(4)特殊需要与特殊要求:
①营养素:健康状况良好且膳食多样化的糖尿病患者很少发生维生素与矿物质缺乏。下列情况应予适量补充:
A 成人每日摄入总热量<5040kJ易发生叶酸缺乏;
B 素食者常缺乏维生素B12,钙,铁,锌和核黄酸;
C 血糖控制不佳者易发生水溶性维生素及矿物质的过量丢失;
D 妊娠或哺乳期对铁,锌,钙和叶酸的需求量增加;
E 药物利尿和慢性肾病可以致镁缺乏。
②食物纤维:食物粗纤维不被小肠消化吸收但能满足饱感,有助于减食减重;能延缓糖类和脂肪的吸收,可溶性食物纤维(谷物,麦片,豆类中含量较多)能吸附肠道胆固醇,延缓糖类吸收,有助于降低血糖和血胆固醇。
③食盐和饮酒:一般每日的食盐摄入量不应超过6g,伴肾病或高血压者应<3g。糖尿病患者可适量饮酒,一般不超过1~2份标准量/日(一份标准量的啤酒285ml,清谈啤酒375ml,红酒100ml,白酒30m1,各约含乙醇10g)。禁忌大量饮酒,因可诱发酮症酸中毒和低血糖症。
在实施过程中,应该根据实际效果和病情变化作必要的饮食调整。

导语:1型糖尿病的自身免疫因素包括体液免疫(自身抗体)和细胞免疫两个方面,但是两者之间又有密切联系。

(1)体液免疫(自身抗体):
约90%新发病的1型糖尿病患者循环血中存在多种抗胰岛B细胞自身抗体。
①目前至少发现了十种,其中研究得较多的是胰岛细胞自身抗体(ICA),胰岛素自身抗体(IAA),谷氨酸脱羧酶自身抗体(IA~2和IA~2B)和锌转运体8自身抗体(ZnT8A)。
②这些抗体均是胰岛B细胞自身免疫损伤的标志物,在糖尿病发病前,某些抗体已经存在于血清中,因而对1型糖尿病的预测有一定意义。
③ICA是胰岛四种细胞共有的抗胞浆组分抗体;GADA和IAA则相对独立,但IAA与外源性胰岛素引起的抗体相同。

(2)细胞免疫:
①细胞免疫在1型糖尿病发病中的作用比体液免疫更重要。
②新发病的1型糖尿病患者在胰岛炎症浸润细胞和B细胞表面可观察到HLA~DR抗原的异常表达和(或)IL~2受体与胰岛细胞表面HLA~1类抗原的过度表达,而外周血的CD4+/CD8+比例,以及IL~1,TNF~∝,INFr水平升高。
胰岛B细胞破坏可以分为两期:
①启动期:
环境因素在IL~1,TNF~∝和IFN~r等免疫因子的介导下,启动胰岛B细胞损伤;
②持续(扩展)期:
若胰岛B细胞表面存在1型糖尿病的抵抗基因,B细胞就不易成为抗原呈递细胞;相反,若存在易感基因,B细胞就很可能成为抗原呈递细胞,并将B细胞损伤后释放的抗原直接(或经巨噬细胞摄取和处理后)呈递给激活了的T淋巴细胞。活化的T细胞大量增殖,分化成细胞毒性T细胞并释放多种细胞因子;其中IL~2可刺激B淋巴细胞产生特异性抗体,IFN~r则激活自然杀伤细胞。在细胞介导的免疫应答进程中,胰岛B细胞作为自身抗原,导致选择性B细胞损伤,并形成恶性循环;当80%~90%的B细胞被破坏时,出现临床1型糖尿病的表现。
目前认为,1型糖尿病是一种由淋巴细胞介导的,以免疫性胰岛炎和选择性胰岛B细胞损伤为特征的自身免疫性疾病,特异性抗原,组织相容性抗原和T淋巴细胞受体构成三元复合体,共同参与免疫反应,以特异性免疫识别为条件,激活T淋巴细胞,启动胰岛B细胞的损伤过程。


导语:与1型糖尿病发病有关的环境因素主要有病毒感染,致糖尿病化学物质及饮食因素等,环境因素以病毒感染最为重要。
 (1)病毒感染:
(1)病毒感染:
已经发現腮腺炎病毒,柯萨奇B4病毒,风疹病毒,巨细胞病毒,脑~心肌炎病毒及肝炎病毒等与1型糖尿病的发病有关。其发病机制可能是:
①病毒直接破坏胰岛B细胞,并在病毒损伤胰岛B细胞后激发自身免疫反应,后者进一步损伤B细胞;
②病毒作用于免疫系统,诱发自身免疫反应。
在这些发病机制中,可能都有遗传因素参与,使胰岛素B细胞或免疫系统易受病毒侵袭,或使免疫系统对病毒感染产生异常应答反应。病毒感染诱发自身免疫反应。的机制可能与病毒抗原和宿主抗原决定簇的结构存在相同或相似序列有关。

(2)致糖尿病化学物质:
①对胰岛B细胞有毒性作用的化学物质或药物(如Vacor,四氧嘧啶,链脲佐菌素,喷他咪等)作用于胰岛B细胞,导致B细胞破坏。
②如B细胞表面是 I 型糖尿病的HLA~DQ易感基因,B细胞即作为抗原呈递细胞而诱发自身免疫反应,导致选择性胰岛B细胞损伤,并引发糖尿病。
(3)饮食因素:
①有报道认为,牛奶喂养的婴儿发生1型糖尿病的风险高,可能是牛奶与胰岛B细胞表面的某些抗原相似所致。
②‘分子模拟机制’认为,当抗原决定簇相似而又不完全相同时,能诱发交叉免疫反应,破坏免疫耐受性,激发自身免疫反应,甚至产生免疫性病变。
③牛奶蛋白只对携带HLA DQ/DR易感基因的个体敏感,引发的自身免疫反应使胰岛B细胞受损,进而导致1型糖尿病。

导语:糖尿病的病因和发病机制十分复杂,不同类型糖尿病的病因和发病机制有明显的差异,而大部分发病机制又基本相同。

(一)1型糖尿病
绝大多数为自身免疫性1型糖尿病,病因和发病机制尚未完全闸明,目前认为与遗传因素,环境因素及自身免疫因素均有关。
1 遗传因素
遗传在1型糖尿病的发病中有一定作用。对1型糖尿病同卵双胎长期追踪的结果表明,发生糖尿病的一致率可达50%;然后从父母到子女的垂直传递率却很低,如双亲中一人患1型糖尿病,其子女患病的风险率仅为2%~5%。
遗传学研究显示,1型糖尿病是多基因,多因素共同作用的结果。現已发现,与1型糖尿病发病相关的基因位点至少有17个,分别定位在不同的染色体。
①目前认为,人组织相容性抗原(HLA)基因(即1型糖尿病 I 基因,定位于染色体6p21)是主效基因,其余皆为次效基因。
②90%~95%的1型糖尿病患者携带HLA~DR3,~DR4或~DR3/~DR4抗原,而在正常人中仅40%~50%,这提示HLA~DR3,~DR4是1型糖尿病发生的遗传背景。
③而在多数人群,与1型糖尿病相关性最强的HLA等位基因是DQB1*0302和(或)DQB1*0201。
④因此目前认为HLA~DQ和HLA~DR是1型糖尿病的致病等位基因。
展开更多











 罗金泉中西医结合诊所
罗金泉中西医结合诊所
 华中科技大学同济医学院生殖医学中心
华中科技大学同济医学院生殖医学中心
 天津市安定医院
天津市安定医院
 江山市人民医院
江山市人民医院
 银川京东互联网医院
银川京东互联网医院
 浙江省武义县第一人民医院
浙江省武义县第一人民医院
 定边县中医院
定边县中医院
 北京弘医堂中医医院
北京弘医堂中医医院
 武汉市精神卫生中心
武汉市精神卫生中心
 武汉市武昌区中南路街第一社区卫生服务中心
武汉市武昌区中南路街第一社区卫生服务中心















