科普文章

看看你有没有中招!

一台高难度的乳腺癌二期DIEP乳房重建患者术后恢复顺利,患肢水肿也好转了

乳腺Paget病

双侧乳腺高度怀疑癌症的患者应该怎么办?
新手宝爸宝妈一定要知道的(千万不要让老一辈的无知毁了宝宝)婴儿乳房肿胀可能是正常现象,也可能是由于过敏外伤急性乳腺炎乳腺增生症等原因引起的。1正常现象婴儿在出生后,体内的激素水平会发生变化,此时可能会导致乳房出现肿胀充血等症状,一般属于正常的生理现象,不需要特殊治疗,通常在一段时间后可自行缓解。2过敏如果婴儿属于过敏体质,在使用了某些沐浴露润肤乳等,可能会导致婴儿出现过敏反应,进而引起乳房肿胀皮肤瘙痒等不适症状。建议家长及时更换婴儿的沐浴露,必要时也可遵医嘱使用炉甘石洗剂等药物治疗。3外伤如果婴儿乳房受到外力撞击,可能会导致局部软组织损伤,从而引起乳房肿胀疼痛等不适症状。如果症状较轻,一般不需要特殊治疗,通常在休息一段时间后,症状可逐渐缓解。如果症状较严重,可以在医生指导下使用布洛芬颗粒对乙酰氨基酚颗粒等药物缓解疼痛。4急性乳腺炎急性乳腺炎是指伴或不伴微生物感染的乳腺组织炎症,可能与乳汁淤积细菌感染等因素有关,患者可能会出现乳房肿胀乳房疼痛等症状。建议患者可以在医生指导下使用阿莫西林胶囊头孢克肟胶囊等药物进行抗感染治疗。5乳腺增生症乳腺增生症是一种常见的良性乳腺疾

经超声检查,该犬的乳腺肿瘤虽然呈浸润性生长,但还未发生淋巴转移,应尽快进行乳腺全切除和子宫卵巢摘除,避免癌细胞扩散转移。
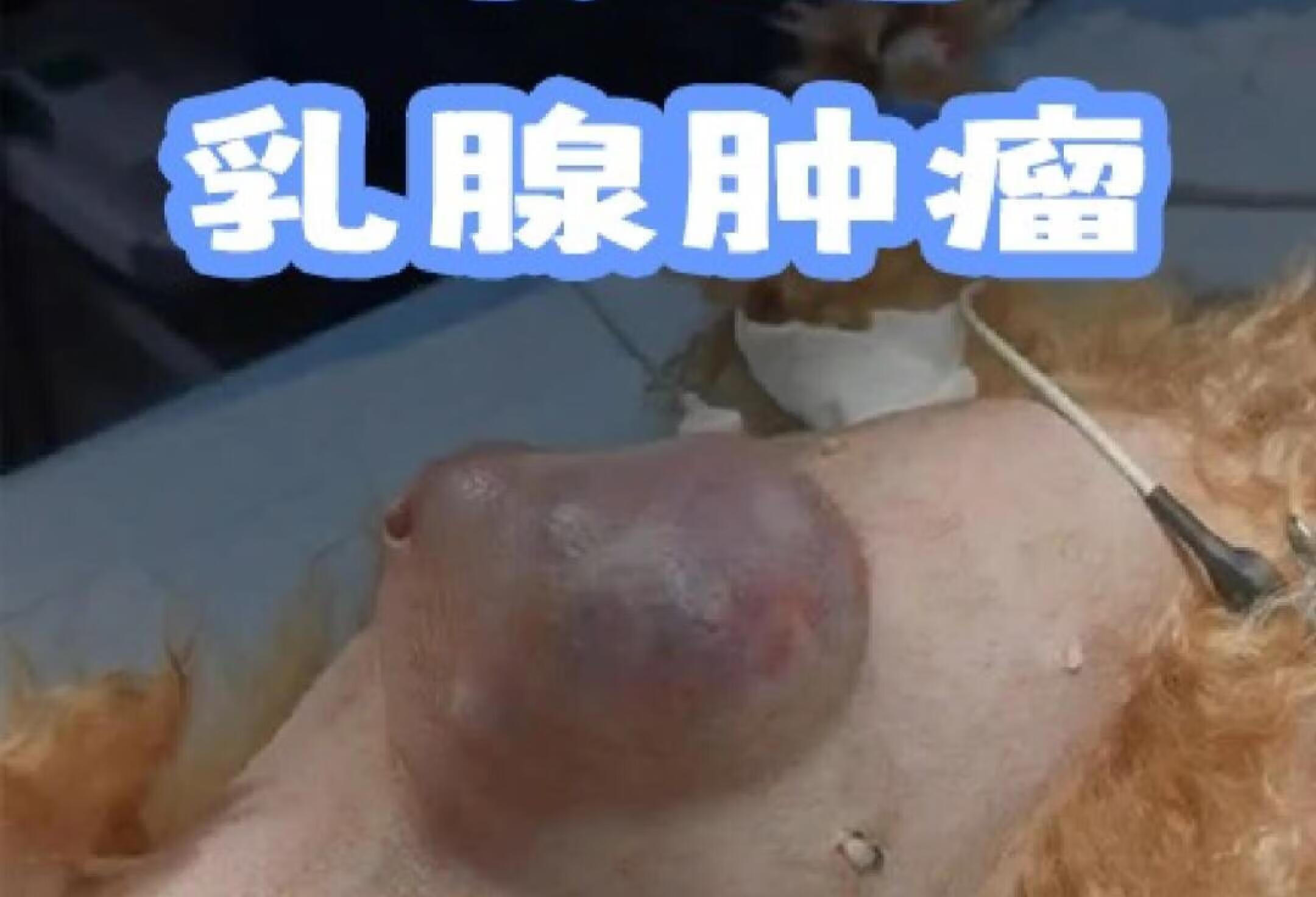
未绝育高发乳腺肿瘤恶性占多数

13岁狗子乳腺肿瘤...
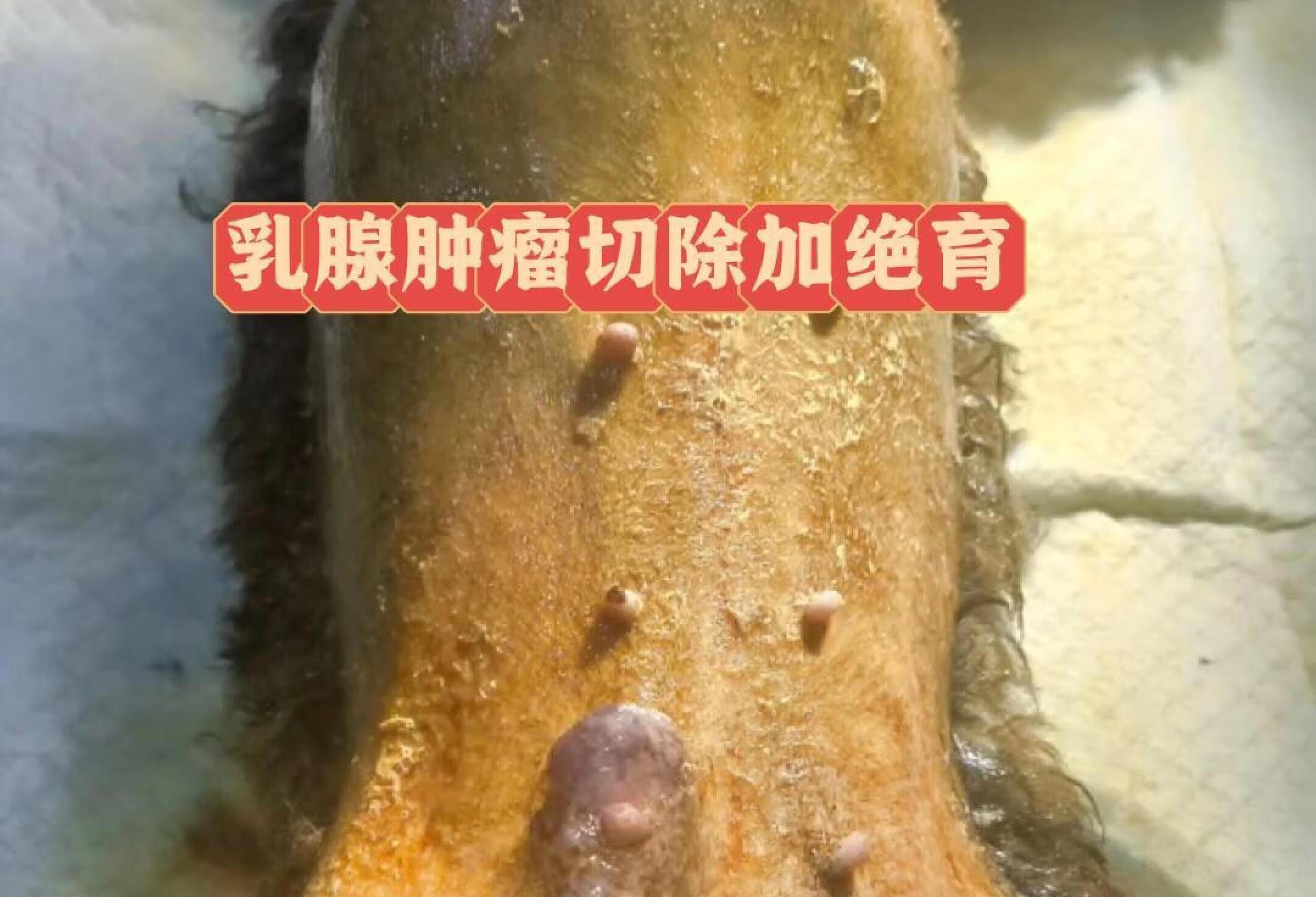
十六岁老奶奶乳腺肿瘤,主人怕破溃后无法护理所以坚定的选择提前切除,只想告诉大家这类疾病能全切不要单排切,能单排切除不单个切,也要一起做绝育,也有主人经常咨询乳腺肿瘤能否用氩氦刀,麻醉允许不建议用消融术。

罕见的患者
展开更多








