糖尿病肾病人能吃的零食有很多,比如无糖饼干、坚果、无糖酸奶等。
1.无糖饼干:制作过程中没有添加糖的饼干,具有饱腹作用,肚子饿的时候可以吃一点。
2.坚果:葵花籽、核桃、板栗、杏仁等,含有丰富营养物质,可以偶尔食用。
3.无糖酸奶:含有益生菌、蛋白质、钙等营养物质,可以帮助人体补充营养,又不含有糖分,可以偶尔食用。糖尿病肾病人吃任何零食都需以适量为主,另外还需及时去正规医院就诊,明确病因由医生指导个性化的诊疗方案,谨遵医嘱用药。

糖尿病肾衰竭死亡率较高。糖尿病肾衰竭是由于糖尿病肾病导致,是糖尿病中晚期的一种表现,早期可出现蛋白尿、高血压、水肿,后期会出现明显的肾功能异常,甚至出现贫血、脂质代谢紊乱、感染、心血管系统并发症等。糖尿病肾衰竭已经进入疾病的终末期,并且其发展速度比一般的肾脏疾病要快。无论是给予透析还是肾移植,患者的远期预后都比其他肾脏疾病导致的肾衰竭预后要差,死亡率较高。
所以建议糖尿病患者平时要积极使用二甲双胍等药物控制血糖,必要时注射胰岛素,使用缬沙坦、卡托普利等控制蛋白尿,后期需要使用透析,或者肾移植治疗,最大程度的延长寿命。建议糖尿病肾衰竭的患者及时就医,积极治疗,以上用药遵医嘱。

肾性糖尿病需要注意控制血糖、控制血压、注意尿液变化、饮食调整、定期检查等。
1.控制血糖:严格控制血糖对于肾性糖尿病患者至关重要,因为高血糖会加重肾脏损害。应通过饮食、运动和药物等综合手段来控制血糖水平。
2.控制血压:严格控制血压可以降低肾脏损伤的风险。患者应在医生的指导下采取合理的降压措施,如饮食控制、适量运动、药物等。
3.注意尿液变化:肾性糖尿病患者需要注意尿液的变化,如出现尿频、尿急、尿痛等症状,可能是尿路感染等肾脏疾病的表现,应及时就医检查。
4.饮食调整:饮食中应注意控制蛋白质的摄入量,以减轻肾脏负担。同时,应适量摄入优质蛋白质,如鱼、肉等。此外,严格控制饮食中盐的摄入也是必要的。
5.定期检查:肾性糖尿病患者需要定期进行肾功能检查,以便及时发现并处理肾脏问题。同时,也需要根据医生建议进行其他相关检查,如尿常规、血糖、血压等。
日常生活中,还应适量运动,提高身体免疫力,有助于延缓肾损害的进展。适量饮水,以利于代谢废物的排出。建议肾性糖尿病患者,严格遵医进行治疗,以免病情加重。

Ⅱ型糖尿病肾病慢性肾炎蛋白尿,血压血糖不稳定,脚踝出现水肿,可以是肾漏蛋白引起,也可以是心功能引起。如果是漏蛋白引起的脚踝水肿,首先是补充点白蛋白,在补充白蛋白的基础上再用止漏蛋白的药,它的效果才比较好。不能只是用止漏,不补白蛋白,血浆渗透压还是低,是不能把水拉回到血管里面去。心肾功能不全引起的静水压高导致下肢水肿,要用一点利尿药才能把脚踝水肿给缓解掉。脚踝水肿一定要验心功能怎么样,BMP怎么样,肾功能怎么样,肌酐水平怎么样,肌肝清除率怎么样,再验24小时尿蛋白定量和血浆白蛋白,综合评价到底是漏蛋白引起的水肿还是心肾功能不全引起的静入水压高导致的水肿。



本期话题:糖尿病肾病是怎么得的呀?
出镜嘉宾:北京医院肾病内科 主任医师 吴华
擅长领域:血液透析、急性、原发性肾小球肾炎、继发性肾炎、糖尿病肾病、高血压肾病、肾动脉狭窄、狼疮性肾炎等、各种泌尿道感染、肾小管间质性肾病、急性肾损伤、慢性肾病,慢性肾功能不全等

一般普通的慢性肾脏病,肾功能进展速度是平均每年肾小球滤过率降低 4ml/min(正常值是 90 以上),而糖尿病肾病的进展速度,则达到了 5-10ml/min。
这是什么概念呢?
我们从刚出现肾功能损害开始算,普通的肾病患者进展到尿毒症(滤过率 15)要多久?(90-15 )/4 = 18.75 年。
而糖尿病肾病进展到要多久?糖肾有两点比较特殊,一是进展速度快,滤过率每年下降 5-10,我们按平均 7.5 算;二是透析早(并发症多、滤过率虚高),滤过率 20 左右就要透析。时间是(90-20 )/7.5 = 9.3 年,早了 9 年多。
这是从肾衰初期开始算。实际上在发生肾衰之前,糖尿病肾病的进展速度也显著领先于其他肾病。流行病学研究数据,多数肾病发展至肾衰在 10-15 年以上;而糖肾从出现尿蛋白到肾衰平均只有 5 年。又早了 5-10 年。
同样是肾病,糖肾进展更快,到尿毒症的时间比平均早 15 年左右。正因如此,糖肾被认为是最难治、最危险的肾病。
所以,糖肾的管控,必须比其他肾病更加严格。
严到什么程度?
我经常说,IgA 肾病、膜性肾病等等这些常见的肾病,尿蛋白控制目标值是 0.5g 以下。比如 0.2g、0.4g,虽然仍然超标,但没有显著危害,只要低于 0.5g 就可以认为是安全的,长期随访数据也支持这一结论,我一直
但糖肾的尿蛋白控制目标则不同: 0.15g 以下。
没错,就是正常值。
其他肾病可以允许尿蛋白略微偏高,而糖肾的尿蛋白,需要降到完全正常。
有必要这么严格吗?是不是小题大做了?
没有小题大做,对于糖肾这种高进展风险的肾病,确实有必要降至完全正常。
最近,《中华肾脏病杂志》发布了《2022 版慢性肾脏病早期筛查、诊断及防治指南》
这部指南在 5 年也发布过一版,但当年我国的糖尿病肾病患者数量刚刚开始飙升,还未引起广泛注意。
而这次的新版指南,专门新增了糖尿病肾病的管控目标:尿微量白蛋白/肌酐比值 30mg/g。
尿微量白蛋白/肌酐比值是一个单次尿的单位,30mg/g 换算为 24 小时尿蛋白定量为 0.15g.
《美国肾脏病学会期刊》曾经发过研究,显示糖肾患者的尿白蛋白肌酐比,在>30mg/g(相当于定量 0.15g)时,就已出现了一定比例的肾单位损伤。只是有其它肾单位接管工作,肾功能才没有出现衰竭。
但不能总让其它肾单位接管工作。肾脏进化出了额外的肾单位,是因为它无法保持高强度的连续工作。肾单位交替工作、休息是必须的,得不到休息就会逐步累死。
在治疗方面,新指南在以前的药物基础上,新增了醛固酮拮抗剂。
因为以前的醛固酮拮抗剂,比如螺内酯、依普利酮,虽然勉强能用,但总归不如人意。近两年出现了第三代醛固酮拮抗剂——非奈利酮。
而且在上个月刚刚过去的欧洲肾脏病年会上,公布了 FIDELITY 研究的亚组分析:非奈利酮治疗 4 期糖肾,肾功能恶化风险降低了 39%,令人鼓舞。
以前,糖肾往往是单药治疗肾脏,达标有一定困难。现在有了列净类、肽类、非奈利酮等新型药物,又有中医药进一步降低尿蛋白,糖肾这种尿毒症风险最大的肾病,正式进入以「完全正常」为导向的时代!
细胞焦亡是一种特殊的溶解性程序性细胞死亡过程,其特点是细胞肿胀、破裂、分泌细胞内容物和显著的促炎作用。在焦亡过程中,通过炎症小体、激活半胱氨酸蛋白酶和裂解胃泌素D(GSDMD)以及分泌IL-18和IL-1β来检测危险信号和细胞事件。焦亡可分为典型途径和非典型途径,其中NLRP3炎症小体是最重要的引发物。糖尿病肾病(DKD)是糖尿病最严重的微血管并发症之一。目前的证据报道了高血糖诱导的细胞应激在肾细胞焦亡中的刺激作用,并且不同的信号通路已经被证明可以调节焦亡的起始。此外,由焦亡引起的炎症和细胞损伤与DKD进展、加重肾纤维化、肾小球硬化和肾小管损伤密切相关。一些已上市的降糖药物在焦亡调节通路中发挥抑制作用。最近的研究也报道了一些潜在的靶向焦亡途径的方法,这些方法在体内或体外模型中可以有效抑制肾细胞焦亡,减轻DKD。本位综合整理DKD中焦亡调控的相关信息,对相关的新见解进行归纳总结。
根据国际糖尿病联合会糖尿病地图集第9版的数据,到2020年,全球将有近10亿人罹患糖尿病,预计到2030年,这一数据将增加25%,到2045年,预计将增加51%。作为糖尿病患者最严重的微血管并发症之一,DKD的发病率也在逐年上升。DKD是一种由多种炎症因子介导的具有复杂生理病理机制的代谢性疾病。多种因素,如高血糖、脂代谢紊乱、氧化应激和晚期糖基化终产物(AGEs)等贯穿于DKD的整个过程。值得注意的是,目前的一些研究已经证明,高血糖、脂肪酸和其他损伤相关分子可以被细胞中一些特定的模式识别受体(Prr)识别,并诱导发生细胞焦亡,导致肾脏损害和功能下降,焦亡的信号转导途径与DKD的发病机制密不可分。
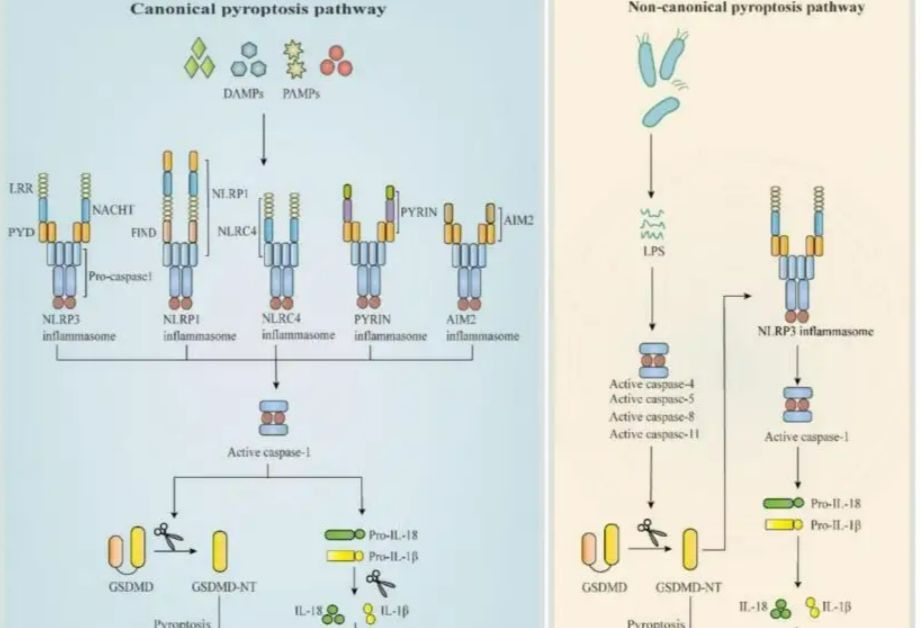
典型的炎症小体焦亡途径
炎症小体是一种多蛋白复合物,在细胞焦亡过程中起分子开关作用,参与多种炎症疾病的发生。不同类型的炎症小体在细胞焦亡过程中起着转换作用,主要包括结节样受体(NLRs)、黑色素瘤缺失的Pyrin和HIN200蛋白(AIM2)。特别是与焦亡有关的NLRP1、NLRP3、NLRP6、NLRP7和NLRC4,主要炎症小体的结构如图1所示。

图1(来源于文献)
NLRP3炎症小体被证明是与焦亡发生联系最紧密的分子,NLRP3炎症小体可被多种刺激激活,参与多种信号机制。目前的研究表明,它在DKD的焦亡起始和促炎细胞因子的产生中起关键作用。例如,小鼠NLRP3缺失可显著阻断caspase -1介导的IL-1β分泌,保护DKD肾脏免受损伤。研究人员还发现,糖尿病组织中与焦亡相关的蛋白ELA VL1、NLRP3和caspase-1明显上调。随着研究的深入,NLRP3炎性小体激活的许多信号机制已被证实参与了DKD的进展,这些诱发因子都与肾脏复杂的代谢变化相互作用。
非典型炎症体焦亡途径
研究发现,在人类中凋亡的非典型途径通过caspase-4和caspase-5介导,在小鼠研究中则为caspase-11。Caspase-4/5和caspase-11具有较高的特异性和亲和力,可直接与脂多糖(LPS)或脂质A结合激活。经检测,GSDMD是炎性caspases的直接底物,而活化的caspase-1/4/5/11为四聚体,用于裂解纯化的重组GSDMD。最近,也有报道称Caspase -8在细胞焦亡中表现出类似于热解的作用。Caspase 11在LPS作用下,通过裂解53 kda的GSDMD前体形式,产生成熟GSDMD的n端前热解片段,从而触发焦亡诱导。同时,也证实了caspase-11介导的GSDMD成熟有助于Nlrp3依赖的caspase-1激活和IL-1β释放。激活的caspase-4/5/11可逆转激活NLRP3炎性小体,推动IL-1β和IL-18的成熟和分泌。Caspase-11甚至可以在没有LPS的刺激下激活NLRP3。此外,有证据报道除了GSDMD外,caspase-4/5/11还可以作用于通道蛋白Pannexin-1,调节炎症介质的释放。
糖尿病肾病细胞焦亡的调控途径
焦亡途径调控在糖尿病肾脏中非常常见,肾损伤与这些调控分子的积累呈正相关。目前的研究表明,在DKD条件下,NLRP3炎症小体激活参与了焦亡途径的调控。确切地说,不同的病原体相关分子模式( PAMPs)直接与Toll样受体( TLRs)结合,触发NLRP3的启动信号,从而刺激NLRP3、caspase-1、pro-IL-1β和pro-IL-18的转录上调。通过这种方式,炎症小体被完全激活,在这一步骤中,多因素风险被整合到不同的细胞应激中(如离子通量、ROS生成、AGEs积累、线粒体功能障碍、吞噬体失稳等),并发挥间接激活剂的作用。
焦亡在糖尿病肾病中的病理作用
糖尿病肾病的发病机制十分复杂,焦亡反应介导的肾脏炎症是导致DKD的一个重要因素,而驻留的肾细胞是触发和维持这种炎症的关键。实际上,肾功能的恶化与焦亡调控分子的强度密切相关。最近的研究显示,在DKD进展过程中,肾驻留细胞焦亡可严重影响肾功能。此外,NLRP3炎性小体的各种激活信号通路参与了肾驻留细胞的焦亡。在DKD的发展过程中,持续肾损伤后未解决的炎症可促进纤维形成阶段,从而导致后期发生胶原沉积和积累,导致肾实质逐渐硬化,形成疤痕,直至肾功能完全衰竭。
糖尿病肾病的靶向治疗药物
目前治疗糖尿病肾病的药物主要有血管紧张素转换酶抑制剂(ACEIs)或血管紧张素II受体阻滞剂(ARBs),它们只能延缓糖尿病肾病的进展,而不能逆转其发展。因此,越来越多的研究聚焦于内在肾脏通路,以发现更多潜在的治疗方法。从焦亡途径出发,目前已经有多种药物正在研发,这些肾保护药物综述如(图2)所示。

图2(来源于文献)
虽然ACEIs和ARB已在临床上使用,但由于其不良反应,仍然存在争议。 典型的钠-葡萄糖共转运体2型抑制剂,如达格列净和恩格列净,可以抑制糖尿病肾脏Asc、Caspase-1、IL-1β的表达和NLRP3炎症体的活性。MCC950可通过抑制NLRP3炎性小体的活化,下调肾树突状细胞IL-18和IL-1β的表达,从而阻止炎症形成,进一步导致肾纤维化。二肽基肽酶-4抑制剂沙格列汀也显示出类似的疗效。虽然这些药物对焦亡的关键分子有明显的抑制作用,并且不依赖于它们的降糖活性来缓解DKD,但它们是否通过细胞焦亡机制发挥这些作用还需要进一步的证实。
尽管仍处于试验阶段,但一些潜在的治疗方法在糖尿病肾脏中表现出了优异的药理作用。例如,腺苷A3受体拮抗剂(ADORA3)已经被证明可以通过抑制HK-2中的NF-κB/NLRP3信号来减弱DKD,从而阻断胱天蛋白酶-1、白介素-18和白介素-1β的表达;P2受体拮抗剂如TNP-三磷酸腺苷和苏拉明也在试验中降低了焦磷酸相关分子的表达,并减弱了DKD;此外,短链脂肪酸NaB可通过抑制焦磷酸典型途径来预防氧化应激和缓解DKD病,这些都对后续的药物研究方向提供了参考。
值得注意的是,随着遗传学的研究趋势,白介素-22和一些类型的长非编码RNA 的基因治疗也在抑制肾细胞焦磷酸症方面发挥了巨大作用,从而减轻肾纤维化和DKD进展。
参考文献:MDPI Int. J. Mol. Sci. 2020, 21, 7057
糖尿病是一种常见病和多发病,我们认识的熟人中基本上都有糖尿病的患者。它是以慢性高血糖为特征的代谢性疾病,是由于胰岛素分泌和(或)利用缺陷所引起的长期碳水化合物以及脂肪、蛋白质代谢紊乱可引起多系统损害,导致眼、肾、神经、心脏、血管等组织器官慢性进行性病变、功能减退及衰竭。在我国,糖尿病是导致成人失明、非创伤性截肢、终末期肾脏病的主要原因。
微血管病变是糖尿病的特异性并发症,其典型改变是微血管基底膜增厚和微循环障碍。常见于病史超过 10 年的病人。糖尿病肾病是糖尿病最常见的并发症,而 2 型糖尿病中约 5%的患者在诊断为糖尿病时已经存在糖尿病肾病。一般要明确是否为糖尿病肾病,需要满足以下 3 点:①有长期的糖尿病史;②出现微量的白蛋白尿;③伴有糖尿病视网膜病变。对于那些不典型的患者,可以行肾穿刺活检明确诊断。
目前对糖尿病肾病的治疗,还是强调干预各种危险因素,比喻积极控制血糖、血压,调节脂质代谢紊乱,调节生活方式(控盐、控烟、控制体重等),及时治疗出现的各种并发症,对于 GFR<15ml/min 的患者,有透析指征的患者积极透析治疗,血透和腹透都可以考虑。具体选择哪种透析模式,根据患者具体情况选择合适的透析方式。
近年来,钠-葡萄糖协同转运蛋白-2(SGLT-2)抑制剂,一种新型的口服降糖药物,包括达格列净、恩格列净和卡格列净等,已被证实对肾具有保护作用,使得糖尿病肾病的治疗迎来了新的曙光,被誉为 20 年以来自血管紧张素转化酶抑制剂(ACEI)类药物后最大的进展。SGLT-2 抑制剂对肾保护机制主要包括降低血糖、改善肾高滤过状态、降低蛋白尿、改善肾缺氧、减轻体重、降低血压、降低尿酸、减轻炎症和氧化应激作用等,可以说是针对糖尿病肾病的各个环节起作用,所以值得我们肾科医生足够的期待。
展开更多











 武汉市精神卫生中心
武汉市精神卫生中心
 京东互联网医院育婴师团队
京东互联网医院育婴师团队
 首都儿科研究所附属儿童医院
首都儿科研究所附属儿童医院
 雄县中医医院
雄县中医医院
 延津县人民医院
延津县人民医院
 重庆医科大学附属儿童医院
重庆医科大学附属儿童医院
 京东互联网医院育婴师团队
京东互联网医院育婴师团队
 济南市儿童医院
济南市儿童医院
 北京同仁堂鞍山大药房有限公司铁东区中医诊所
北京同仁堂鞍山大药房有限公司铁东区中医诊所
 武汉市精神卫生中心
武汉市精神卫生中心









