
视频简介
作者信息:北京大学第一医院 感染内科 主任医师 陆海英
流行性乙型脑炎属于病毒性感染疾病,具有一定的自愈性。但流行性乙型脑炎是属于一种比较严重的脑炎,可以出现一些严重的并发症,有一定的病死率,需要及时的住院治疗减少或避免后遗症的发生。
第一、如果一旦发现患有流行性乙型脑炎,必须第一时间到医院进行治疗,如果没有进行及时的治疗会造成病情的延误或者是病情的加重,尤其是对孩子来说,可能会造成脑部的损伤,影响到智力。
第二、要做好患者的护理工作,包括个人的卫生、清洁、饮食、营养补充等,这些护理措施对病情的恢复都起到至关重要的作用。
第三、除了通过西医治疗或饮食的调理外,还可以采用中医中药的方式进行治疗,在急性期以清热解毒药物,也可以用物理的方式帮助缓解身体的不适症状,比如说可以用针灸、按摩、理疗、推拿帮助缓解疾病症状问题。
因此轻型的流行性乙型脑炎可以自愈,但大部分的流行性乙型脑炎需要通过上述的方式治疗以达到治愈的效果。

视频简介
作者信息:北京大学第一医院 感染内科 主任医师 陆海英
流行性乙型脑炎疫苗的免疫时间为5~10年,中国规定乙脑疫苗接种的对象主要是流行期6个月到10岁的儿童,以及非流行区进入流行区的人群。
乙脑灭活疫苗一共要接种两针,宝宝满6个月接种第一针,7~10天后接种第二针,1岁半到2岁,也就是18个月到24个月,以及4岁、6岁各加强免疫一针。乙脑灭火疫苗保护率在60%~90%,免疫效果可维持10年。
乙脑减毒疫苗一岁时接种一针,2岁时加强一针,7岁再加强免疫一针,乙脑减毒疫苗第一次注射后保护率达百分之80左右,第二次打了加强疫苗后,保护率能达到90%以上,免疫的效果可持续5~11年。

进入六月,天气炎热,蚊子明显多了起来,讨厌的蚊子不光扰民,而且还可以传播多种传染病,乙脑就是由蚊子传播的一种小儿急性传染病。
乙脑即乙型病毒性脑炎,患儿主要表现为持续高热、头痛、呕吐、昏迷不醒、频繁抽搐等。重症患儿还可留有癫痫、精神失常等神经系统后遗症,病死率高达 30%左右。好可怕!您可能还不知道吧,乙脑多在夏季流行,我国病例主要集中在 7、8、9 三个月。有关乙脑预防,宝爸宝妈还需知道哪些事呢?
1. 乙脑有什么症状?
乙脑病例大多集中在 10 岁以下的儿童,以 2-6 岁组发病率最高,严重的乙脑会导致体温迅速上升,高烧甚至会超过 40℃,伴有反复或持续强烈抽搐,于 1~2 日内出现深昏迷,有脑疝和中枢性呼吸衰竭等表现,如不及时抢救,常因呼吸衰竭而死亡。
2. 乙脑的传染源和传播途径是什么?
病人和猪是乙脑的主要传染源。乙脑主要通过蚊虫叮咬传播给人类。
3. 哪些人群容易感染乙脑?
人对乙脑病毒普遍易感,但绝大多数是无症状的隐性感染者,少年儿童是主要发病人群,大多数成人因隐性感染而获得持久免疫力。近年来由于儿童和青少年广泛接种疫苗,成人及老年人的发病率则相对增加。
4. 日常生活中如何预防乙脑?
接种疫苗
儿童应按期进行乙脑疫苗的预防接种,以使体内产生抗乙脑病毒的抗体,保护儿童免遭乙脑病毒的侵袭。
防蚊灭蚊
- 日落后避免在树荫、草丛、牲畜棚附近逗留;
- 户外活动时,应穿长袖衣服及长裤,并在外露的皮肤及衣服上涂抹蚊虫驱避药物;
- 家庭应安装蚊帐、纱窗;
- 及时清理家中花盆、水缸、废弃罐子的积水。
蚊子作为众多传染病的储存宿主,除了传播裂谷热、乙脑外,还可能携带有登革热、疟疾、寨卡病毒病、基孔肯雅热等 80 多种传染病的病原。而采取有效的措施防蚊灭蚊,可以避免这些疾病的侵袭,保证身体健康。为了度过一个愉快又健康的夏天,就从防蚊灭蚊开始吧!
流行性乙型脑炎主要流行于夏秋季,80%-90%乙脑的病例集中在 7、8、9 三个月,具有发病急、进程快、疫情凶险、病死率高等特点。正值夏季,预防乙脑势在必行!
流行性乙型脑炎到底是什么?
流行性乙型脑炎,是以蚊虫为传播媒介的人畜共患的一种急性病毒性传染病。
与其它传染病相比,乙脑的发病率虽然不高,但病死率高,部分患者病愈后还会留下后遗症。
乙脑的流行特征
- 乙脑的流行季节为每年 7-9 月,其中 7 月下旬至 8 月上旬为发病高峰期,乙脑通过携带乙脑病毒的蚊子叮咬传播,其中三带喙库蚊是主要的传播媒介。
- 乙脑发病主要以儿童和青少年为主,但近年来成人发病呈现增多趋势。
早期诊治乙脑是治疗的关键
乙脑发病初 1-2 日常有发热、头痛,并伴有恶心、呕吐、嗜睡等症状,与感冒相似。多数乙脑发病后 4 到 10 天症状会加重,有的甚至会出现昏迷、抽搐和呼吸衰竭。在夏秋季,如果遇到发病比较急,出现高烧、头痛的病人,就要及时送往医院诊断,以免延误治疗。
如何预防乙脑
- 做好防蚊、灭蚊,消灭蚊虫孳生地。保持家畜、禽舍的卫生,消除积水,填平洼地。夏天可以使用纱窗、蚊帐、蚊香,涂擦驱蚊剂等措施防止被蚊虫叮咬。
- 对易感人群接种乙脑疫苗。儿童可在 8 个月龄免费接种 1 剂乙脑减毒活疫苗,2 岁时可接种第 2 剂。
- 流行季节出现持续高热、头痛、抽搐等类似症状,应立即送医就诊,及早明确诊断,以免贻误病情。
乙脑疫苗
我国 70 年代以后大范围接种乙脑疫苗,为了更多的儿童远疫苗。我国的乙脑减活疫苗,质量标准高,并获得世界卫生组织预认证,免疫效果和安全性被世界卫生组织认可。还有一种乙脑灭活疫苗,是自费疫苗。
2016 年 12 月 6 日,国家卫计委发布最新版疫苗免疫程序和说明,里面明确给出了流行季节疫苗接种建议:国家免疫规划使用的疫苗都可以按照免疫程序和预防接种方案的要求,全年(包括流行季节)开展常规接种,或根据需要开展补充免疫和应急接种。
乙脑减毒活疫苗的接种
乙脑减毒活疫苗全程需要接种 2 针次,第一针是宝宝满 8 月时,第二针是宝宝满 2 岁时。乙脑灭活疫苗全程需要接种 4 针次,8 月龄接种 2 剂,间隔 7~10 天;2 周岁和 6 周岁各接种 1 剂
流行性乙型脑炎简称“乙脑”“日本脑炎”,是因为乙型脑炎病毒感染人体引起的以脑实质发生炎性病变的一种中枢神经系统急性传染病,属于我国法定的乙类传染病。诊断明确后需要采取相应的隔离措施。
乙脑是经蚊传播,多发生于夏、秋两季,典型临床症状有高热、脑膜刺激征、意识障碍等。乙脑的诊断主要需要根据流行病学史、症状体征以及特异性的病原学化验等。乙脑需要积极预防,接种乙脑疫苗是保护易感人群的根本措施。那么,为什么打乙脑会发烧呢?具体有以下几个方面的内容:
- 乙脑属于一类计划免疫接种范畴,我国目前多使用地鼠肾细胞灭活、或者是减毒的活疫苗,保护率可达到 75%左右。
- 乙脑疫苗的接种对象一般为十岁以下的少年儿童、以及进入乙脑疫区的人员,常规接种两次,两次间隔在 7-10 天左右。
- 不论是接种减毒还是灭活的乙脑疫苗,都是刺激人体引起免疫反应而产生抗体。同时,也可引起发烧等副反应的发生。
- 接种乙脑疫苗后引起发烧,一般为一过性的发热,不需要特殊处理。如果持续出现高热症状,药物退热的同时注意及时面诊。
综合以上所叙述的几方面的内容,乙脑需要积极预防,做到防蚊灭蚊、预防接种等多项措施。如果有可疑的流行病学史、或出现相关的症状,一定及时诊治。
乙脑也称为日本脑炎,是因为乙型脑炎病毒感染人体导致,多侵犯中枢神经系统。乙脑属于乙类防控管理的传染病,好发生于夏、秋两季,人对乙脑病毒存在普遍的易感性。明确诊断后需要采取相应的隔离措施。
乙脑的潜伏期一般在 10-14 天左右,根据临床表现的不同可分为初期、极期、恢复期、以及后遗症期。乙脑需要积极预防,做到防蚊灭蚊,按时接种疫苗。那么,接种乙脑减毒活疫苗后出现发烧怎么办呢?具体有以下几个方面的内容:
- (一)目前我国多使用地鼠肾细胞灭活、或减毒的乙脑疫苗,接种对象以 10 岁以下的少年儿童为主。如果是进入疫区的人员,感染风险大,也需要接种疫苗。
- (二)乙脑减毒活疫苗为降低了毒性的乙脑病毒。接种后可刺激人体免疫系统反应而在不致病的情况下产生大量抗体,从而起到预防疾病发生的目的。
- (三)使用乙脑减毒活疫苗后,机体发生免疫反应的过程中会出现体温升高等副反应。
- (四)接种减毒活疫苗后如出现低热,一般可以通过多喝水、物理降温等对症措施来缓解接种疫苗后的副反应。
- (五)接种乙脑减毒活疫苗后如出现高热,物理降温的同时注意配合布洛芬、乙酰氨基酚混悬滴剂进行药物退烧治疗。如接种者持续高热不退,需及时面诊,以防出现高热惊厥等并发症。

流行性乙型脑炎简称“乙脑”“日本脑炎”,是因为乙型脑炎病毒感染人体引起的以脑实质发生炎性病变的一种中枢神经系统急性传染病,属于我国法定的乙类传染病。诊断明确后需要采取相应的隔离措施。
乙脑是经蚊传播,多发生于夏、秋两季,典型临床症状有高热、脑膜刺激征、意识障碍等。乙脑的诊断主要需要根据流行病学史、症状体征以及特异性的病原学化验等。乙脑需要积极预防,接种乙脑疫苗是保护易感人群的根本措施。那么,为什么打乙脑会发烧呢?具体有以下几个方面的内容:
(一)乙脑属于一类计划免疫接种范畴,我国目前多使用地鼠肾细胞灭活、或者是减毒的活疫苗,保护率可达到75%左右。
(二)乙脑疫苗的接种对象一般为十岁以下的少年儿童、以及进入乙脑疫区的人员,常规接种两次,两次间隔在7-10天左右。
(三)不论是接种减毒还是灭活的乙脑疫苗,都是刺激人体引起免疫反应而产生抗体。同时,也可引起发烧等副反应的发生。
(四)接种乙脑疫苗后引起发烧,一般为一过性的发热,不需要特殊处理。如果持续出现高热症状,药物退热的同时注意及时面诊。
综合以上所叙述的几方面的内容,乙脑需要积极预防,做到防蚊灭蚊、预防接种等多项措施。如果有可疑的流行病学史、或出现相关的症状,一定及时诊治。

夏季来临,随着气温的攀升及雨水的逐渐增多,蚊虫进入每年的活跃期,蚊虫滋扰带来的不止有皮肤鼓包红肿、嗡嗡噪音,最可恶的是会传播多种疾病。流行性乙型脑炎即为其中一种。
”
流行性乙型脑炎(简称乙脑),又称日本脑炎。是由乙脑病毒引起的侵害中枢神经系统的一种急性传染病。其发病具有明显的季节性和地理区域分布特点,世界范围分布以亚洲地区为主,是引起亚洲儿童神经系统感染的首要病因。我国是发病主要国家之一,发病高峰期在夏秋季,儿童发病为主。
乙型脑炎主要传染源为猪,尤其是仔猪,蚊虫叮咬感染乙脑病毒的猪后其受感染率很高,再由被感染蚊虫叮咬人,即构成猪-蚊-人的传播模式。本病潜伏期4-21天,一般10-14天,人感染后大多为隐性感染,而发病人群中主要临床症状以高热、惊厥、昏迷、及脑膜刺激征为特征,重症则伴有呼吸衰竭,病死率高达20-30%,幸存者中约有30-50%存在严重神经系统后遗症,包括失语、意识障碍、肢体障碍、痴呆及癫痫等,其中癫痫后遗症可持续终生。
流行性乙型脑炎是可防可控的。
主要防范措施有
一、接种疫苗:目前国内外应用的乙脑疫苗有灭活疫苗(Vero细胞)和乙脑减毒活疫苗两种。我省已将乙脑减毒活疫苗纳入扩大国家免疫规划,适龄儿童可免费接种,免疫程序为两剂次,8月龄及2周岁各接种1剂次。
二、防蚊灭蚊:防止蚊虫叮咬,在皮肤或衣服表面使用含有避蚊胺成分的驱避剂,睡眠时使用蚊帐、蚊香等防护用品。晨间及黄昏户外出行时穿着长袖及长裤。保持良好的生活环境,及时清除垃圾及积水,防止蚊虫孳生。
对流行季节期间或到过流行地后出现的高热或类似感冒病征的应及时就医,早发现,早诊断,早治疗。

2024年10月10日,辉瑞宣布,口服聚ADP-核糖聚合酶(PARP)抑制剂talazoparib与雄激素受体通路抑制剂(ARPI)enzalutamide联合治疗转移性去势抵抗性前列腺癌(mCRPC)患者的TALAPRO-2研究的总生存期(OS)结果呈阳性。
前列腺癌是全球男性第二大常见癌症,也是男性癌症死亡的第五大常见原因,mCRPC是一种转移到前列腺以外的癌症,且在接受药物/手术治疗后肿瘤仍继续进展。大约10%-20%的前列腺癌患者在诊断后5-7年内发展为mCRPC[1-3]。辉瑞的这个研究(TALAPRO-2 试验),也是目前唯一一个PARP抑制剂与ARPI联用的新疗法,或能显著提高转移性去势抵抗性前列腺癌患者的生存率。
TALAPRO-2试验是一项多中心随机双盲对照研究,目前招募了1,035名mCRPC患者。去势睾酮水平的患者随机分为两组,治疗组接受talazoparib0.5mg/天+enzalutamide 160mg/天,对照组接受安慰剂和enzalutamide160mg/天。

该试验的主要终点是rPFS。次要终点包括总生存期(OS)、客观缓解率(ORR) 、缓解持续时间(DOR)等[4]。根据辉瑞报道,与单药治疗(对照组)相比,所有参与者最终OS改善具有统计学意义和临床意义。
这个联合疗法于2023年6月获得美国食品药品监督管理局 (FDA批准,用于治疗HRR基因突变的 mCRPC成人患者。该联合疗法还于2024年1月获得欧盟委员会批准,用于治疗无临床指征的 mCRPC成人患者。除了治疗前列腺癌,talazoparib适应证还包括乳腺癌,适用于作为单一药物治疗有害/疑似有害种系乳腺癌易感基因 (BRCA)突变 (gBRCAm) 人表皮生长因子受体 2 (HER2) 阴性局部晚期或转移性乳腺癌的成年患者。
此外,新药应用还需关注其安全性,talazoparib用药可能引发严重不良后果[5],如骨髓增生异常综合征 / 急性髓系白血病(MDS/AML),在临床研究中,788 名实体瘤患者中有 0.4%(3 人)在单药使用 talazoparib后出现该病症。TALAPRO-2 研究中,511 名使用 talazoparib和恩杂鲁胺的患者中有 2 人(0.4%)出现 MDS/AML,而 517 名使用安慰剂和恩杂鲁胺的患者无人出现。出现 MDS/AML 的 5 名患者使用 talazoparib的时长分别为 0.3、1、2、3 和 5 年,多数患者此前接受过含铂化疗药物和 / 或其他 DNA 损伤药物包括放疗。用药前需确保患者从前期化疗导致的血液毒性中充分恢复,治疗期间每月监测血细胞计数,若出现长期血液毒性,暂停 talazoparib并每周监测计数,4 周内未恢复则转诊至血液科做进一步检查包括骨髓分析和细胞遗传学血样检查,若确诊 MDS/AML 需停药。
talazoparib还会引发骨髓抑制,表现为贫血、中性粒细胞减少和 / 或血小板减少。单药使用时,39%、21% 和 15% 的患者分别出现≥3 级的贫血、中性粒细胞减少和血小板减少,因这三种情况停药的患者分别占 0.7%、0.3% 和 0.3%。在 TALAPRO-2 中,使用 talazoparib和恩杂鲁胺的患者中分别有 45%、18% 和 8% 出现≥3 级上述情况,39% 的患者(199/511)需要输血,22%(111/511)需要多次输血,因这三种情况停药的患者分别占 7%、3% 和 0.4%。若因前期治疗出现血液毒性,需暂停 TALZENNA,治疗期间每月监测血细胞计数,28 天内未解决则停药并转诊至血液科做进一步检查。
基于作用机制和动物实验数据,talazoparib对孕妇有胎儿毒性,在动物生殖研究中,怀孕大鼠在器官发生期使用 talazoparib 会导致胎儿畸形、骨骼结构变异和胚胎死亡,暴露量为人类推荐剂量 1mg 每日的 AUC 的 0.24 倍。告知孕妇和有生育潜力的女性潜在风险,有生育潜力的女性在治疗期间及末次用药后 7 个月内需采取有效避孕措施。基于遗传毒性和动物生殖研究结果,建议有生育潜力女性伴侣或伴侣怀孕的男性患者在治疗期间及末次用药后 4 个月内采取有效避孕措施。
参考文献
1.Pfizer’s TALZENNA® in Combination with XTANDI® Prolongs Overall Survival in Phase 3 TALAPRO-2 Trial.
2.Bray F, Laversanne M, Sung H, et al. Global cancer statistics 2022: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries.CA: A Cancer Journal for Clinicians. 2024;74(3):229-263. Published 2024 April 4. 3.Kirby M, Hirst C, Crawford ED. Characterising the castration-resistant prostate cancer population: a systematic review. Int J Clin Pract. 2011 Nov;65(11):1180-92.
4.Talazoparib + Enzalutamide vs. Enzalutamide Monotherapy in mCRPC (TALAPRO-2)
5.Agarwal N, Azad A, Shore ND, Carles J, Fay AP, Dunshee C, Karsh LI, Paccagnella ML, Santo ND, Elmeliegy M, Lin X, Czibere A, Fizazi K. Talazoparib plus enzalutamide in metastatic castration-resistant prostate cancer: TALAPRO-2 phase III study design. Future Oncol. 2022 Feb;18(4):425-436. doi: 10.2217/fon-2021-0811. Epub 2022 Jan 26. PMID: 35080190.
6.TALZENNA- talazoparib capsule, liquid filled
当地时间2024年10月10日,FDA批准组合疗法用于乳腺癌治疗[1]。组合疗法包括inavolisib、palbociclib和氟维司群,组合疗法所治疗的乳腺癌并不一般,是内分泌耐药、PIK3CA突变、激素受体(HR)阳性、人表皮生长因子受体2(HER2)阴性、局部晚期或转移性乳腺癌,且这类乳腺癌在辅助内分泌治疗期间或完成辅助内分泌治疗后复发。

最常见的乳腺癌与耐药
激素受体阳性、HER2-乳腺癌是最常见的乳腺癌亚型[2]。晚期或转移性疾病的初始治疗包括单独使用内分泌治疗 (ET) 或与靶向治疗联合治疗,此后,治疗选择包括单独使用ET或与PI3K/AKT/mTOR通路抑制剂联合使用。但约40%的激素受体(HR)阳性、HER2阴性晚期乳腺癌患者携带PIK3CA基因突变[3]。PIK3CA突变的存在导致磷酸肌醇 3-激酶 (PI3K) 信号通路过度激活、治疗耐药和更差的预后。适应性和获得性耐药的出现,可用疗法的临床获益仍然有限。
为了解决耐药问题,罗氏设计了一项随机双盲对照III期试验,以评估包括inavolisib在内的组合疗法在HR+/HER2-局部晚期或转移性乳腺癌中的疗效。患者按1:1的比例随机分配至inavolisib 9mg或安慰剂口服,每日一次;palbociclib 125mg口服,每日一次,连续21天,然后停药7天;氟维司群 500 mg 在第1周期的第1天和第15天肌肉注射,然后在每 28 天周期的第1天肌肉注射。
无进展生存期达15个月,缓解持续时间有18.4个月
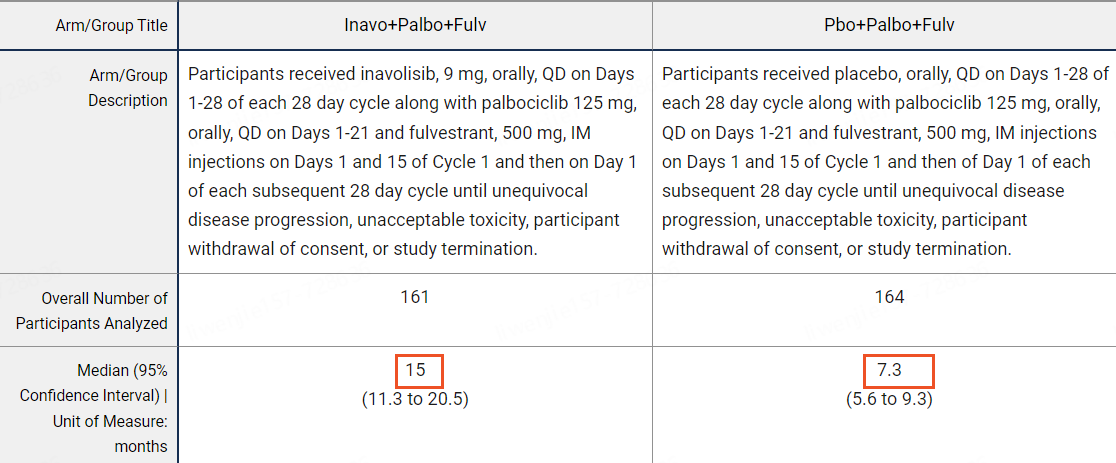
疗效主要结局用无进展生存期 (PFS)评估,也包括括总生存期(OS) 、客观缓解率(ORR)和缓解持续时间(DOR)。
研究结果表明,inavolisib组的中位PFS为15.0个月 (95% CI: 11.3, 20.5),对照组为 7.3 个月 (95% CI: 5.6, 9.3) (风险比 0.43 [95% CI: 0.32, 0.59] p 值 <0.0001)。inavolisib组的 ORR为58% (95% CI: 50, 66),对照组的ORR为25% (95% CI: 19, 32)。中位 DOR 分别为 18.4 个月 (95% CI: 10.4, 22.2) 和 9.6 个月 (95% CI: 7.4, 16.6)[1,4]。
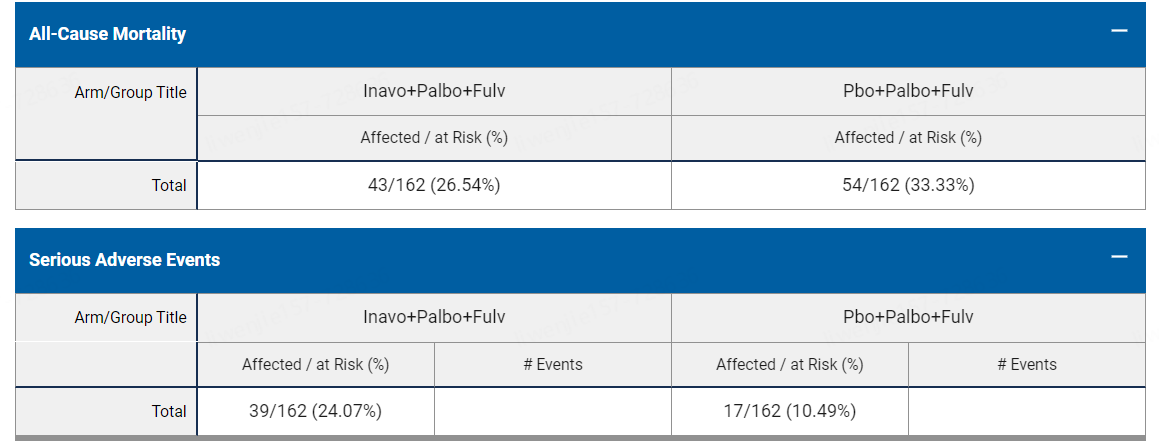
在安全性方面,最常见的不良反应 (≥20%),包括实验室异常,是中性粒细胞减少、血红蛋白降低、空腹血糖升高、血小板减少、淋巴细胞减少、口腔炎、腹泻、钙减少、疲劳、钾减少、肌酐增加、ALT增加、恶心、钠减少、镁减少、皮疹、食欲下降和头痛等。组合疗法组和对照的全因死亡率分别为26.54 vs 33.33%,而严重不良反应发生率分别为24.07% vs 10.49%[4]。
应用新药还需注意什么?
注意到这项试验中的一些不良反应,应用新药时还需注意高血糖、腹泻等风险。
1.高血糖风险
高血糖在inavolisib应用中较为常见,但也可能很严重。因此在用药前和治疗期间监测需要注意血糖水平。如果患者刚好还有糖尿病病史,则更需要注意监测血糖。另外在治疗期间,应保持充足的水分。如果出现下列症状,可能为高血糖,需及时就医。
症状包括呼吸困难、持续2h恶心和呕吐、食欲异常增加、胃痛、过度口渴、口干、脸红、困倦或疲倦、和皮肤干燥,以及排尿比平时更频繁或尿量比正常多[5]。
2.腹泻
用inavolisib期间可能出现腹泻,严重腹泻会导致体内水分流失过多(脱水)和肾损伤。如果您在治疗期间出现腹泻、胃部区域(腹痛)或看到粪便中有粘液或血液,需及时就医。此外用药期间注意多喝水。
3.联合用药
这次获批为组合疗法,最常见的不良反应和异常血液检查结果包括:白细胞计数、红细胞计数和血小板计数降低,血液中的钙、钾、钠和镁水平降低,血液中肌酐水平升高,血液中肝酶丙氨酸转氨酶 (ALT) 水平升高,恶心和食欲不振、头痛。
参考文献:
1.FDA approves inavolisib with palbociclib and fulvestrant for endocrine-resistant, PIK3CA-mutated, HR-positive, HER2-negative, advanced breast cancer.
2.Jhaveri KL, Accordino MK, Bedard PL, Cervantes A, Gambardella V, Hamilton E, Italiano A, Kalinsky K, Krop IE, Oliveira M, Schmid P, Saura C, Turner NC, Varga A, Cheeti S, Hilz S, Hutchinson KE, Jin Y, Royer-Joo S, Peters U, Shankar N, Schutzman JL, Juric D. Phase I/Ib Trial of Inavolisib Plus Palbociclib and Endocrine Therapy forPIK3CA-Mutated, Hormone Receptor-Positive, Human Epidermal Growth Factor Receptor 2-Negative Advanced or Metastatic Breast Cancer. J Clin Oncol. 2024 Sep 5:JCO2400110. doi: 10.1200/JCO.24.00110. Epub ahead of print. PMID: 39236276.
3.Potential for Long-Term Disease Control with Alpelisib Plus Fulvestrant Spans Patient Subgroups in HR+PIK3CA-Mutated Advanced Breast Cancer,The Oncologist, Volume 26, Issue S3, July 2021, Pages S11–S12,https://doi.org/10.1002/onco.13873
4.A Study Evaluating the Efficacy and Safety of Inavolisib + Palbociclib + Fulvestrant vs Placebo + Palbociclib + Fulvestrant in Patients With PIK3CA-Mutant, Hormone Receptor-Positive, Her2-Negative, Locally Advanced or Metastatic Breast Cancer (INAVO120)
5.FDA Approves Genentech’s Itovebi, a Targeted Treatment for Advanced Hormone Receptor-Positive, HER2-Negative Breast Cancer With aPIK3CAMutation
展开更多















