
膝关节置换手术下肢水肿可以通过一般治疗、药物治疗、饮食调理等方法进行缓解。
1.一般治疗:首先要注意根据医生的指导,适当进行康复运动和活动,可以促进血液的循环和淋巴的流动。同时需要避免长时间的静坐或者站立。另外在休息或睡眠的时候,将下肢抬高,以促进血液和淋巴液的流动。如果局部肿胀和疼痛明显,还可适当采用冷敷的方法进行缓解。
2.药物治疗:可以在医生指导下,服用利尿剂将液体排出体外,达到消肿的作用,如常用的呋塞米、布美他尼等。
3.因素调理:要注意控制盐分的摄入,因为盐分可导致水分潴留,同时要注意保持均衡的饮食,摄入足够的蛋白质和营养,也可起到促进病情的恢复。
一旦出现膝关节置换手术后下肢水肿的现象,需尽快到医院就诊,在医生指导下进行合理治疗。
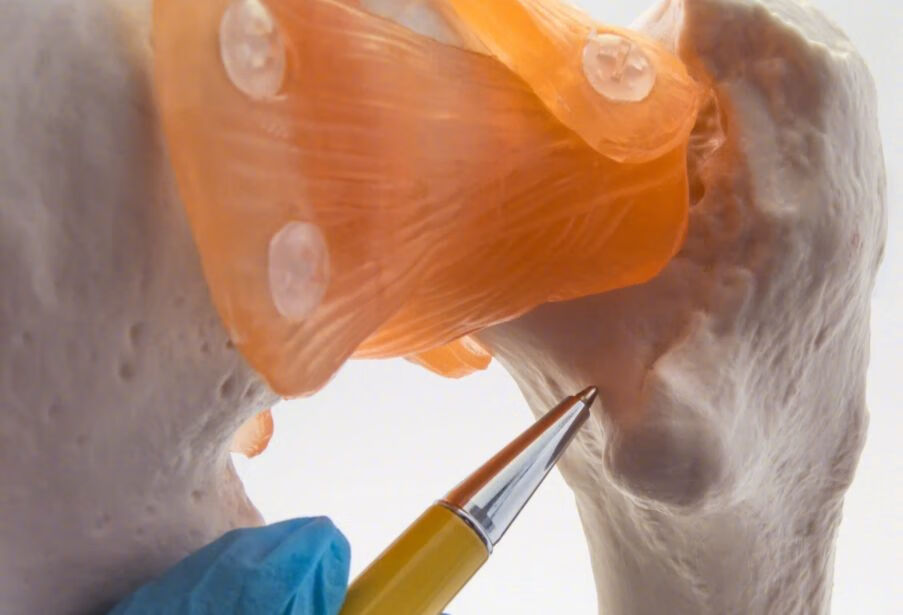
人工膝关节置换术后功能锻炼
术后早期功能锻炼,不仅可以促进患肢血液循环,又有利于消肿,防止肌肉萎缩,可以避免关节僵硬等作用。
1、术后在患肢小腿处垫一软枕,抬高患肢,利于患肢血液回流,使膝关节处于伸直状态,防止膝关节屈曲畸形。
2、术后用 1-2 斤冰米袋在伤口处予以局部冰敷,冰敷不仅可以起到止血的作用,而且具有消肿、止痛、促进炎症局限等作用。
3、术后 6h 进行踝泵运动,踝关节背伸、跖屈运动,每个动作坚持 5s,再放松,每天 60 次左右,踝关节旋转运动:每天 3—4 次,每次重复五遍。
4、术后第 1 天
- 上肢肌力训练:可以进行床上引体向上拉力练习。
- 下肢按摩运动,向心性按摩,先足底,再小腿,最后大腿的顺序,避开伤口,每隔半小时揉捏 5—10 分钟。
- 股四头肌收缩运动:患者卧床,收紧大腿肌肉,尽量伸直膝关节,每次 20—30 次,每日 3 次。
- 直腿抬高训练:收紧大腿肌肉,尽量伸直膝关节,用力抬高足部使其离床 30 厘米,持续 10s,慢慢放低。
- 髌骨松动术:以手指指腹或掌根推髌骨边缘,向上、下、左、右四个方向缓慢用力推动髌骨,每方向 10-20 次,2-3 次/日。
5、术后 3—5 天进行腘绳肌等长练习,患膝关节的主被动伸屈活动,促进伤口愈合,防止肌肉萎缩,改善关节活动度。
6、术后 6 天-2 周进行离床训练,健肢先离床并使足部着力,然后患肢离床,在床尾练习站立,此时重心在健肢,以后重心逐渐过渡到患肢,开始扶助行器行走,行走时健肢在前先行,患肢跟上,上床时,按相反方向进行,由患肢先上床。
7、出院指导:
- 饮食:进食高热量、高蛋白、富含纤维素、维生素丰富饮食,限制饮酒、浓茶、咖啡、辛辣等刺激性食物,以促进疾病康复,保持大小便通畅。
- 进一步加强下肢平衡训练、本体感觉、肌力训练,回家一周后可使用静态自行车进行康复训练,术后 6 周内避免跳舞、体育运动等有强度的运动。
- 股四头肌肌力训练: a、直腿抬高: 100 个/天,10 个/组,至少 3 个月。b、坐床边抬腿练习:踝部加沙袋 1-2 斤。
- 行走时应每天增加行走次数,其次才是逐渐增加行走的距离。
- 术后 1 个月、3 个月、6 个月定期复查,以后每年复查一次。



术前,患者需要做以下几点:
1、术前3天开始指导患者进行咳嗽、深呼吸练习,吸烟患者应戒烟;
2、练习床上大小便;
3、患肢进行患肢的主动运动,如进行屈膝、伸膝、大腿外展、患腿上举等动作的练习,练习使用助行器;
4、肥胖者还应适当减肥。











术后的功能锻炼对膝关节置换的患者尤为重要,它关系到术后关节功能恢复的好坏。
术后功能锻炼分早期功能锻炼(住院期间功能锻炼)和出院后功能锻炼。早期功能锻炼术后抬高双侧下肢,增加下肢回流血量。
术后第 1天,患者即可在康复医生的指导下进行趾、踝关节屈伸和小腿肌肉的主动舒缩运动及深呼吸,此后循序渐进,以不疲劳为宜;
术后2天,患者可进行关节持续被动运动锻炼,在康复医生的帮助下进行屈膝锻炼。开始从40°开始,每天增加 5~10°,
一般术后 2 周内屈膝应超过90°。在出院后的康复训练中,一般在6周内都一直要用护膝保护膝关节,锻炼也应以增加肌力为主。主动运动可以通过手力协助,协助主动屈伸膝关节。此外,患者还可以下地负重行走练习,以改善肌肉协调性,改善身体一般状况,但一定要注意保护,避免摔倒。一些膝关节不稳者可以佩戴膝关节支架或借助步行器、拐杖。
术后6个月内,应按医嘱到医院进行复查,
此后每半年去医院复查一次。



本内容转载自捷迈邦美,京东健康已获授权,未经授权,不可二次转载。如涉侵权请联系jdh-hezuo@jd.com。
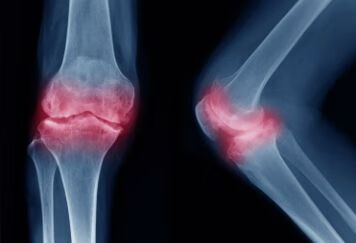
为了降低磨损,延长膝关节假体在年轻患者中的使用寿命。
1976 年,Goodfellow 和 OConner 研制 Oxford 膝关节假体,作为双髁置换假体,其特点在于股骨髁为单一矢状曲率半径,与胫骨案乙烯衬垫完匹配,聚乙烯衬垫易于在抛光的金属托上移动。膝关节的稳定由完整的交叉韧带和侧副韧带维持。这*设计聚乙烯接触应力很低,但要求所有交叉韧带和侧副韧带功能良好,易引起内衬后脱位与韧带不平衡之后,Beuchel 吸收了 Oxford 膝关节假体的特点并进行了改进,研制出低接触应力(low contact stressLCS )假体,这种假体既保持了股骨假体向后逐渐减小的曲率半径,同时金属托上的鸠尾槽样弓形沟控制了内衬的前后移动,减少了脱位的风险。
Insall 等在后交叉韧带替代型假体的基础上,研制了限制性髁假体(CCK、TC3 ),即加大了胫骨聚乙烯衬的中央柱,将其限制在加深的股骨假体中央凹槽的内外侧壁。
这种机制可控制内外翻稳定,仅允许少量内外翻扭曲。最初设计为股骨和胫骨侧采用骨水泥髓内柄,后来演变为生物型固定压配柄,以混合固定方式提高骨水泥界面强度。

1973 年,纽约特种外科医院的 Insall 等设计了全髁膝关节假体,提出了“假体符合力学因素应优于解剖复制正常膝关节运动”的动力学理念原则。受到以前 LCLH 假体设计的影响极大,切除前后叉韧带,矢状面稳定由关节面几何形状维持。全髁假体的钴铬股骨部件,带有对称的与髌骨形成关节的前翼,股骨髁后方具有在矢状面逐渐减小的曲率半径;胫骨假体的双盘状关节面在冠状面及矢状面上与股骨假体匹配度较好。假体的移位和脱位由胫骨假体前后唇和内侧突起所阻挡。胫骨假体带有髓内柄,对抗负荷不对称的假体倾斜。后来添加的金属托可均匀传导应力,防止聚乙烯蠕变。
早期的全髁型假体设计未考虑到股骨后滚,屈膝范围较小,在大约屈膝 95°时,后方股骨干与胫骨关节面将发生撞击。同时,如果屈伸间隙不完全平衡,在屈膝位有向后半脱位的倾向。为了纠正这两个问题,1978 年研制了 Insall-Burstein 后稳定设计(后交叉替代假体),即在全髁假体的几何关节面上增加了中央柱。在屈膝约 70°时,股骨假体上的凹槽咬合胫骨关节面的中央柱,引起股骨胫骨关节的接触点向后移位,产生股骨后滚效应,避免了撞击,允许进一步屈膝。目前,临床上保留和不保留后交叉韧带假体的应用已有超过 20 年的随访报道,两种假体的总体临床效果无明显差异,但关于是否保留后交叉韧带的争论仍在继续。
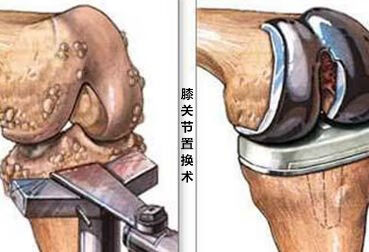
膝关节置换是一项关节置换的手术,简单的来说就是把膝关节内损坏的影响到关节正常活动的软骨,及其以下鼓面部分,代替成人工设计的假体组件,进行置换是要通过手术的方法,进行截骨植入假体,清理关节面操作膝关节置换术适用于以下患者:
- 通过正规保守治疗效果差,症状反复发作、疼痛得不到缓解,严重影响生活;
- 排除其它引起膝关节疼痛的疾病,且存在影像改变。各种类型的非感染性关节炎以及继发性骨性关节炎,造成了膝关节严重疼痛,其功能丧失是初次人工全膝关节置换术首选的适应症,包括骨性关节炎、类风湿性关节炎、强直性脊柱炎、创伤性关节炎。
- 现在高龄或更年轻的患者也被认为可以进行膝关节置换术,年龄的指征明显放宽。手术主要目的是解除关节疼痛、改善功能,手术的禁忌症包括膝关节局部或全身性感染,过度肥胖只被认为是手术相对禁忌症。
“医生只会换关节不算本事,有本事就想办法保住每一个膝关节!”
以上这句话是南京医科大学第二附属医院何斌副主任医师经常说的一句话,何主任介绍说:以前的自己也很热衷于做关节置换,因为做关节置换的病人都是症状非常严重、疼痛非常厉害的关节炎患者,这些病人通常术后效果都很好,自己做完手术也很有成就感。

只是随着自己手术做得越多,越觉得医生不应该把精力都放在做关节置换上,医生只会换关节不算本事,有本事就想办法保住每一个膝关节。毕竟膝关节置换可能会出现一些并发症,如术后顽固性疼痛、感染、假体松动、静脉血栓、切口愈合不良等等,有些并发症甚至会给病人带来灾难性的后果,而且假体也是有一定的寿命的,如果假体到了寿命再进行翻修又是一次较大的手术。

按照膝关节炎的诊疗规范,医生应该进行个体化、阶梯化的一个治疗,这就好比是一个金字塔,我们大多数人应该从底层开始进行治疗,而关节置换术是最高层,处于金字塔的塔尖,是终末期的手术,也就是说不到万不得已不做关节置换,做了就没有退路了。
何主任继续介绍说,其实我现在为病人做的一切努力就是要保住膝盖,争取让患者早诊断、早治疗,争取不做手术,如果要做,也是做修复性治疗。就好像这两天刚收了一个59岁的男性病人,是外地专程来找我的,之前他膝关节已经疼痛难忍很久,走了多家医院都建议做关节置换,我一定要把他的膝关节保住。
在做了一些辅助检查以后,何主任发现病人的膝关节内侧关节炎症较重,半月板磨损,也有少量积液,膝关节外侧炎症并不重,如果行膝关节置换就很可惜。这样的病人可以行截骨矫形治疗(胫骨高位截骨术),将胫骨上段截取一段后再进行固定,纠正膝关节的内翻畸形,从而治疗膝关节炎。
胫骨高位截骨术的手术适应症是:
患者小于65岁,女性可小于60岁;
膝关节活动度正常,至少屈膝大于100度;
仅仅是膝关节内侧的骨关节炎;
屈曲挛缩畸形小于15度,胫骨内翻畸形大于5度;
内侧胫骨近端角小于85度;
外侧软骨及半月板功能正常;
韧带存在,无关节不稳。

何主任在认真查体、仔细评估后,决定给该病人行胫骨高位截骨术,并进行了详细的术前准备工作,用心测量每一个角度,在术前就模拟出手术的整个过程,以保证手术的准确性,增加手术的安全性,缩短手术时间。何主任表示,每一个医生都应该有工匠精神,做好每一个细节。
事实证明,这样用心的去做手术,手术也一定会很成功。何主任介绍说,这个手术不仅仅是做了胫骨高位截骨,因为病人的膝关节内侧半月板也有损伤,于是同时还用关节镜微创做了半月板修整。
术后患者病情稳定,预期效果非常好。何主任最后还再次强调,医生只会换关节不算本事,有本事就想办法保住每一个膝关节!
2024年10月3日,FDA批准纳武利尤单抗(Opdivo)用于可切除非小细胞肺癌的新辅助(治疗)/ 辅助(治疗)[1]。纳武利尤单抗联合铂类双药化疗作为新辅助治疗,此后可在手术后单独使用纳武利尤单抗作为辅助治疗,用于可切除(肿瘤≥ 4cm 和/或淋巴结阳性)非小细胞肺癌 (NSCLC) 且无已知表皮生长因子受体 (EGFR) 突变或间变性淋巴瘤激酶 (ALK) 重排的成人患者。

该项获批基于Ⅲ期随机双盲试验,试验目的是围辅助治疗(新辅助治疗,然后是辅助治疗)免疫疗法是否会延长早期非小细胞肺癌患者的无事件生存期。试验主要结果主要包括无事件生存期(EFS),时间范围从随机分组至疾病进展、恶化、复发或任何原因导致的死亡(最长约 44 个月)[2]。

试验纳入了 461 例既往未经治疗且可切除的 NSCLC 患者 (IIA 期至选择 IIIB 期)。患者被随机分配 (1:1) 接受纳武利尤单抗组/对照组,接受铂类化疗,每3周一次,最多4个周期(新辅助治疗),然后继续接受纳武利尤单抗单药或安慰剂,每4周一次,最多13个周期(辅助治疗)。试验结果表明,纳武利尤单抗组未达到中位EFS (95% CI: 28.9, 不可估计 [NE]),化疗组未达到 18.4 个月 (95% CI: 13.6, 28.1) (风险比 0.58 [95% CI: 0.43, 0.78];p 值 0.00025)[2]。
安全性方面,在接受新辅助纳武利尤单抗治疗的患者中,5.3%的患者因不良反应而无法接受手术,而安慰剂组为3.5%。此外,纳武利尤单抗组接受新辅助治疗和手术的患者有4.5%因不良反应而延误手术,而安慰剂组为 3.9%[1]。
根据该药说明书,纳武利尤单抗是一种单克隆抗体,与程序性死亡受体 1 (PD-1) 或 PD 配体 1 (PD-L1) 结合的药物,阻断 PD-1/PD-L1 通路,从而消除免疫反应的抑制,可能打破外周耐受性并诱导免疫介导的不良反应。因此不良反应主要和免疫反应有关,总结如下,临床应用过程中需按医嘱用药。
A.可引起免疫介导的肺炎,发生率约为3.1%;
B.可引起免疫介导性结肠炎,发生率约为2.9%;
C.可引起免疫介导性肝炎,发生率约为1.8%
D.可导致原发性或继发性肾上腺皮质功能减退症,发生率约为1%。对于2级或更高级别的肾上腺皮质功能减退症,开始对症治疗,包括根据临床指征进行激素替代治疗。
E.可引起免疫介导的垂体炎。垂体炎可表现为与占位效应相关的急性症状,例如头痛、畏光或视野缺损。垂体炎可导致垂体功能减退症。
F.可引起免疫介导的肾炎。
G.可引起免疫介导的皮疹或皮炎,PD-1/PD-L1 阻断抗体曾发生剥脱性皮炎,包括 Stevens-Johnson 综合征、中毒性表皮坏死松解症 (TEN) 和 DRESS(伴有嗜酸性粒细胞增多症和全身症状的药疹)。
若因出现免疫反应而需停药,给予全身性皮质类固醇治疗(1 至 2 mg/kg/天泼尼松或等效药物),直到改善至1级或更低,并开始皮质类固醇减量,并在至少1个月内继续减量。对于皮质类固醇治疗无法控制免疫介导的不良反应的患者,考虑使用其他全身性免疫抑制剂。
此外,该药可引起严重的输液相关反应,在临床试验中,<1.0% 的患者报告了这种反应。对于有严重或危及生命的输液相关反应的患者,应停止使用。
参考来源:
1.FDA approves neoadjuvant/adjuvant nivolumab for resectable non-small cell lung cancer
2.A Study of Neoadjuvant Chemotherapy Plus Nivolumab Versus Neoadjuvant Chemotherapy Plus Placebo, Followed by Surgical Removal and Adjuvant Treatment With Nivolumab or Placebo for Participants With Surgically Removable Early Stage Non-small Cell Lung Cancer
3.product information:OPDIVO- nivolumab injection
2024年10月7日,卡罗林斯卡医学院决定将2024年诺贝尔生理学/医学奖共同授予给Victor Ambros和Gary Ruvkun,以表彰他们“发现microRNA及其在转录后基因调控中的作用”[1]。

Victor Ambros是在1953年12月1日出生在美国新罕布什尔州的汉诺威小镇,现就职于马萨诸塞大学医学院。Gary Ruvkun比Victor早一年出生,出生地是加利福尼亚州伯克利市,现就职于哈佛大学医学院麻省总医院。

二位诺奖得主一直专研的microRNA,通过PubMed来搜这一词,可以找到约17万条结果,其中有8000多条和癌症有关。
有助于癌症早期诊断
microRNA(miRNA)是一类进化上保守的短非编码调节RNA基因,影响miRNA 活性的无数调节机制都与致癌过程有关。差异化的miRNA表达在区分恶性与良性疾病、癌症分期、癌症分型方面已被广泛研究,在疾病诊断方面,许多研究已经证实microRNAs 在人类癌症的发病机制中起重要作用,鉴定与特定肿瘤细胞表型相关的表达模式可能为癌症的早期诊断和治疗开辟新的可能性[2]。
例如9-miRNA与早期乳腺癌患者的区域转移性疾病相关,可用于指导哪些患者在淋巴结转移风险低时可以选择不进行腋窝(前哨)淋巴结活检,哪些患者在高风险时应进行活检。在尿液样本里,两个miRNA(miR-148 和 miR-375)可以区分前列腺癌、前列腺良性病症患者以及健康人群,将这个 miRNA和血清里的前列腺特异性抗原(PSA)结合起来,诊断效果更好[3]。
在癌症治疗方面,miRNA 可用作药物或治疗靶点,很多临床前和体外实验在癌细胞里抑制了那些会致癌miRNA或者重新加入了有肿瘤抑制作用的miRNA,结果证明这些治疗方法在阻止癌细胞迁移/增殖、或者促进细胞凋亡方面很有效[4]。
miRNA新药奔向临床
越来越多miRNA药物开展临床试验,一篇发布于Cell的文章总结了进入临床试验的miRNA药物,这些药大多通过皮肤或静脉注射给药[5]。药物适应证涉及糖尿病、肺癌、心衰、肝炎和神经退行性疾病。
mRNA 药物名称 |
靶向miRNA |
作用方式 |
疾病 |
体内应用 / 细胞摄取许可 |
临床试验编号 |
AMT-130 |
人工miRNA |
amiRNA 表达 |
亨廷顿病 |
立体定向输注 / 病毒转移(腺相关载体) |
NCT04120493 |
RG - 012/ademirsen/SAR339375 |
miR - 21 |
抗miRNA |
奥尔波特综合征 |
皮下注射 / 化学修饰(硫代磷酸酯) |
NCT03373786、NCT02855268 |
RG - 125/AZD4076 |
miR - 103/107 |
抗miRNA |
2 型糖尿病 / 糖尿病前期患者的非酒精性脂肪性肝炎(NASH) |
皮下注射 / 生物分子结合(GalNAc) |
NCT02612662、NCT02826525 |
MRG - 110 |
miR - 92a |
抗miRNA |
伤口 |
皮肤注射 / 化学修饰(LNA) |
NCT03603431 |
MesomiR1 |
miR - 16 |
miRNA 模拟物 |
恶性胸膜间皮瘤、非小细胞肺癌 |
静脉注射 / 载体转移(非活性微细胞) |
NCT02369198 |
CDR132Ld |
miR - 132 |
抗miRNA |
心力衰竭 |
静脉注射 / 化学修饰(LNA) |
NCT04045405 |
RemlarsenMRG - 201 |
miR - 29 |
miRNA 模拟物 |
瘢痕疙瘩病 |
皮肤注射 / 生物分子结合(胆固醇) |
NCT02603224、NCT03601052 |
Mravrsen/SPC3649 |
miR - 122 |
抗miRNA |
慢性丙型肝炎病毒 |
皮下注射 / 化学修饰(LNA) |
NCT02508090、NCT02452814、NCT01200420、NCT01872936、NCT01727934、NCT01646489 |
MRX34 |
miR - 34a |
miRNA 模拟物 |
实体瘤(如肝细胞癌、黑色素瘤) |
静脉注射 / 载体转移(脂质体) |
NCT01829971、NCT02862145 |
RG - 101 |
miR - 122 |
抗miRNA |
慢性丙型肝炎病毒 |
皮下注射 / 生物分子结合(GalNAc) |
EudraCT 编号 2015 - 001535 - 21、2015 - 004702 - 42、2016 - 002069 - 77 |
CcbomarsenMRG - 106 |
miR - 155 |
抗miRNA |
蕈样肉芽肿 |
参考来源:
1.https://www.nobelprize.org/
2.Szczepanek J, Skorupa M, Tretyn A. MicroRNA as a Potential Therapeutic Molecule in Cancer. Cells. 2022 Mar 16;11(6):1008. doi: 10.3390/cells11061008. PMID: 35326459; PMCID: PMC8947269.
3.Sempere LF, Azmi AS, Moore A. microRNA-based diagnostic and therapeutic applications in cancer medicine. Wiley Interdiscip Rev RNA. 2021 Nov;12(6):e1662. doi: 10.1002/wrna.1662. Epub 2021 May 17. PMID: 33998154; PMCID: PMC8519065.
4.Hussen BM, Hidayat HJ, Salihi A, Sabir DK, Taheri M, Ghafouri-Fard S. MicroRNA: A signature for cancer progression. Biomed Pharmacother. 2021 Jun;138:111528. doi: 10.1016/j.biopha.2021.111528. Epub 2021 Mar 23. PMID: 33770669.
5.Diener C, Keller A, Meese E. Emerging concepts of miRNA therapeutics: from cells to clinic. Trends Genet. 2022 Jun;38(6):613-626. doi: 10.1016/j.tig.2022.02.006. Epub 2022 Mar 15. PMID: 35303998.
展开更多















